”节能减排、低碳生活”已经走进百姓生活、城市建设以及经济发展等各个领域,下列有关说法不正确的是( )

A.太阳能、地热能、核能等均属于”新能源”
B.”低碳”是指采用含碳量低的烃类化合物作燃料
C.上图中甲烷经一氯甲烷转化成低碳烯烃的途径体现了”节能减排”的思想
D.减少化石能源的使用能减少![]() 的排放量
的排放量
知识点:化学与生活
B
略
(2012安徽师大附中高三模拟)下图是氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是( )
A.氢氧燃料电池中![]() 向b极移动
向b极移动
B.该装置中只涉及两种形式的能量转化
C.电池正极电极反应式为![]() ==
==![]()
D.P型半导体连接的是电池负极
知识点:原电池
C
略
已知1 mol白磷变成红磷放出73.56 ![]() 的热量,下列两个反应
的热量,下列两个反应
![]() 白磷
白磷![]()
![]()
![]()
![]() H
H![]()
4P(红磷![]()
![]()
![]()
![]() H
H![]()
![]() H
H![]() 和
和![]() H
H![]() 的关系正确的是( )
的关系正确的是( )
A.![]() H
H![]() H
H![]() B.
B.![]() H
H![]() H
H![]()
C.![]() H
H![]() H
H![]() D.
D.![]() H
H![]() H
H![]()
知识点:化学反应的热效应
C
略
如图所示装置中,两电极上发生的电极反应分别为:a极:![]()
![]()
![]()
![]() ↑,b极:
↑,b极:![]()
![]()
![]() 则以下说法不正确的是( )
则以下说法不正确的是( )
A.该装置可能是电解池
B.溶液pH变大
C.a、b可能是同种电极材料
D.该过程中能量的转换一定是化学能转化为电能
知识点:电化学基础
D
略
(2012安徽合肥八中高三月考)已知反应:
①101 kPa时![]() ==2CO(g)
==2CO(g) ![]() H=-221
H=-221
![]()
②稀溶液中![]() ===
===![]()
![]() H=-57.3
H=-57.3 ![]()
③红磷的化学式为P,白磷的化学式为![]() 已知
已知
![]() ===
===![]()
![]() H=-3
093.2
H=-3
093.2 ![]()
4P ![]() ===
===![]()
![]() H=-2
954.0
H=-2
954.0 ![]()
下列结论正确的是( )
A.由于红磷转化为白磷是放热反应,等质量的红磷能量比白磷低
B.稀硫酸与稀NaOH溶液反应的中和热![]() H=57.3
H=57.3 ![]()
C.碳的燃烧热大于-110.5 ![]()
D.稀醋酸与稀NaOH溶液反应生成1
mol水![]() H大于-57.3
H大于-57.3 ![]()
知识点:化学反应与能量的变化
D
略
(2012河南豫南九校第一次联考)![]() 电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:
电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:![]()
![]()
![]() 含
含![]() 的导电固体为电解质。下列有关
的导电固体为电解质。下列有关![]() 电池说法不正确的是( )
电池说法不正确的是( )
A.可加入硫酸以提高电解质的导电性
B.充电时![]() 既发生氧化反应又发生还原反应
既发生氧化反应又发生还原反应
C.充电过程中,电池正极材料的质量减少
D.放电时电池正极反应为:![]()
![]()
![]()
知识点:电化学基础
A
略
已知:![]() 在水溶液中水解的热化学方程式为:
在水溶液中水解的热化学方程式为:![]()
![]()
![]()
![]()
![]() H=+a
H=+a ![]() ;稀盐酸和稀NaOH的中和热为b
;稀盐酸和稀NaOH的中和热为b ![]() 。则等物质的量的
。则等物质的量的![]() 与稀盐酸反应的
与稀盐酸反应的![]() H等于( )
H等于( )
A.+(a+b) ![]() B.+(a-b)
B.+(a-b)
![]()
C.-(a-b) ![]() D.-(a+b)
D.-(a+b)
![]()
知识点:化学反应的热效应
B
略
(2012合肥八中高三月考)如图所示是298
K时![]() 与
与![]() 反应过程中能量变化的曲线图。下列叙述正确的是( )
反应过程中能量变化的曲线图。下列叙述正确的是( )

A.该反应的热化学方程式为:![]()
![]()
![]() H=-92
H=-92 ![]()
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.在温度、体积一定的条件下,通入1
mol ![]() 和3
mol
和3
mol ![]() 反应后放出的热量为Q
反应后放出的热量为Q![]() kJ,若通入2 mol
kJ,若通入2 mol ![]() 和6
mol
和6
mol ![]() 反应后放出的热量为Q
反应后放出的热量为Q![]() kJ,则184>
kJ,则184>![]()
![]()
知识点:化学反应的热效应
D
略
已知A、B为单质,C为化合物。
![]()
能实现上述转化关系的是( )
①若C溶于水后得到强碱溶液,则A可能是Na
②若C的溶液遇![]() 能放出
能放出![]() 气体,则A可能是
气体,则A可能是![]()
③若C的溶液中滴加KSCN溶液显红色,则B可能是Fe
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则A可能是Cu
A.①② B.②④ C.①④ D.③④
知识点:元素及其化合物的综合运用
B
略
以石墨为电极,电解500 mL NaCl溶液,当两极产生气体总体积为16.8 mL时(标准状况),溶液的pH范围是( )
A.5 --6 B.7 --8 C.8-- 10 D.10 --12
知识点:电解池
D
略
(2012山西大同高三学情调研测试)Li-Al/FeS电池是一种正在开发的车载电池,该电池正极的电极反应式为:![]() ===
===![]() 有关该电池的下列说法正确的是( )
有关该电池的下列说法正确的是( )
A.LiAl在电池中作为负极材料,该材料中Li的化合价是+1价
B.充电时,阴极发生的电极反应式为:![]() ==
==![]()
C.放电时,负极的电极反应式:![]() ==
==![]()
D.该电池的电池反应式为:2Li+FeS===![]()
知识点:电化学基础
D
略
(2012河北南宫中学模拟)一种碳纳米管(氢气)二次电池原理如下图,该电池的电解质为6
![]() KOH溶液,下列说法不正确的是( )
KOH溶液,下列说法不正确的是( )

A.储存![]() 的碳纳米管放电时为负极,充电时为阴极
的碳纳米管放电时为负极,充电时为阴极
B.放电时负极附近pH减小
C.放电时电池正极的电极反应为:![]()
![]()
![]()
D.放电时,电池反应为![]()
![]()
![]()
知识点:电化学基础
D
略
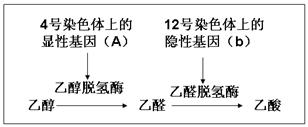
(改编题)2011年10月7日,英汤普森航空试航”地沟油”航班,在空中飞行了4个小时,并美其名”生物燃料”,该燃料属于生物质能。但有英环保组织质疑其”地沟油”成分很少,仅为”作秀”,引来一片质疑声。已知地沟油(生物质)的主要转化途径及主要产物如下图所示。

(1)下列有关说法正确的是 。
a.生物燃料本质上能量来源于太阳能
b.由纤维素水解获得的乙醇属生物质能
c.生物质裂解获得的汽油、柴油等属于纯净物
d.由植物秸秆等发酵获得的沼气,主要成分是甲烷
e.生物质资源是一种污染小的可再生能源
(2)由生物质能获得的CO和![]() 当两者1∶1催化反应,其原子利用率达100%,合成的物质可能是 。
当两者1∶1催化反应,其原子利用率达100%,合成的物质可能是 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)已知在生物质气化炉中可发生如下反应:
![]()
![]() 2CO(g)
2CO(g)
![]() H=172
H=172
![]()
![]()
![]()
![]()
![]() H=206
H=206
![]()
![]()
![]()
![]()
![]() H=165
H=165
![]()
则:![]()
![]()
![]()
![]() H=
H=
![]() 。
。
(4)已知碳的气化反应在不同温度下平衡常数的对数值(lg K)如下表:
反应:![]()
![]() 该反应的
该反应的![]() H
0(选填:”>““<“或”=”);在900 K时,该反应平衡常数的对数值(lgK)=
。
H
0(选填:”>““<“或”=”);在900 K时,该反应平衡常数的对数值(lgK)=
。
(5)燃油中所含硫以二硫醚的形式存在,工业上常用催化加氢的方法脱硫,然后综合利用生产硫酸。如二硫丙醚![]() —S—S—
—S—S—![]() 脱硫综合利用的有关反应为:
脱硫综合利用的有关反应为:
![]() —S—S—
—S—S—![]()
![]()
![]()
![]() H
H![]()
已知某些化学键的键能数据如下表:

则![]() H
H![]()
![]() 用字母式表示)。
用字母式表示)。
知识点:化学反应与能量的变化
(1)abde
(2)cd
(3)131
(4)< 0.36
(5)2f+e+3c-2b-4d
略
(2012皖南八校第一次联考)某中学课外兴趣小组用惰性电极电解饱和食盐水(含少量![]() 、
、![]() 做下列探究,装置如下图所示:
做下列探究,装置如下图所示:

根据题目信息及相关现象回答下列问题。
(1)电解时,甲同学发现电极a附近溶液出现浑浊,请用离子方程式表示原因: 。
(2)一段时间后,你认为C中溶液可能出现的现象是 ,请用离子方程式表示原因: 。
(3)实验结束后,乙同学将A中的物质冷却后加入到![]() 溶液中发现有气泡出现,但加入到稀盐酸中却没有任何现象。请用化学方程式和简要的文字解释原因
。
溶液中发现有气泡出现,但加入到稀盐酸中却没有任何现象。请用化学方程式和简要的文字解释原因
。
(4)随着反应的进行,兴趣小组的同学们都特别注意到D中溶液红色逐渐褪去。他们对溶液红色褪去主要原因提出了如下假设,请你完成假设二。
假设一:B中逸出气体与水反应生成的物质有强氧化性,使红色逐渐褪去;
假设二 : 。
(5)请你设计实验验证(4)中假设一,写出实验步骤及结论 。
知识点:综合性实验
![]()
![]()
![]() ↑
↑![]()
![]()
![]()
(2)有淡黄色沉淀 ![]()
![]()
![]()
(3)Ag置换![]() 的反应式为:
的反应式为:![]()
![]()
![]() ↑,表明
↑,表明![]() 的溶解度比AgCl小很多
的溶解度比AgCl小很多
(4)可能是![]() 中和了
中和了![]() 造成褪色
造成褪色
(5)取少量D中褪色后的溶液于试管中,滴加1--2滴酚酞溶液,如果又显红色,则假设一正确
略
电化学在生产、生活中有着极为重要的开发利用前景,下面是对电化学知识的利用,请按要求回答相关问题。

(1)某研究性学习小组为探究利用电化学原理合成氨,设计如图甲所示的装置。
①电极B为 极;电极A发生的电极反应式为 。
②该电池工作一段时间后,电解质溶液pH (填增大、减小或不变)。
(2)有人设想以如图乙所示装置用电化学原理生产硫酸,写出通入![]() 的电极的电极反应式:
。
的电极的电极反应式:
。
(3)下图所示装置中,甲池的总反应式为:
![]()
![]()
![]()
①图中甲池的装置是 。乙池中A电极的名称是 。
②写出通入![]() 的电极的电极反应式是
。
的电极的电极反应式是
。
③乙池中反应的化学方程式为 。
④当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗![]() mL(标准状况下)。
mL(标准状况下)。
知识点:电化学基础
(1)①负 ![]()
![]()
![]() ②增大
②增大
![]()
![]()
![]()
(3)①原电池 阳极
②![]()
![]()
![]()
![]()
③![]()
![]()
![]() ↑
↑![]()
④280
略
丹聂耳(Daniell)电池是由锌片和铜片两个半电池组成,锌半电池和铜半电池用盐桥连接起来,装置如图1。某化学兴趣小组提出疑问:如果将实验中的盐桥换成导线(铜制),电流表是否也偏转呢?带着疑问,该小组成员在课后立即做了如图2的实验,发现电流计指针同样发生偏转,且产生的电流较大。
试回答下列问题:


(1)对于该实验中产生电流的原因,该小组成员进行了深入的探讨,后经老师提醒注意到使用的是铜导线,烧杯Ⅰ中实验为原电池。那么在烧杯Ⅱ铜片上发生的反应为 。
(2)该小组另一成员认为如果将实验中铜导线换成铁丝,则可以明显观察到电流表的读数增大,你认为他的观点 (填”正确”或”不正确”),理由是 。
(3)对于图2中烧杯Ⅰ是原电池的问题,该小组成员产生了较大的分歧:
①一部分同学认为是由于![]() 在水溶液中水解显酸性,此时原电池实际上是由Zn、Cu作电极
在水溶液中水解显酸性,此时原电池实际上是由Zn、Cu作电极![]() 溶液作为电解质溶液而构成原电池,如果这个观点正确,那么原电池的正极反应为 。
溶液作为电解质溶液而构成原电池,如果这个观点正确,那么原电池的正极反应为 。
②另一部分同学则认为是由于溶解在溶液中的氧气的作用,使ZnCu之间形成电化学腐蚀,如果这个观点正确,那么原电池的正极反应为 。
(4)请你设计一个实验验证(3)中两个观点哪个正确。
知识点:原电池
![]()
![]() Cu
Cu
(2)正确 当铜导线换成铁丝后,恰好形成两个原电池,而且串联在同一个回路里,产生的电流会明显增大。
(3)①![]()
![]()
![]() ↑ ②
↑ ②![]()
![]()
![]()
(4)将烧杯Ⅰ中的![]() 溶液换成非酸性溶液(NaCl、KCl等),如果电流表仍然有读数,则②正确;如果没有读数,则①正确。
溶液换成非酸性溶液(NaCl、KCl等),如果电流表仍然有读数,则②正确;如果没有读数,则①正确。
略