今年3月修订的《环境空气质量标准》中新纳入的强制监测指标是(考察化学时事)
A.PM2.5
B.NOx
C.SO2
D.可吸入颗粒物
知识点:化学与社会的相互关系
A
略
下列说法中正确的是(考察原子相关知识)
A.人们已知道了107种元素,即已经知道了107种原子
B.互为同位素的原子,它们原子核内的中子数一定不相等
C.![]() 和
和![]() 原子中的中子数相等
原子中的中子数相等
D.质子数相同的微粒,核外电子数一定相同,但化学性质不一定相同。
知识点:原子结构与性质
B
略
实验室中进行粗盐提纯时,下列试剂添加过程中不符合绿色化学的是(考察粗盐的提纯)
A.BaCl2→Na2CO3 B.Na2CO3→HCl C.Na2CO3→Ca(OH)2 D.水→BaCl2
知识点:物质的分离、除杂和提纯
C
略
用化学方法鉴别HCl和氯气,不能选用的是 (考察HCl和氯气的基本性质)
A.湿润的蓝色石蕊试纸 B.湿润的红色石蕊试纸
C.硝酸银溶液 D.湿润的淀粉KI试纸
知识点:物质的检验和鉴别
C
略
砹是卤族元素中的一种,其原子序数比碘大。推测下列单质或化合物的性质中有明显错误的是
(考察卤素单质的递变规律)
A.砹单质可能为黑色的固体 B.砹的氢化物很稳定
C.砹单质不易溶于水,易溶于有机溶剂 D.砹的简单阴离子有较强的还原性
知识点:卤素
B
略
R2O8n-离子在一定条件下可以把Mn2+氧化为MnO4-离子,若反应后R2O8n-离子变成RO42-,又知反应中氧化剂与还原剂的物质的量之比为5∶2,则R2O8n-中R元素的化合价为(考察氧化还原反应的计算)
A.+5 B.+6 C.+8 D.+7
知识点:氧化还原反应
D
略
关于如图所示装置的叙述,正确的是(考察原电池相关知识)
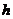
A.Zn为负极,Cu为正极
B.正极反应为 Zn-2e→![]()
C.负极反应为Cu-2e→![]()
D.该装置能将电能转化为化学能
知识点:原电池
A
略
痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中的一种,人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上。如果将溶液①小心地涂到纸上,溶液①中的溶质就跟汗渍中的物质②作用,生成物质③,物质③在光照下,分解出的银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由棕色变成黑色的指纹线。用下列化学式表示这三种物质都正确的是(考察氯、溴、碘离子的性质)A
A.①AgNO3 ②NaCl ③AgCl B.①AgNO3②NaBr ③AgBr
C.①AgNO3 ②NaI ③AgI D.①AgCl ②AgNO3 ③NaCl
知识点:卤素
A
略
根据下列热化学方程式,判断氢化物的稳定性顺序正确的是
![]() N2(g) +
N2(g) +![]() H2(g) —— NH3(g) + 46.19 kJ
H2(g) —— NH3(g) + 46.19 kJ
![]() H2(g) +
H2(g) +![]() Cl2(g) —— HCl(g) + 92.3 kJ
Cl2(g) —— HCl(g) + 92.3 kJ
![]() I2(g) +
I2(g) +![]() H2(g) —— HI(g) -25.96 kJ (考察热化学方程式)
H2(g) —— HI(g) -25.96 kJ (考察热化学方程式)
A. HCl![]() NH3
NH3![]() HI B.HI
HI B.HI![]() HCl
HCl![]() NH3 C.
HCl
NH3 C.
HCl![]() NH3 D.NH3
NH3 D.NH3![]() HI
HI![]() HCl
HCl
知识点:分子结构与性质
A
略
氮化硅(Si3N4)是一种新型的耐高温耐磨材料,在工业上有广泛用途,它属于(考察化学键及晶体)
A.原子晶体 B.分子晶体 C.金属晶体 D.离子晶体
知识点:晶体结构与性质
A
略
下列化合物可由两种单质直接化合得到的是(考察氮、硫的化合物的性质)
A.H2S B.NO2 C.CuS D.FeCl2
知识点:元素及其化合物的综合运用
A
略
某金属单质跟一定浓度的硝酸发生反应,假定只有单一的还原产物,当参加反
应的单质与被还原的硝酸的物质的量之比是2:1,还原产物是(考察硝酸的相关计算)
A.NO2 B.NO C.N2O D.N2
知识点:氧化还原反应
C
略
常温下某溶液中由水电离的c(H+) = 1×10-10 mol/L,该溶液中溶质不可能是(考察pH知识)
A.NaHSO4 B.Al2(SO4)3 C.NaOH D.HCl
知识点:水的电离和溶液的酸碱性
B
略
有关合成氨工业的说法中,正确的是(考察化
工的知识)
A.从合成塔出来的混合气体,其中氨气只占15%,所以生产氨的工厂的效率都很低。
B.由于氨易液化,氮气、氢气在在实际生产中是循环使用,所以总体来说氨的产率很
高。
C.合成氨工业的反应温度控制在500℃,目的是使化学平衡向正反应方向方向移动。
D.合成氨厂采用的压强是2×107Pa ~ 5×107Pa,因为该压强下铁触媒的活性最大。
知识点:化学与技术
B
略
在PH = 1无色透明溶液中能大量共存的离子组是(考察离子共存的知识)
A. Al3+、Ag+、NO3-、Cl- B.Mg2+、NH4+、NO3-、Cl-
C. Ba2+、K+、S2-、Cl - D.Cu2+、Na+、NO3-、SO42-
知识点:离子共存
B
略
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是(考察图像知识)


A.反应的正方向吸热(t2时升温) B.H2S气体通入氯水中![]()
![]()
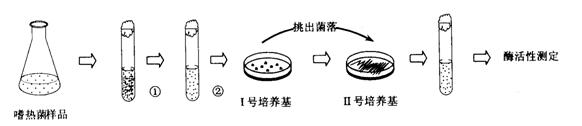
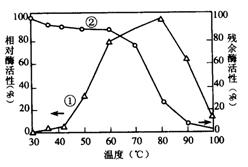
C. t秒时合成氨反应达到平衡
D. NaOH溶液滴入Ba(HCO3)2溶液中![]()
知识点:基本概念、基本理论的综合运用
C
略
下列离子方程式的书写正确的是(考察离子方程式的书写)
A.实验室用浓盐酸与MnO2反应制Cl2:MnO2 +2H++2Cl- →Cl2↑+Mn2+ +H2O
B.将标准状况下1.12 L氯气通入10 mL 1 mol / L的溴化亚铁溶液中:
2Fe2++4Br-+3Cl2 →2Fe3++6Cl-+2Br2
C.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:
Ca2++ HCO3- +OH- →CaCO3↓+H2O
D.向Fe(OH)3悬浊液中加入氢碘酸: Fe(OH)3 + 3H+→Fe3+ + 3H2O
知识点:离子方程式
B
略
我国的四大发明之一黑火药,爆炸时反应放出大量热,常用于军事与烟火,后传入欧洲。请根据反应中的元素回答下列问题:
⑴.右图所示为元素周期表中钾元素框图,数据“39.10”表示的是____________;钾元素的原子结构示意图是___________________。
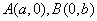
⑵.写出题干所描述的化学反应方程式_____________________________________。
⑶.上述方程式的元素中,简单离子组成与氩原子相同的是_____________;已知硫的相关化合物亚硫酸能与氯单质反应,写出亚硫酸的电离方程式____________________。
⑷.题干描述反应的生成物中,属于非电解质的是_________________(写化学式),熔点最高的物质的电子式是______________。
知识点:基本概念、基本理论的综合运用
⑴. 钾元素的(平均)相对原子质量 ;略;
⑵. S + 2KNO3 + 3C → K2S + 3CO2↑+ N2↑
⑶. S与K(2分);H2SO3 ![]() H+
+ HSO3—(合理即可);
H+
+ HSO3—(合理即可);
⑷.CO2,![]() ;
;
略
BCl3是重要的化工原料,其沸点12℃。500℃时,向2L的密闭容器中按一定比例投入B2O3、C、Cl2,模拟工业制取三氯化硼的反应如下:B2O3(s)
+ 3C(s) + 3Cl2(g) ![]() 2BCl3 (g) + 3CO(g)。
2BCl3 (g) + 3CO(g)。
⑴.反应起始至3min时固体质量减少了15.9克,则氯气的平均反应速率为_____________。
⑵.反应至4min时达到平衡,则下列说法正确的是______(填序号)。
a. 3min时,CO的消耗速率大于氯气的消耗速率
b. 2min至4min时BCl3的生成速率比0至2min时的快
c. 反应起始至平衡,气体的密度不断增大
d. 达到平衡后,容器内的压强不再变化
⑶.达到平衡后,若向容器内加入少量的B2O3 ,则该反应的平衡将______(填:向正反应方向、向逆反应方向、不移动);若提高反应体系的温度,容器内的气体平均分子量减小,则该反应为_____(填:“吸”、“放”)热反应。
⑷.若要提高单位时间内BCl3的产量,且保持温度不变,下列做法正确的是_____(填序号)。
a. 增大反应容器的体积 b. 将经冰水浴冷却后的混合气体,循环进入反应容器
c. 加入适当的催化剂 d. 加入适量的B2O3(g)
知识点:化学平衡状态及移动
⑴. 0.075 mol/(L·min);
⑵. cd;
⑶. 不移动;吸(注:用极值法。全为氯气,式量71;全是BCl3、CO,平均式量63.8);
⑷. c
略
某学生做了如下实验:
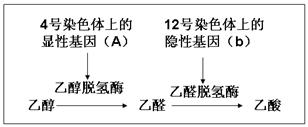
实验一:向含10 mol KI的硫酸溶液中逐滴加入高锰酸钾溶液。整个过程中含碘物质与加入高锰酸钾的物质的量的关系如图。
⑴.a→b过程中,被氧化的元素为_____,b点生成的含碘物质为_____,转移电子______mol。(提示:为逐步氧化。)
⑵.已知在b→c过程中,酸性条件下MnO4— 转变为Mn2+,生成的含碘物质为IO3—,写出相应的离子反应方程式_____________________________ _______。
实验二:向KI和硫酸混合溶液中加入过氧化氢溶液,迅速反应放出大量气泡,溶液呈棕色。
查阅资料知,反应过程如下:① H2O2 + 2KI + H2SO4 → I2 + K2SO4 + 2H2O;
② H2O2 + I2 → 2HIO; ③ H2O2 + 2HIO → I2 + O2↑+ 2H2O
⑶.上述实验过程②与③中,I2起到了____________的作用。
⑷.试判断,酸性条件下HIO、H2O2、O2三种物质氧化性的强弱:____________(填化学式)。
知识点:氧化还原反应
⑴.![]() (-1价的碘);I2,10;
(-1价的碘);I2,10;
⑵. 2MnO4— + I2 + 4H+ → 2Mn2+ + 2IO3— + 2H2O
⑶. 催化剂;
⑷. H2O2 >HIO>O2,强调,氧化性:氧化剂>氧化产物);注,反应③不能说明氧
化性HIO>H2O2,该反应与Na + KCl→NaCl+K↑类似,O2为气体,离开反应体系。)
略
化学实验在化学学习中有着举足轻重的地位,请根据要求完成下列填空:
甲:右图是实验室制取HCl气体并验证气体性质的装置图。
⑴.玻璃仪器A的名称是 。B瓶中浓硫酸的作用是 。
⑵.C瓶中观察到的实验现象是 ,
反应的化学方程式是 。
⑶.证明HCl气体中含有氯元素的实验方法和现象是
。
乙:实验室若欲制取少量的硝酸。
⑷.写出相应的化学反应方程式: 。
⑸.乙实验在制取硝酸的过程中,下列说法有误的是
A.用NaOH溶液吸收多余的硝酸蒸汽 B.欲获得干燥的硝酸,可用碱石灰干燥
C.制备的装置可采用甲实验装置的A、B、C D.收集的硝酸蒸汽可能带有棕黄色
知识点:物质的制备
⑴. 圆底烧瓶 ;干燥氯化氢气体
⑵. 有白烟产生 NH3+ HCl→NH4Cl
⑶. 将气体通入硝酸银溶液中,有白色沉淀产生
⑷. NaNO3+H2SO4(浓) → NaHSO4+HNO3↑
⑸. BC
略
如图是实验室制取Cl2,并用Cl2与红热的炭反应的装置

⑴.A中是MnO2和浓盐酸反应生成Cl2的装置。该反应的化学方程式_____________________。
⑵.装置a的名称是__________________,装置C的名称是____________。
⑶.实验操作:①检查装置___________。②装入药品后,打开活塞K,点燃A处酒精灯,至_____________________________(填现象)后,再点燃D处酒精灯。③D处反应完毕后,关闭活塞K,再移去A、D两处酒精灯。由于余热的作用,A处仍然产生少量Cl2,此时观察到B瓶中的现象是______________________。
⑷.D处氯气和炭等反应生成CO2和HCl,写出D处反应的化学方程式________________。
⑸.B瓶中饱和食盐水的作用_______________________________________,C瓶中水的作用________________________。
⑹.E处石蕊的现象_________________,E中倒放的漏斗所起的作用_____________________。
⑺.若将E处溶液改为澄清石灰水,是否有白色沉淀?_____(填“有”或“没有”),其原因是______________________________________________________________。
知识点:物质的制备
⑴. MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
⑵. 长颈漏斗; 洗气瓶(集气瓶;细口瓶、广口瓶不可,因为其不能作为反应器)。
⑶. ①气密性。②装置中充满黄绿色气体。③长颈漏斗a中液面上升。。
⑷. 2Cl2+C+2H2O ![]() CO2+4HCl。
CO2+4HCl。
⑸. 除去氯气中的氯化氢;提供水蒸气。
⑹. 紫色变红色; 防止溶液倒吸。
⑺. 没有;生成的HCl会将沉淀CaCO3溶解。
略