环境污染已成为人类社会面临的重大威胁,各种污染数不胜数。下列名词与环境污染无关的是①温室效应②赤潮③酸雨④光化学污染⑤臭气空洞⑥水俣病⑦潮汐⑧大脖子病⑨水华
A.②⑨ B.⑦⑧ C.⑥⑦⑧ D.②⑤⑦ 答:
知识点:化学与生活
B
略
H-离子可以跟NH3反应:![]() ,根据该反应事实,可以得出的正确结论是
,根据该反应事实,可以得出的正确结论是
A.NH3具有还原性 B.H-是很强的还原剂
C.H2既是氧化产物又是还原产物 D.该反应属于置换反应 答:
知识点:氧化还原反应
BC
略
设NA为阿佛加德罗常数,下列说法正确的是
A. 标准状况下,22.4LCO2与CO的混合气体中含有1mol碳原子
B. 活泼金属与盐酸反应,每放出1molH2,其电子转移的数目为NA
C. 由生石膏加热失去结晶水生成1mol熟石膏时,生石膏失去的结晶水分子数为3NA
D. 常温常压,22.4LN2所含的分子数多于NA个 答:
知识点:化学中常用计量
AC
略
在一定温度下,有A、B两个容器,A是恒容密闭容器,B是恒压密闭容器。两容器起始状态完全相同,其中都充有NO2气体,如果只考虑发生下列可逆反应:
![]() 2NO2
N2O4,分别经过一段时间后,A、B都达到平衡。下列有关叙述正确的是
2NO2
N2O4,分别经过一段时间后,A、B都达到平衡。下列有关叙述正确的是
A.平衡反应速率:A>B B.平衡时NO2物质的量:B>A
C.平衡时NO2的转化率:A>B D.平衡时N2O4物质的量:B>A 答:
知识点:化学平衡状态及移动
D
略
日常所用干电池其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2氧化吸收H2),电极反应可简化为:![]() ,
,![]() (NH3再用于结合Zn2+)。根据上述叙述判断下列说法中正确的是
(NH3再用于结合Zn2+)。根据上述叙述判断下列说法中正确的是
A. 干电池中Zn为正极,碳为负极
B. 干电池工作时,电子由碳极经外电路流向Zn极
C. 干电池长时间连续使用时内装糊状物可能流出腐蚀电器
D. 干电池可以实现化学能向电能的转化和电能向化学能的转化 答:
知识点:原电池
C
略
某温度下,Wg下列物质在足量的O2中充分燃烧,其燃烧产物立即与过量的Na2O2固体反应,该固体增重也是Wg,符合此要求的是
①H2 ②CO ③CO、H2混合气 ④HCHO ⑤CH3COOH
A.①②③ B.①②③④ C.④⑤ D.①②③④⑤ 答:
知识点:钠和碱金属
D
略
在铁与铜的混合物中,加入不足量的稀硝酸,反应后剩余金属m1g;再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2g,则m1与m2之间的关系是
A.m1一定大于m2 B.m1可能等于m2
C.m1一定等于m2 D.m1可能大于m2 答:
知识点:氮族元素
A
略
在重铬酸钾(K2Cr2O7)溶液中存在如下平衡:![]()
![]()
![]()
![]()
![]() ,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
A.Ag2Cr2O7 B.Ag2CrO4 C.AgHCrO4 D.Ag2O 答:
知识点:溶解平衡
B
略
现有1L含SO3为30%的发烟硫酸(ρ=1.95g/cm3),要把它稀释成浓度为95%的浓H2SO4,应将它缓缓加入水中,水的体积是
A.120mL B.180mL C.240mL D.300mL 答:
知识点:氧族元素
C
略
工业上制备HNO3的尾气中,尚含有少量未被吸收的NO和NO2,如果不加处理就排放到空气中,会造成污染。为消除氮的氧化物对大气的污染,变废为宝,常用碱兴吸收尾气中氮的氧化物,使之转化为相应的硝酸盐。亚硝酸盐和水。依据上述原理,判断下列混合气体不可能被NaOH溶液完全吸收的是
A.1molO2和4molNO2 B.1molNO和4molNO2
C.1molO2和4molNO D.4molNO和4molNO2 答:
知识点:氮族元素
D
略
将一定量的锌与100mL 18.5mol/L浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的pH=1,则下列叙述中错误的是
A. 气体A为SO2和H2的混合物
B. 气体A中SO2与H2的体积比为4︰1
C. 反应中共消耗Zn97.5g
D. 反应中共转移电子3mol 答:
知识点:氧族元素
B
略
元素X能分别和B、N、O形成二元化合物,在这些二元化合物中各元素的质量分数分别是:B:16.2%;N:19.7%;O:29.7%。它们的相对分子质量分别是54、68和71(未按顺序),则下列说法正确的是
A.X可能是氟元素 B.X可能是金属元素
C.X可能是氢元素 D.仅依据上述条件还不能确定X是何种元素 答:
知识点:卤素
A
略
三甲苯和甲乙苯分子式都是C9H12,其同分异构体共有6种。其中有n种异构体将它们分别进行一硝化(即:向分子中苯环上导入一个硝基),都分别只能得到两种异构体产物(C9H11NO2)。则n等于
A.0 B.1 C.2 D.3 答:
知识点:芳香烃 石油 苯 煤
C
略
在下面的分子结构式中,哪个说法是正确的
A.
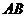 所有的碳原子有可能处在同一个平面上
所有的碳原子有可能处在同一个平面上
B. 所有的碳原子不可能处在同一个平面上
C. 所有的氧原子有可能同时处在苯环平面上
D. 所有的氢原子有可能同时处在苯环平面上 答:
知识点:乙醇和醇类
AC
略
(22分)工业产品碳酸钠中,常混有氯化钠,测定碳酸钠质量分数的仪器装置图如下:
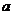
供选用的试剂有:NaOH溶液、饱和石灰水、蒸馏水、浓硫酸、稀硫酸、浓盐酸。稀盐酸、硝酸、碱石灰、无水氯化钙、无水硫酸铜、试样(含有少量氯化钠的碳酸钠)。
请回答:(1)各有关仪器中使用的药品及作用:
A. ,作用
B. ,作用
C. ,作用
D. ,作用
E. ,作用
F的作用
(2)实验步骤(到得到实验数据止)
① 称量:称试样质量及装有干燥剂的球形干燥管的质量,并记录数据。
②
③
![]()
知识点:物质的检验和鉴别
(22分)
(1)(12分)
A.饱和石灰水或NaOH溶液(1分); 吸收空气中的CO2(1分);
B.试样(1分); 产生CO2(1分);
C.稀硫酸(1分);【盐酸得0分】 使试样转化成CO2(1分);
D.浓硫酸(1分); 干燥CO2气体(1分);
E.碱石灰(1分); 吸收反应产生的CO2(1分);
F.第一次鼓空气,以赶尽仪器装置中有CO2的空气(1分);
第二次鼓空气,赶出残留在仪器装置中反应产生的CO2(1分);
(2)(10分)
②在接球形干燥管前,先检查装置的气密性;
③有关仪器中装上药品待用;
④打开甲、乙弹簧夹,用气唧鼓气,以赶尽装置中的CO2,然后接上已称量过装有吸收剂的球形干燥管;
⑤关闭甲弹簧夹,将分液漏斗中的稀硫酸加到装有试样的平底烧瓶中;
⑥反应完全后,打开弹簧夹甲,用气唧鼓气,直至装置中的CO2全部赶出为止;
⑦称量干燥管质量并记录数据。
本小题评分原则:
(1) 顺序错误扣3分;
(2) 未除装置中空气里的CO2扣3分;
反应完全后未赶尽装置中的CO2扣3分;
略
(12分)已知:A—H中均含有A元素。它们的转化关系如下图所示
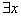
试写出下列物质的化学式:
A B C D
E F G H
并写出下列反应的化学方程式:
(1) D+A:
(2) G+HNO3(稀):
知识点:无机框图推断
(12分)
A S ; B H2S ; C SO2 ; D Na2SO3 ;
E Na2S2O3 ; F Ag2S2O3 ; G Ag2S ; H Na2S ; (每空1分)
(1)![]() (2分)
(2分)
(2)![]() (2分)
(2分)
略
(12分)烯烃中的烯键可以被(1)臭氧化(2)NaBH4还原,反应结果烯键断裂,两端
(乙醇)
碳原子都连上了羟基,例如:
(异丙醇)
某二烯烃A(分子式C10H18),经(1)臭氧化(2)NaBH4,得到2mol异丙醇和1mol某种二元醇B(C4H10O2),A的可能结构式共有多少种?如果其中之一的结构简式和键线式是:
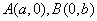
![]()
其名称为2,7-二甲基-2,7-辛二烯。
请写出A的其它的所有可能结构的键线式,并一一命名之。
知识点:有机化合物的分类、命名与结构特点
(12 分)
有5种(2分),
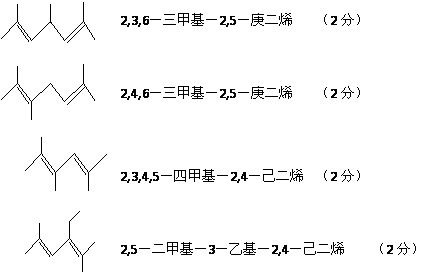
如果不用键线式,则各式各扣1分。4种全对共给10分(含奖励分2分)
略
(12分)虽然分子中同一碳原子同时连接两个OH的化合物容易失水成为羰基(C=O)而无法分离,但是,一个碳原子同时连两个OR基或一个OR、一个OH基的化合物(称作缩醛、半缩醛)却是可以存在的。
RCHO+H2O![]() RCH(OH)2 不安定
RCH(OH)2 不安定
酸催化
R′OH过量,酸催化
稀酸
稀酸
半缩醛
缩醛
(在碱中安定,可以分离出来)
请写出下列反应式中A、B、C、D、E的结构式
![]()
酸
![]() (1) +C2H5OH A
(1) +C2H5OH A
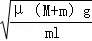
![]()
酸
![]()
酸
稀酸
△
稀酸
![]()
△
(5)E(C9H18O3) CH3CH2COOH+CH3CH2CHO+CH3CH2CH2OH知识点:有机合成及高分子化合物
(12分)
(1)A (2分) (2)B (2分)
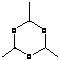 |
|||
(3)C (2分) (4)D (3分)
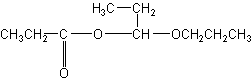 |
(5)E (3分)
略
(10分)
(1)写出实验中的关键反应(写出离子方程式并配平)。
(2)根据实验数据计算Na2S2O3标准溶液的浓度(要求四位有效数字)
实验:称取样品0.1389gK2Cr2O7于250mL碘瓶(带磨口塞的锥形瓶)中,用少量蒸馏水使其溶解,加入1gKI和10mL 6mol/LHCl,反应中,![]() 转化为
转化为![]() ,盖好瓶塞充分混合后,放在暗处5分钟,然后用蒸馏水稀释至100mL,在不停摇动下用标准Na2S2O3溶液滴定至溶液由棕色变为淡黄色(I2和Na2S2O3发生氧化还原反应生成Na2S4O6),加入2mL0.5%淀粉(指示剂)继续摇动滴定至溶液蓝色消失为止,读得Na2S2O3溶液消耗的体积为25.02mL。(K2Cr2O7的式量请用:294.18)
,盖好瓶塞充分混合后,放在暗处5分钟,然后用蒸馏水稀释至100mL,在不停摇动下用标准Na2S2O3溶液滴定至溶液由棕色变为淡黄色(I2和Na2S2O3发生氧化还原反应生成Na2S4O6),加入2mL0.5%淀粉(指示剂)继续摇动滴定至溶液蓝色消失为止,读得Na2S2O3溶液消耗的体积为25.02mL。(K2Cr2O7的式量请用:294.18)
知识点:溶液浓度的计算
(10分)①![]()
![]() (2分)
(2分)
![]()
![]() (2分)
(2分)
②![]()
![]() (6分)
(6分)
略
(12分)取25.0gCuSO4·5H2O晶体,加热使之均匀、缓慢升温至1000℃并恒温1小时,试通过计算回答下列问题(如果是混合物,要算出混合物中各组分的质量):
(1)在某中间温度时,固体产物质量是否可能为10g?
(2)不考虑实验带来的误差,在反应条件下,反应气态产物除去水后,物质的量可能为
A.0mol B.0.1mol C.大于0.1mol
(3)你认为最终固体产物为多少克?产物颜色如何?
(4)如果某同学做此实验时最后固体质量为7.6g,试计算其组分。
知识点:铜及其化合物
(12分) (1)可能(1分) 产物中有CuO(6g),CuSO4(4g) (2分)
![]()
![]()
(2)C;(1分)
气体产物除去水后应大于0.125mol,原因如下:(1分)
![]() (1分)
(1分)
2SO3
![]() 2SO2+O2↑ (1分)
2SO2+O2↑ (1分)
(3)7.2g(2分) 红色(1分)
(4)Cu2O (3.6g),CuO (4g) (2分)
略
(10分)已知2-丁烯有顺、反两种异构体,前者能量比后者高(△G°),在某反应条件下它们处于平衡,其平衡常数K平如下:
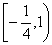
![]()
顺-2-丁烯 反-2-丁烯
自由能差△G°和平衡常数K平有如下关系
△G°=-RTlnK平=-2.303RTlogK平
式中R=8.31J/K·mol,T=298K
试 (1)求该平衡时,顺反式的摩尔分数(物质的量分数)
(2)求顺、反式的自由能差(请用kJ/mol表示)。
(答数均取3位有效数字)
知识点:有机计算
(10分)设此时顺式、反式分别为x和1-x
则:![]()
答:此时顺式为23.8%,反式为76.2% (5分)
或答:顺︰反=0.312︰1 或反︰顺=3.20︰1 都对
△G°=-2.303×8.31×298×0.505=2880J/mol=2.88kJ/mol (5分)
略