 www.ks5u.com下列物质属于纯净物的是()
www.ks5u.com下列物质属于纯净物的是()
A.氯化钠 B.氨水 C.漂白粉 D.碘酒
知识点:物质的分类
A
考点:混合物和纯净物.
分析:纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质,据此结合常见物质的组成成分逐项分析即可.
解答:解:A、氯化钠只有一种物质,属于纯净物,故A选;
B、氨水中含有氨气分子、水,属于混合物,故B不选;
C、漂白粉中含有次氯酸钙、氯化钙等多种物质,属于混合物,故C不选;
D、碘酒中含有碘单质和水,属于混合物,故C不选;故选A.
点评:解答本题要充分理解纯净物和混合物的区别,要分析物质是由几种物质组成的,如果只有一种物质组成就属于纯净物,如果含有多种物质就属于混合物.
如果你在厨房不小心将花生油与凉开水混在一起,你将采用下列何种方法进行分离()
A.过滤 B.蒸馏 C.分液 D.萃取
知识点:物质的分离、除杂和提纯
C
考点:分液和萃取.
专题:化学实验基本操作.
分析:过滤适用于固液混合物的分离,蒸馏适用于沸点不同的液体混合物的分离,分液适用于互不相溶的液体,萃取是利用溶质在不同溶剂中的溶解度不同的分离方法.
解答:解:花生油和水互不相溶,可用分液方法分离,
故选C.
点评:本题考查物质的分离,题目难度不大,注意常见物质的分离方法和操作注意事项.
根据厦门气象台报道,近年每到春季,厦门市经常出现大雾天气,致使高速公路关闭,航班停飞.雾属于下列分散系中的()
A.溶液 B.悬浊液 C.乳浊液 D.胶体
知识点:分散系
D
考点:分散系、胶体与溶液的概念及关系.
分析:根据常见的胶体有淀粉溶液、冬天的大雾、牛奶、鸡蛋(蛋白质溶液)溶液、Al(OH)3胶体、Fe(OH)3胶体等.
解答:解:分散质粒子直径在1nm~100nm之间的分散系属于胶体,胶体具有丁达尔现象,大雾时,用灯照射时会出现一条光亮的通路,则雾属于胶体分散系,故选:D.
点评:本题考查学生题考查学生教材知识的记忆熟练程度,可以根据所学知识进行回答,记住常见的胶体是解题的关键,题目较简单.
在地壳中含量最多的金属元素是()
A.铁 B.氧 C.硅 D.铝
知识点:镁铝及其化合物
D
考点:金属冶炼的一般原理.
专题:金属概论与碱元素.
分析:根据地壳中含量最多的前五种元素和金属元素的判断方法考虑.
解答:解:地壳中含量最多的前五种元素:氧、硅、铝、铁、钙,汉字中带钅字旁(汞和金除外)的属于金属元素,所以地壳中含量最多的金属元素是铝.
故选D.
点评:解答本题关键是要知道金属元素的判断方法,掌握地壳中含量最多的前五种元素.
实验室中,通常将金属钠保存在()
A.水中 B.煤油中 C.四氯化碳中 D.汽油中
知识点:钠和碱金属
B
考点:钠的化学性质.
专题:几种重要的金属及其化合物.
分析:根据钠的保存需要考虑钠的性质,如钠与空气和水发生反应,与四氯化碳、汽油、煤油不反应,钠的密度比四氯化碳小、比煤油、汽油的密度大以及汽油的沸点低于煤油,易挥发.
解答:解:A、金属钠和水之间能反应,所以不能保存在水中,故A错误;
B、金属钠与煤油不反应,且密度比煤油大,沉于煤油底部,隔开了空气,所以钠能保存在煤油中,故B正确;
C、金属钠与四氯化碳不反应,但密度比四氯化碳小,浮于煤油,能接触到空气,所以钠不能保存四氯化碳中,故C错误;
D、金属钠与汽油中不反应,密度比汽油大,沉于煤油液面,但汽油的沸点低于煤油,易挥发,所以钠不能保存汽油中,故D错误;
故选:B.
点评:金属的保存需要考虑金属的物理性质和化学性质.
下列物质中,属于不合金的是()
A.水银 B.黄铜 C.钢铁 D.生铁
知识点:元素及其化合物的综合运用
A
考点:生活中常见合金的组成.
分析:合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质;合金具有以下特点:①一定是混合物;②合金中各成分都是以单质形式存在;③合金中至少有一种金属,④合金的硬度大,熔点低.据此分析解答.
解答:解:A.水银是金属汞单质,不是混合物,不属于合金,故A错误;
B.黄铜是铜和锌的合金,故B正确;
C.钢铁是含碳量质量百分比低于2%的铁碳合金,故C正确;
D.根据铁中含有的碳的质量分数的大小,把铁的合金分为生铁和钢;含碳量在2%~4.3%之间的属于生铁,故D正确;
故选A.
点评:本题主要考查了合金的判别,掌握合金的概念及特征是解答的关键,题目较简单.
NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,下列分类标准不正确的是()
A.可与硝酸反应 B.钠的化合物 C.可溶于水 D.电解质
知识点:物质的分类
A
考点:钠的重要化合物;电解质与非电解质.
分析:A.氯化钠、硫酸钠均不能与硝酸反应;
B.依据各种物质是否含钠元素分类;
C.依据物质的溶解性;
D.依据电解质的概念:在溶液中或熔融状态下能导电的化合物是电解质判断解答.
解答:解:A.氯化钠、硫酸钠均不能与硝酸反应,故A错误;
B.NaOH、Na2CO3、NaCl、Na2SO4都含有钠元素,都是化合物,故B正确;
C.NaOH、Na2CO3、NaCl、Na2SO4都易溶于水,故C正确;
D.NaOH是碱、Na2CO3、NaCl、Na2SO4是盐,溶于水,自身都能电离出离子,使溶液导电,都属于电解质,故D正确;
故选:A.
点评:本题考查了物质的分类,明确物质的性质、电解质的概念是解题关键,题目难度不大.
下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是()
①Na2CO3 ②Al2O3 ③Al(OH)3 ④Al.
A.③④ B.②③④ C.①③④ D.全部
知识点:镁铝及其化合物
B
考点:两性氧化物和两性氢氧化物.
专题:几种重要的金属及其化合物.
分析:根据物质间的反应进行判断,中学常见的既能与酸反应又能与碱反应的物质主要有:
①两性物质:Al2O3、ZnO、Al(OH)3、Zn(OH)2、氨基酸、蛋白质等;
②多元弱酸的酸式盐:NaHCO3、KHS、KHSO3、NaH2PO4等;
③弱酸的铵盐及其酸式盐:(NH4)2S、NH4HS、(NH4)2CO3、NH4HCO3、CH3COONH4等;
④某些具有两性的金属:Zn、Al等;
⑤某些非金属:Si、S等;
⑥其它一些物质.如:a、某些盐类物质既与酸反应,又与碱反应;
b、个别酸性氧化物SiO2;
c、具有还原性的无氧酸:H2S、HI等与氧化性酸反应、与碱反应;
d、具有氧化性酸:浓H2SO4、HNO3等与还原性酸反应、与碱反应,以此解答本题.
解答:解:①Na2CO3与盐酸反应生成氯化钠、二氧化碳与水,不能与氢氧化钠反应,故C①不符合;
②Al2O3是两性氧化物,溶于强酸强碱,和盐酸反应生成氯化铝和水,与氢氧化钠溶液反应生成偏铝酸钠和水,故②符合;
③氢氧化铝是两性氢氧化物,能与盐酸反应生成氯化铝与水,与氢氧化钠反应生成偏铝酸钠与水,故③符合;
④Al与盐酸反应生成氯化铝和氢气,和氢氧化钠溶液反应生成偏铝酸钠和氢气,故④符合;
故选B.
点评:本题考查了物质的性质,难度不大,旨在考查学生对知识的理解识记与知识归纳,明确物质的性质是解本题的关键,注意基础知识的积累.
氧化还原反应的实质是()
A.氧元素的得失 B.化合价的升降
C.电子的转移 D.原子的重新组合
知识点:氧化还原反应
C
考点:氧化还原反应.
分析:氧化还原反应的特征为化合价的升降,其实质为电子的转移,以此来解答.
解答:解:A.氧化还原反应不一定有氧元素参加,如氢气和氯气的反应,故A错误;
B.元素化合价变化为氧化还原反应的特征,故B错误;
C.电子的转移为氧化还原反应的实质,故C正确;
D.原子重新组合时一定发生化学反应,但不一定为氧化还原反应,故D错误.
故选C.
点评:本题考查氧化还原反应的实质,明确实质为电子的转移,特征为化合价的升降即可解答,题目较简单.
下列金属只能与高温水蒸气反应而不与热水反应的是()
A.Ca B.Mg C.Fe D.Cu
知识点:铁及其化合物
C
考点:铁的化学性质.
分析:A.Ca为活泼金属,既可以与水反应,更可以与高温水蒸气反应;
B.Mg为活泼金属,既可以与热水反应,更可以与高温水蒸气反应;
C.Fe为较活泼金属,不与热水反应,可以与高温水蒸气反应;
D.Cu为不活泼金属,既不与热水反应,也不与高温水蒸气反应;
解答:解:A.Ca为活泼金属,既可以与水反应,更可以与高温水蒸气反应,故A不选;
B.Mg为活泼金属,既可以与热水反应,更可以与高温水蒸气反应,故B不选;
C.Fe为较活泼金属,不与热水反应,可以与高温水蒸气反应生成四氧化三铁和氢气,故C选;
D.Cu为不活泼金属,既不与热水反应,也不与高温水蒸气反应,故D不选;
故选C.
点评:本题考查金属的活泼性,侧重与热水以及水蒸气反应考查,为高考常见题型,把握几种常见金属的性质为解答的关键;
向紫色石蕊溶液中加入过量Na2O2粉末,振荡,正确的叙述是()
A.最后溶液变蓝色
B.溶液先变蓝色最后褪色
C.溶液仍为紫色
D.因为Na2O2与石蕊发生氧化还原反应而无气泡产生
知识点:钠和碱金属
B
考点:钠的重要化合物.
专题:元素及其化合物.
分析:过氧化钠与水反应生成NaOH和氧气,并且Na2O2具有强氧化性,能使紫色溶液褪色,以此解答.
解答:解:过氧化钠与水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑,溶液中有气泡产生,过氧化钠过量,且有强氧化性,能使紫色石蕊溶液因氧化而褪色,溶液最终变为无色.
故选B.
点评:本题考查过氧化钠的性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意过氧化钠能使紫色溶液褪色的性质.
关于Na2O与Na2O2的叙述正确的是()
A.都是白色固体 B.都是供氧物质
C.都能和水反应形成强碱溶液 D.都是强氧化剂
知识点:钠和碱金属
C
考点:钠的重要化合物.
专题:元素及其化合物.
分析:A、Na2O是白色的,Na2O2是黄色的固体;
B、Na2O2与水、二氧化碳反应生成氧气;Na2O不能与其他物质反应产生氧气;
C、Na2O与水反应生成氢氧化钠,Na2O2与水反应生成氢氧化钠和氧气;
D、强氧化剂是物质的组成元素化合价降低的性质,根据元素化合价来判断.
解答:解:A、Na2O是白色的,而Na2O2是黄色的固体,故A错误;
B、Na2O2与水、二氧化碳反应生成氧气,可作供氧物质,Na2O不能与其他物质反应产生氧气,不作供氧物质,故B错误;
C、Na2O与Na2O2与水反应都能生成氢氧化钠,氢氧化钠是强碱,故C正确;
D、Na2O中氧元素的化合价是﹣2价,Na2O2中氧元素的化合价是﹣1价,Na2O2具有氧化性,故D错误;
故选C.
点评:本题考查钠的氧化物的性质,明确发生的化学反应及相关的概念是解答本题的关键,难度不大.
下列物质中不与二氧化硅反应的是()
A.烧碱 B.氢氟酸 C.硝酸 D.生石灰
知识点:碳族元素
C
考点:硅和二氧化硅.
专题:碳族元素.
分析:二氧化硅为酸性氧化物,具有酸性氧化物的通性,但与水不反应,除与氢氟酸反应外,与其它酸不反应.
解答:解:A.二氧化硅与烧碱反应生成硅酸钠和水,反应方程式为SiO2+2NaOH=Na2SiO3+H2O,故A不选;
B.氢氟酸与二氧化硅反应生成四氟化硅和水,反应的方程式为SiO2+4HF=SiF4↑+2H2O,故B不选;
C.硝酸和二氧化硅不反应,故C选;
D.生石灰和二氧化硅在高温下反应生成硅酸钙,反应的方程式为SiO2+CaO CaSiO3,故D不选,
CaSiO3,故D不选,
故选C.
点评:本题考查二氧化硅的性质,题目难度不大,注意基础知识的积累.
下列离子方程式书写正确的是()
A.铝粉投入到NaOH溶液中:2Al+2OH﹣═2AlO2﹣+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++3OH﹣═Al(OH)3↓
C.三氯化铁溶液中加入铁粉Fe3++Fe=2Fe2+
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl﹣
知识点:离子方程式
D
考点:离子方程式的书写.
专题:离子反应专题.
分析:A、铝粉投入到NaOH溶液中产生氢气;
B、氨水是弱电解质,不能拆成离子形式;
C、离子反应遵循电荷守恒;
D、氯气能加亚铁离子氧化到最高价.
解答:解:A、铝粉投入到NaOH溶液中产生氢气,反应实质为:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑;
B、氨水是弱电解质,不能拆成离子形式,应改为:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故B错误;
C、三氯化铁溶液中加入铁粉的反应为:2Fe3++Fe=3Fe2+,故C错误;
D、氯气能加亚铁离子氧化到最高价,即2Fe2++Cl2=2Fe3++2Cl﹣,故D正确.
故选D.
点评:本题考查学生离子方程式书写的正误判断,该题型是现在高考的热点,难度不大.
向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液.下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)()
A. B.
B. C.
C. D.
D.
知识点:镁铝及其化合物
D
考点:镁、铝的重要化合物.
专题:图示题;几种重要的金属及其化合物.
分析:根据Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓、Al(OH)3+OH﹣═AlO2﹣+2H2O来分析.
解答:解:因横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量,
则向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液,
发生Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓,则沉淀的质量一直在增大,直到最大,
然后发生Al(OH)3+OH﹣═AlO2﹣+2H2O,沉淀的质量减少,但氢氧化镁不与碱反应,则最后沉淀的质量为一定值,
显然只有D符合,
故选D.
点评:本题考查化学反应与图象的关系,明确图象中坐标及点、线、面的意义,明确发生的化学反应是解答本题的关键,注意氢氧化铝能溶于碱,而氢氧化镁不能来解答.
实验室中,要使AlCl3溶液中的Al3+离子全部沉淀出来,适宜用的试剂是()
A.NaOH溶液 B.Ba(OH)2溶液 C.盐酸 D.氨水
知识点:镁铝及其化合物
D
考点:镁、铝的重要化合物.
专题:几种重要的金属及其化合物.
分析:根据题意,Al3+转化为不溶于水的物质是Al(OH)3,Al(OH)3具有两性,既能和强酸反应又能和强碱反应,要使Al2(SO4)3溶液中的Al3+完全沉淀,选取试剂时就不能选强碱,只能是弱碱.
解答:解:Al3+转化为不溶于水的物质是Al(OH)3,Al(OH)3具有两性,既能和强酸反应又能和强碱反应,要使Al2(SO4)3溶液中的Al3+完全沉淀,选取试剂时就不能选强碱,只能是弱碱.
A、NaOH溶液是强碱,能溶解氢氧化铝沉淀,故A错误;
B、Ba(OH)2 溶液是强碱,能溶解氢氧化铝沉淀,故B错误;
C、盐酸是酸,与Al3+不反应,故C错误;
D、氨水是弱碱,加入过量的氨水能把铝离子完全沉淀,故D正确;
故选D.
点评:本题考查铝的重要化合物的性质,难度不大,注意题目要求意在考查氢氧化铝的两性这一特性.
下列叙述正确的是()
A.1mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1mol任何物质体积均为22.4L
知识点:物质的量的计算
C
考点:物质的量的相关计算.
专题:计算题.
分析:A.1mol水的质量为18g;
B.甲烷的摩尔质量为16g/mol;
C.根据n=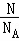 计算二氧化硫的物质的量,再根据m=nM计算二氧化硫的质量;
计算二氧化硫的物质的量,再根据m=nM计算二氧化硫的质量;
D.气体摩尔体积使用对象是气体.
解答:解:A.水的摩尔质量是18g/mol,1mol水的质量为18g,故A错误;
B.甲烷的摩尔质量为16g/mol,1mol甲烷的质量是16g,故B错误;
C.3.01×1023个SO2分子的物质的量=0.5mol,二氧化硫的质量=0.5mol×64g/mol=32g,故C正确;
D.气体摩尔体积使用对象是气体,标准状况下任何物质,不一定都是气体,故D错误;
故选C.
点评:本题考查常用化学计量的有关计算,比较基础,注意对公式的理解与灵活运用,注意气体摩尔体积的使用条件与对象.
下列反应中,不是氧化还原反应的是()
①H2+Cl2 2HCl ②Na2CO3+2HCl═2NaCl+H2O+CO2↑ ③2H2O
2HCl ②Na2CO3+2HCl═2NaCl+H2O+CO2↑ ③2H2O 2H2↑+O2↑④CuO+2HNO3═Cu(NO3)2+H2O ⑤2HgO
2H2↑+O2↑④CuO+2HNO3═Cu(NO3)2+H2O ⑤2HgO 2Hg+O2↑
2Hg+O2↑
A.②④ B.①③ C.①②③ D.④⑤
知识点:氧化还原反应
A
考点:氧化还原反应.
专题:氧化还原反应专题.
分析:判断元素的化合价是否发生变化,凡是有化合价升降的反应一定为氧化还原反应.
解答:解:①H和Cl的化合价发生变化,属于氧化还原反应,故①不选;
②各元素的化合价都没有变化,不是氧化还原反应,故②选;
③H和Cl的化合价发生变化,属于氧化还原反应,故③不选;
④各元素的化合价都没有变化,不是氧化还原反应,故④选;
⑤Hg和O的化合价发生变化,属于氧化还原反应,故⑤不选.
故选A.
点评:本题考查氧化还原反应,题目难度不大,氧化还原反应的特征是化合价发生变化,注意化合价的判断.
(双选)Al粉投入某无色澄清的溶液中产生H2,则下列离子组合正确的是()
A.H+、Ca2+、Na+、CO32﹣ B.Na+、Mg2+、Al3+、Cl﹣
C.Cu2+、Mg2+、Cl﹣、OH﹣ D.Ba2+、Cl﹣、OH﹣、NO3﹣
知识点:离子共存
BD
考点:离子共存问题.
分析:Al粉投入某无色澄清的溶液中产生H2,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,并结合离子的颜色来解答.
解答:解:Al粉投入某无色澄清的溶液中产生H2,为非氧化性酸或强碱溶液,
A.Ca2+、CO32﹣结合生成沉淀,H+、CO32﹣结合生成水和气体,不能大量共存,故A不选;
B.碱性溶液中不能大量存在Mg2+、Al3+,酸性溶液中该组离子之间不反应,可大量共存,且离子均为无色,故B选;
C.Cu2+、Mg2+分别与OH﹣结合生成沉淀,且Cu2+为蓝色,与无色不符,故C不选;
D.碱性溶液中该组离子之间不反应,可大量共存,且离子均为无色,故D选;
故选BD.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意常见离子的颜色,题目难度不大.
只用一种试剂通过一步实验来鉴别氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,这种试剂是()
A.盐酸 B.烧碱 C.硫酸钠溶液 D.KSCN溶液
知识点:物质的检验和鉴别
B
考点:物质的检验和鉴别的实验方案设计.
分析:加入NaOH后,与AlCl3溶液先生成白色沉淀后消失、与FeCl2溶液生成白色沉淀最后变为红褐色、与FeCl3溶液生成红褐色沉淀、与MgCl2溶液生成白色沉淀,现象各不相同,与NaCl不反应,以此来解答.
解答:解:A.均与盐酸不反应,不能鉴别,故A不选;
B.加入NaOH后,与AlCl3溶液先生成白色沉淀后消失、与FeCl2溶液生成白色沉淀最后变为红褐色、与FeCl3溶液生成红褐色沉淀、与MgCl2溶液生成白色沉淀,现象各不相同,与NaCl不反应,现象不同,可鉴别,故B选;
C.均与硫酸钠不反应,不能鉴别,故C不选;
D.KSCN溶液只能鉴别氯化铁,故D不选;
故选B.
点评:本题考查物质的鉴别,为高频考点,注意根据几种物质的不同性质,用实验的方法逐一区别.注意鉴别的界定条件,如只用一种试剂就能加以区别等,题目难度不大.
下列变化过程属于还原反应的是()
A.H+→H2O B.Na→Na+ C.CO→CO2 D.Fe3+→Fe2+
知识点:氧化还原反应
D
考点:氧化还原反应.
分析:氧化还原反应中,氧化剂发生还原反应,氧化剂中某元素的化合价降低,以此来解答.
解答:解:A.H元素化合价没有发生变化,属于复分解反应,故A错误;
B.Na元素化合价升高,被氧化,属于氧化反应,故B错误;
C.C元素化合价升高,被氧化,属于氧化反应,故C错误;
D.Fe元素化合价降低,被还原,属于还原反应,故D正确.
故选D.
点评:本题考查氧化还原反应,为高考高频考点,把握反应中元素的化合价变化为解答的关键,侧重基本概念的考查,注意把握氧化剂发生还原反应,题目难度不大.
在溶有0.5molNa2SO4的水溶液中,含有的Na+离子数是()个.
A.3.01×1023 B.6.02×1023 C.0.5 D.1
知识点:物质的量的计算
B
考点:物质的量的相关计算.
分析:根据化学式为Na2SO4,利用硫酸钠的物质的量来确定钠离子的物质的量,再利用N=n×NA来计算钠离子的数目
解答:解:0.5molNa2SO4中钠离子的物质的量为0.5mol×2=1mol,
则由N=n×NA可知,
则钠离子的个数为1mol×NAmol﹣1=NA≈6.02×1023,
故选B.
点评:有关阿伏伽德罗常数的计算,题目在注重对计算关系的考查的同时,又隐含对物质状态、物质结构、氧化还原反应、电离、水解知识的考查.
在化学反应2H2O2═2H2O+O2中,H2O2中的氧元素()
A.只是被氧化 B.只是被还原
C.既被氧化又被还原 D.以上都不是
知识点:氧化还原反应
C
考点:氧化还原反应.
分析:该反应双氧水中O元素化合价由﹣1价变为0价和﹣2价,得电子化合价降低的元素被还原,失电子化合价升高的元素被氧化,据此分析解答.
解答:解:该反应双氧水中O元素化合价由﹣1价变为0价和﹣2价,得电子化合价降低的元素被还原,失电子化合价升高的元素被氧化,所以双氧水中的氧元素既被氧化又被还原,故选C.
点评:本题考查氧化还原反应,侧重考查基本概念,明确元素化合价变化是解本题关键,注意双氧水、过氧化钠中氧元素化合价,为易错点.
苹果汁是人们喜爱饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色,若榨汁时加入维生素C,可有效防止这种现象发生.这说明维生素C具有()
A.氧化性 B.还原性 C.碱性 D.酸性
知识点:铁及其化合物
B
考点:铁盐和亚铁盐的相互转变.
专题:几种重要的金属及其化合物.
分析:根据苹果汁在空气中会由淡绿色变为棕黄色,可知铁元素的化合价升高被氧化,而加入维生素C,能使铁元素的化合价降低,并利用氧化还原反应来分析.
解答:解:在空气中,氧气能够把+2价铁氧化成+3价;而加入维生素C则能防止这种氧化,说明维生素C具有还原性,与三价铁发生氧化还原反应,
故选B.
点评:本题考查氧化还原反应,明确铁元素的化合价变化是解答的关键,学生应理解氧化反应概念来解答.
北京奥运会开幕式上的焰火“脚印”、“笑脸”、“五环”让奥运会更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关.下列说法中正确的是()
A.焰色反应均应透过蓝色钴玻璃观察
B.NaC1与Na2CO3灼烧时火焰颜色相同
C.做焰色反应实验时,用稀硫酸洗涤铂丝
D.所有金属及其化合物灼烧时火焰均有颜色
知识点:钠和碱金属
B
考点:焰色反应.
分析:A.只有钾的焰色反应应透过蓝色钴玻璃观察;
B.无论是单质还是化合物,只要含有的金属元素相同,灼烧时火焰颜色就相同;
C.做焰色反应实验时,用稀盐酸洗涤铂丝;
D.有些金属及其化合物灼烧时火焰没有颜色.
解答:解:A.只有钾的焰色反应的观察需要透过蓝色钴玻璃滤去黄光,避免钠的焰色对钾的焰色的干扰,故A错误;
B.因焰色反应是元素的性质,只要含有的金属元素相同,无论是单质还是化合物灼烧时火焰颜色都相同,NaC1与Na2CO3灼烧时,火焰颜色为钠的颜色,都为黄色,故B正确;
C.做焰色反应实验时,用稀盐酸洗涤铂丝,稀盐酸加热易挥发,稀硫酸不能挥发,故C错误;
D.并不是所有的金属及其化合物灼烧时火焰都有颜色,如铁灼烧时火焰没有颜色,故D错误;
故选B.
点评:本题主要考查了焰色反应,焰色反应是某些金属或它们的化合物在无色火焰中灼烧时使火焰呈现特征的颜色的反应,平时须熟记常见的元素的焰色.