已知热化学方程式:2H2(g)+O2(g)===2H2O(g);ΔH1=-483.6kJ·mol-1。则对于热化学方 程式:2H2O(g)===2H2(g)+O2(g);ΔH2=bkJ·mol-1的说法正确的是( )
A.热化学方程式中H2O前面的“2”表示“每2个液态水分子分解,就有bkJ·mol-1的热量变化”
B.b=+483.6 C.|ΔH2|>|ΔH1| D.|ΔH2|<|ΔH1|
知识点:化学反应与能量的变化
B
略
下列事实不能用原电池原理解释的是 ( )
A.海轮的水线以下的船壳上装一定数量的锌块
B.铝片不用特殊方法保护
C.纯锌与稀硫酸反应时,滴入少量氯化铜溶液后产生气泡的速率加快
D.镀锌铁比镀锡铁耐用
知识点:原电池
B
略
关于铅蓄电池Pb+PbO2+2H2SO4 ![]() PbSO4+2H2O的说法正确的是
PbSO4+2H2O的说法正确的是
A.在充电时,电池中硫酸的浓度不断变小
B.在充电时,阳极发生的反应是 PbSO4(s)+2e—= Pb(s)+ SO42—(aq)
C.在放电时,正极发生的反应是 Pb(s) +SO42—(aq)= PbSO4(s) +2e—
D.在放电时,该电池的负极材料是铅板
知识点:原电池
D
略
钢铁发生吸氧腐蚀时,正极上发生的电极反应是( )
A. 2H++2e-=H2 B. Fe2++2e-=Fe
C. 2H2O+O2+4e-=4OH- D. Fe3++e-=Fe2+
知识点:金属的电化学腐蚀与防护
C
略
在原电池和电解池的电极上所发生的反应,属于氧化反应的是
A.原电池的正极和电解池的阳极所发生的反应
B.原电池的正极和电解池的阴极所发生的反应
C.原电池的负极和电解池的阳极所发生的反应
D.原电池的负极和电解池的阴极所发生的反应
知识点:电化学基础
C
略
在298K、100kPa时,已知:①2![]() ⊿
⊿![]()
②![]() ⊿
⊿![]()
③![]() ⊿
⊿![]()
则⊿![]() 与⊿
与⊿![]() 和⊿
和⊿![]() 间的关系正确的是
间的关系正确的是
A .⊿![]() =⊿
=⊿![]() +2⊿
+2⊿![]() B ⊿
B ⊿![]() =⊿
=⊿![]() +⊿
+⊿![]()
C. ⊿![]() =⊿
=⊿![]() -2⊿
-2⊿![]() D. ⊿
D. ⊿![]() =⊿
=⊿![]() - ⊿
- ⊿![]()
知识点:化学反应的热效应
A
略
在外界提供相同电量的条件,Cu2+或Ag+分别按Cu2++2e→Cu或Ag++e-→Ag在电极上放电,若析出铜的质量为1.92g,则析出银的质量为
A.1.62g B.6.48g C.3.24g D.12.96g
知识点:物质的量的计算
B
略
在一定温度下,在一容积不变的密闭容器中发生可逆反应A(g)+3B(g) ![]() 2C(g),其达到平衡状态的标志是
2C(g),其达到平衡状态的标志是
A. C生成的速率与C分解的速率相等
B. 单位时间生成n mol A,同时生成3n mol B
C. 体系的压强不再变化
D. A、B、C的浓度之比为1∶3∶2
知识点:化学平衡状态及移动
AC
略
灰锡(常温下以粉末状存在)和白锡是锡的两种同素异形体。
已知:①Sn(s,白)+2HCl(aq)== SnCl2(aq)+H2(g) ΔH1
②Sn(s,灰)+2HCl(aq)== SnCl2(aq)+H2(g) ΔH2
③Sn(s,灰)![]() Sn(s,白) ΔH3 =
+2.1 kJ·mol-1
Sn(s,白) ΔH3 =
+2.1 kJ·mol-1
下列说法正确的是( )
A.ΔH1>ΔH2
B.锡在常温下以白锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏
知识点:化学反应与能量的变化
BD
略
下列叙述错误的是
A.生铁中含有碳,抗腐蚀能力比纯铁弱
B.用锡焊接的铁质器件,焊接处易生锈
C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液
D.铁管上镶嵌锌块,铁管不易被腐蚀
知识点:金属的电化学腐蚀与防护
C
略
用石墨电极电解下列溶液一段时间后再加入一定量的某种纯净物(方括号内物质),能使 溶液恢复到原来的成分和浓度的是( )
A.AgNO3[AgNO3] B.NaOH[H2O] C.KCl[KCl] D.CuSO4[CuO]
知识点:电解池
BD
略
对于化学反应方向的确定,下列说法正确的是
A. 在温度、压力一定的条件下,焓因素和熵因素共同决定一个化学反应的方向
B. 温度、压力一定时,放热的熵增加反应一定能自发进行
C. 反应焓变是决定反应能否自发进行的唯一因素
D. 固体的溶解过程与焓变有关
知识点:化学反应进行的方向
AB
略
在一密闭容器中进行反应2SO2
+ O2 ![]() 2SO3,已知反应过程中某一时刻SO2、 O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
2SO3,已知反应过程中某一时刻SO2、 O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
A.SO2为 0.4mol/L,O2为0.2mol/L B. SO2为0.25mol/L
C.SO2、SO3均为0.15mol/L D.SO3为0.4mol/L
知识点:化学平衡状态及移动
B
略
写出下列反应的热化学方程式
(1)46gC2H5OH(l)与适量O2(g)反应,生成CO2(g)和H2O(l),放出1366.8kJ热量。
。
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:
知识点:反应热的计算
(1) C2H5OH(l) + 3 O2(g) = 2 CO2(g) + 3 H2O(l) △H=-1366.8 kJ·mol-1
(2) 1/2 H2(g)+ O2(g)= H2O(g) △H=-241.8 kJ·mol-1
略
已知H2(g)+Cl2(g)=2HCl(g) △H= ―184.6kJ·mol-1, 则反应HCl(g)=1/2H2(g)+1/2Cl2(g)的△H为
知识点:反应热的计算
+92.3kJ·mol-1
略
如图所示,水槽中试管内有一枚铁钉,放置数天观察:
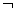
(1)铁钉在逐渐生绣。
(2)若试管内液面上升,发生 腐蚀,电极反应:
负极: ,正极:
(3)若试管内液面下降,则原溶液呈 性,发生的电极反应:
正极: 。
知识点:金属的电化学腐蚀与防护
(2) 吸氧 负极: Fe —2e- = Fe2+ ,
正极: 2H2O+O2+4e-=4OH-
(3) 酸 正极: 4H++4e-=2H2 ↑ 。
略
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解
液a;X、Y是两块电极板,通过导线与直流电源相连。
请回答以下问题:

⑴若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,
同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是 。
在X极附近观察到的现象是 。
②Y电极上的电极反应式是 ,
⑵如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式是
②Y电极的材料是 ,电极反应式是
(说明:杂质发生的电极反应不必写出)
知识点:电解池
①电解池中X极上的电极反应式是 2H++2e-=H2 ↑ 。
在X极附近观察到的现象是 无色溶液变红
②Y电极上的电极反应式是 2Cl- —2e- = Cl2 ↑
⑵如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 粗铜 ,电极反应式是 Cu (粗铜) —2e- =Cu2+
②Y电极的材料是 精 铜 ,电极反应式是 Cu2+ +2e- = Cu ( 精 铜 )
(说明:杂质发生的电极反应不必写出)
略
已知A(g)+B(g) ![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/ ℃
700
800
830
1000
1200
平衡常数K
1.7
1.1
1.0
0.6
0.4
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“>”“=”);
(2)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和A的物质的从相等
(3) 1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为
。
A(g)+B(g)的平衡常数的值为
。
(4)某温度下平衡浓度符合下式
c(A)·c(B)==c(C)·c(D) 试判断此时的温度为 ℃
知识点:化学平衡状态及移动
(1)K= c(C)·c(D)/ c(A)·c(B) ,△H < 0
(2) C (3) 2.5 (4) 830
略