下列仪器中常用于物质分离的是( )
①漏斗;②量筒;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥研钵;⑦蒸发皿
A.①③④ B.①②⑥ C.①③⑤⑦ D.①③⑥
知识点:仪器和基本操作
C
略
在某无色透明的酸性溶液中,能共存的离子组是 ( )
A.Na+ 、K+、SO42-、HCO3- B.Cu2+、K+、SO42-、NO3-
C.Na+、 K+、Cl-、 NO3- D.Fe3+、K+、SO42-、Cl-
知识点:离子共存
C
略
下列说法中正确的是( )
A.1mol氮约含有6.02×1023个粒子
B.1mol H2O中含有1molO原子和2molH原子
C.钠的摩尔质量等于它的相对原子质量
D.硫酸的摩尔质量等于98g
知识点:化学中常用计量
B
略
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法。下列关于“Na2CO3”的分类不正确的是 ( )
A.电解质 B.碳酸盐 C.钠盐 D.碱
知识点:物质的分类
D
略
下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是( )
A. 2Na + 2H2O ==2NaOH + H2↑ B. CH4 + 2O2==CO2 + 2H2O
C.2 KClO3==2KCl + 3O2↑ D. CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
知识点:氧化还原反应
B
略
右边示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量可忽略不计)。其中能表示等质量的氢气与氦气的是( )
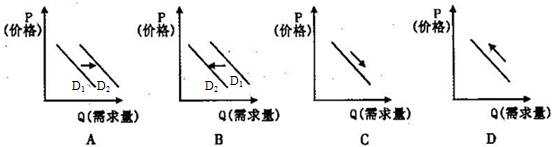
知识点:阿弗加德罗定律
A
略
下列实验操作中有错误的是( )
A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B.实验室制取蒸馏水的装置中,温度计水银球应与蒸馏烧瓶的支管口在同一水平线
C.用淘洗的方法从沙里淘金
D.用蒸发方法使NaCl从溶液中析出时,应边加热边搅拌直至溶液蒸干
知识点:仪器和基本操作
D
略
下列离子方程式中正确的是( )
A.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
B.向氢氧化钡溶液中加硫酸溶液:SO42-+Ba2+= BaSO4↓
C.向稀硫酸溶液中加铁:2Fe + 6 H+ =2Fe3+ +3H2↑
D.向硝酸银溶液中加盐酸:Ag+ + Cl- = AgCl↓
知识点:离子方程式
D
略
设NA表示阿伏加德罗常数,下列说法不正确的是( )
A.1 mol醋酸的质量与NA个醋酸分子的质量相等
B.NA个氧气分子和NA个氢气分子的质量比等于16∶1
C.30 g乙烷(C2H6)所含的原子数目为NA
D.在标准状况下, 0.5NA个氯气分子所占体积约是11.2 L
知识点:物质的量的计算
C
略
下列叙述正确的是( )
A.氯化钠溶液在电流作用下电离成钠离子和氯离子
B.溶于水后电离出氢离子的化合物都是酸
C.硫酸钡难溶于水,但硫酸钡是电解质
D.二氧化碳的水溶液能导电,故二氧化碳属于电解质
知识点:物质的分类
C
略
能用H++OH-=H2O来表示的化学反应是( )
A.氢氧化镁和稀盐酸反应 B.Ba(OH)2溶液滴入稀硫酸中
C.澄清石灰水和稀硝酸反应 D.二氧化碳通入澄清石灰水中
知识点:离子方程式
C
略
下列电离方程式,书写正确的是( )
A. Al2(SO4)3 =2Al3+ + 3SO42- B.AlCl3 = Al3+ +Cl3-
C. Mg(NO3)2 = Mg+2 +2NO3- D.KMnO4 =K+ +Mn7+ +4O2-
知识点:化学用语
A
略
胶体区别于其他分散系的本质特征是 ( )
A. 光束穿过胶体时形成一条光亮的“通路” B. 胶体粒子大小在l nm ~ l00 nm 之间
C. 胶体粒子可以透过滤纸 D. 胶体粒子不能透过半透膜
知识点:分散系
B
略
下列反应中属于氧化还原反应,但水既不作氧化剂又不作还原剂的是 ( )
A. 2H2O![]() 2H2↑+O2↑ B. Cl2+H2O=HCl+HClO
2H2↑+O2↑ B. Cl2+H2O=HCl+HClO
C. 2F2+2H2O=4HF+O2 D. 2Na+2H2O=2NaOH+H2↑
知识点:氧化还原反应
B
略
配制100 ml 2.0 mol/L NaCl溶液时,下列情况中会导致最终浓度偏大的是( )
A. 容量瓶使用前未干燥
B.转移溶液后,烧杯没有洗涤
C. 在称量NaCl固体时,天平指针偏左
D. 定容时,不小心加水超过了刻度线后,用胶头滴管吸出部分溶液至刻度线
知识点:仪器和基本操作
C
略
下列溶液中,溶质的物质的量浓度为1mol/L的是( )
A.含Na+为2mol的Na2SO4溶液
B.将80g SO3溶于水(SO3+H2O=H2SO4)并配成1L的溶液
C.将0.5mol/L的某饱和溶液100mL,加热蒸发掉50g水后的溶液
D.将58.5gNaCl溶于1L水所得的溶液
知识点:溶液浓度的计算
B
略
为了除去粗盐中Ca2+、Mg2+、SO42-,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是:( )
①过滤 ②加过量的NaOH溶液 ③加适量盐酸
④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
A.①④②⑤③ B.④①②⑤③ C.②④⑤①③ D.⑤②④①③
知识点:物质的分离、除杂和提纯
D
略
选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.结晶法 C.分液法 D.蒸馏法 E.过滤法
⑴分离饱和食盐水和沙子的混合物: ;
⑵从硝酸钾和氯化钠的混合溶液中获得硝酸钾: ;
⑶分离水和油的混合物: ;
⑷分离CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合物: ;
⑸从碘的水溶液中提取碘: 。
知识点:物质的分离、除杂和提纯
(1)E (2)B (3)C (4)D (5)A
略
⑴通常状况下,甲同学取1 mol H2O加热到 100℃时,液态水会汽化为水蒸气(如图所示),
该过程属于 变化。(填“物理”或“化学”)在保持压强不变的情况下,水蒸气的体积 22.4L 。 (填“>”、“<”或“=”)
(2)乙同学做H2在O2中燃烧的实验,该实验过程属于 变化,(填“物理”或“化学”)
在该变化过程中,一定保持相等的是 (填序号)。
A、反应物分子数目与生成物分子数目 B、反应物原子总物质的量与生成物原子总物质的量
C、反应物总质量与生成物总质量 D、反应物体积与生成物体积
知识点:物质的量
物理 > 化学 BC
略
现有A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子则可能是NO3-, SO42-, Cl-,CO32-离子中的某一种(不重复)。
(1)若把四种盐溶解在四支试管中,只有C盐溶液呈蓝色。
(2)若向(1)的四支试管中分别加入盐酸,B盐溶液中有沉淀生成,D盐溶液中有无色无味气体放出。
根据以上实验事实推断它们的化学式为:A B C D
写出B盐与盐酸反应的离子方程式
知识点:离子反应
A BaCl2 B AgNO3 C CuSO4 D Na2CO3 Ag + + Cl- =AgCl↓
略
已知铜在常温下能被稀HNO3溶解,反应为:3Cu+8HNO3
3Cu(NO3)2+2NO↑+4H2O。
(1)请将上述反应改写成离子方程式_______。
(2)上述反应中,氧化剂是________(填化学式),氧化产物是_________(填化学式)。
(3)用双线桥法或单线桥法标出该反应的电子转移方向和数目。
(4)氧化剂与氧化产物的物质的量之比是________________
(5)此反应若生成NO 67.2L(标准状况),则转移了_______ mol 电子
知识点:氧化还原反应
(1) 3Cu+8H+十2NO3--═3Cu2++2NO↑十4H2O;
(2)HNO3 NO
(3)![]()
(4)2:3
(5)9
略