(12分)过氧化氢和臭氧都是常见的绿色氧化剂,在工业生产中有着重要的用途。
(1)据报道以硼氢化合物NaBH4(B的化合价为+3价)和H2O2作原料的燃料电池,可用作通信卫星电源。负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图7所示。该电池放电时正极的电极反应式为: ▲ ;
以MnO2做正极材料,可能是因为 ▲ 。
(2)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知: N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H = – 534 kJ·mol—1
H2O2(l) = H2O(l) + 1/2O2(g) △H = – 98.64 kJ·mol—1
H2O(l) = H2O(g) △H= + 44kJ·mol—1
反应N2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) 的 △H= ▲ 。
(3)O3 可由臭氧发生器(原理如图8所示)电解稀硫酸制得。
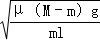
①图中阴极为 ▲ (填“A”或“B”)。
②若C处通入O 2,则A极的电极反应式为: ▲ 。
③若C处不通入O 2 ,D、E处分别收集到11.2L和有4.48L气体(标准状况下),则E处收集的气体中O3所占的体积分数为 ▲ (忽略 O 3 的分解)。
(4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx
95%以上是以NO形式存在的,可发生反应NO(g)+ O3 (g) ![]() NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是 ▲
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是 ▲
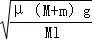
a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.反应物的总能量低于生成物的总能量
d.Δt1=Δt2时,NO的转化率:a~b段小于b~c段
知识点:基本概念、基本理论的综合运用
(14分)
(1)H2O2 + 2e—= 2OH—; 除了作电极材料,MnO2还对电极反应具有催化作用 (各2分)
(2)-643.28kJ·mol—1 (2分)
(3) ① A ② O2+4H++4e-=2H2O ③50% (各2分)
(4)d (2分)
略