下列实验操作中错误的是( )
A.在由氢氧化铜分解制氧化铜时,要边加热边用玻璃棒搅拌
B.用药匙或者纸槽把粉末状药品送入试管的底部
C.如果没有试管夹,可以临时手持试管给固体或液体加热手
D.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
知识点:仪器和基本操作
C
略
对于相同物质的量的SO2和SO3,下列说法中正确的是( )
A.氧元素的质量比为1∶1 B.分子数之比为1∶1
C.原子总数之比为1∶1 D.质量之比为1∶1
知识点:化学计算的综合运用
B
略
现有一瓶物质甲和乙的混合物,已知甲和乙的某些性质如下表。
物质
分子式
熔点/ ℃
沸点/ ℃
密度/ g·cm-3
水中溶解性
甲
C3H6O2
-98
57.5
0.93
可溶
乙
C4H8O2
-84
97.8
0.90
可溶
据此判断,将甲和乙相互分离的最佳方法是( )
A.蒸馏法 B.升华法
C.萃取法 D.分液法
知识点:物质的分离、除杂和提纯
A
略
根据中央电视台报道,近年来,我国的一些沿江或沿海城市多次出现大雾天气致使高速公路关闭,航班停飞,雾属于下列分散系中的( )
A.溶液 B.悬浊液 C.乳浊液 D.胶体
知识点:分散系
D
略
用NA表示阿伏德罗常数,下列叙述正确的是( )
A.标准状况下,22.4 L酒精中含有的分子数为 NA
B.常温常压下,10.6 g Na2CO3固体中含有Na+ 个数为0. 2 NA
C.25℃,1.01×105 Pa下,NA 个CO2分子占有的体积为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
知识点:物质的量
B
略
磁悬浮的核心技术是利用超导体的反磁性。以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导物质YBa2Cu3Ox 。现欲合成 0.5mol 此高温超导物质,理论上需取Y2O3、BaCO3和CuO的物质的量(单位:mol)分别为( )
A.0.50、0.50、0.50 B.0.50、1.0、1.5
C.0.25、1.0、1.5 D.1.0、0.25、0.17
知识点:物质的量的计算
C
略
等质量的①CH4、②H2、③HCl、④SO2,在标准状况下所占体积由大到小排列的顺序是( )
A.②>①>③>④ B.④>③>①>②
C.③>②>④>① D.①>④>②>③
知识点:气体体积的计算
A
略
完全沉淀等物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗等物质的量浓度的AgNO3溶液的体积比为3∶2∶1,则上述溶液的体积比为( )
A.1 :1 :1 B.3 :2 :1
C.6 :3 :2 D.9 :3 :1
知识点:化学计算的综合运用
D
略
实验室用饱和的FeCl3溶液制取Fe(OH)3胶体,下列操作正确的是( )
A.将饱和FeCl3溶液滴入蒸馏水中
B.将饱和FeCl3溶液滴入氢氧化钠溶液中,并不断搅拌
C.将饱和FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色液体
D.将饱和FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色沉淀
知识点:分散系
C
略
下列各组中的离子,能在溶液中大量共存的是( )
A.H+、 K+、 CO32-、SO42- B.Ba2+、Na+、CO32-、OH-
C.Mg2+、Ba2+、OH-、NO3- D.K+、Mg2+、NO3-、Cl-
知识点:离子共存
D
略
下列离子方程式书写正确的是( )
A.将固体CuO加入稀H2SO4中:CuO + 2H+ = Cu2+ + H2O
B.氢氧化钡与硫酸反应:Ba2+ + H+ + SO42- + OH- = BaSO4↓ + H2O
C.把金属铁放入稀硫酸中制取氢气:2Fe + 6H+ = 2Fe3+ + 3H2↑
D.石灰石与盐酸反应制取二氧化碳:CO32- + 2H+ = CO2↑ + H2O
知识点:离子方程式
A
略
下列化学方程式中,不能用离子方程式 Ba2+ + SO42-= BaSO4↓ 表示的是( )
A.Ba(NO3)2 + H2SO4= BaSO4↓ + 2HNO3
B.BaCl2 + Na2SO4= BaSO4↓+ 2NaCl
C.BaCO3 + H2SO4= BaSO4↓+ H2O + CO2↑
D.BaCl2+ H2SO4= BaSO4↓+2HCl
知识点:离子方程式
C
略
物质X(![]() )和物质Y(
)和物质Y(![]() )的反应中,微粒之间的关系如下图所示,对该反应的描述,下列反应方程式正确的是( )
)的反应中,微粒之间的关系如下图所示,对该反应的描述,下列反应方程式正确的是( )
A.3X + 8Y ![]() X3Y8
X3Y8
B.X + 2Y ![]() XY2
XY2
C.3X + 6Y ![]() X3Y6
X3Y6
D.3X + 8Y ![]() 3XY2 + 2Y
3XY2 + 2Y
知识点:基本概念、基本理论的综合运用
B
略
在19世纪,化学家对氧化锆的化学式有争议。经测定,锆(Zr)的相对原子质量为91,其氯化物的相对分子质量是233。若氧化锆中锆的化合价与氯化物中的相同,试判断氧化锆的化学式为( )
A.Zr2O B.ZrO2 C.Zr2O3 D.ZrO
知识点:元素及其化合物的综合运用
B
略
(4分)选择下列实验方法分离物质,将分离方法的序号填在横线上。(4分)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏
(1)分离饱和食盐水与沙子的混合物 ;
(2)从碘的水溶液里提取碘 ;
(3)分离水和汽油的混合物 ;
(4)分离CCl4(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物 。
知识点:物质的分离、除杂和提纯
![]()
略
(6分)将以下几种物质中,按要求将正确答案填写在相应的空格内
①干燥的食盐晶体; ②液态氯化氢; ③水银; ④蔗糖;
⑤CO2; ⑥KNO3溶液; ⑦氯气
以上物质中能导电的是 ;属于电解质的是 ;属于非电解质的是 ;(填正确答案的序号)
知识点:物质的分类
![]()
略
(6分)按要求计算并填空
(1)49 g H2SO4中含有 mol 氢原子,所含氧原子的个数为 , 与 克SO2中所含S原子数相等;
(2)0.2 mol 的 O2 和 0.3 mol 的 O3 的质量比是 ,它们所含原子个数比为 ,同温同压下二者的体积比是 ;
知识点:化学计算的综合运用
![]()
略
按要求写出方程式(8分)
(1)氯化钠溶液中滴加硝酸银溶液(离子方程式)
(2)澄清石灰水中通入少量二氧化碳气体(离子方程式)
(3)Cu2+ + 2OHˉ = Cu(OH)2↓(对应的一个化学方程式)
(4)CO32- +2H+ = CO2↑+ H2O(对应的一个化学方程式)
知识点:离子方程式
(1)Ag+ + Cl- = AgCl↓
(2)CO2 + Ca2+ + 2OH- = CaCO3↓ + H2O
(3)CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4
(4)Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
略
(9分)从海水得到的粗盐含有少量的CaCl2、MgSO4等杂质,某同学用粗盐进行提纯,获取纯净的食盐,实验步骤如下图所示。请回答:
(1)步骤①和②的操作名称是 。
(2)步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止 ,当蒸发皿中有较多量固体出现时,应 。
(3)根据相关知识,完成相关猜想和验证,将下表中空白部分补充完整
猜想
验证的方法
现象
结论
猜想Ⅰ:固体A中含CaCO3、MgCO3等物质
取少量固体A于试管中,滴加稀盐酸,并用蘸有澄清石灰水的小烧杯罩于试管口
猜想Ⅰ成立
猜想Ⅱ:最后制得的NaCl固体中仍含有少量Na2SO4
取少量NaCl晶体溶于试管中加入少量蒸馏水溶解,
猜想Ⅱ成立
知识点:物质的分离、除杂和提纯
(1)过滤 (2)溶液受热不均,造成液体飞溅; 移去酒精灯,用余热将溶液蒸干
(3)答案见下表
|
猜想 |
验证的方法 |
现象 |
结论 |
|
猜想Ⅰ:固体A中含CaCO3、MgCO3等物质 |
取少量固体A于试管中,滴加稀盐酸,并用蘸有澄清石灰水的小烧杯罩于试管口 |
澄清石灰水变浑浊 |
猜想Ⅰ成立 |
|
猜想Ⅱ:最后制得的NaCl固体中仍含有少量Na2SO4 |
取少量NaCl晶体溶于试管中加入少量蒸馏水溶解,加入盐酸,然后向溶液中滴加BaCl2溶液 |
产生白色沉淀 |
猜想Ⅱ成立 |
略
(13分)实验室欲配制0.5 mol/L的NaOH溶液500 mL:
(1)需称取NaOH固体的质量为 g
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如下图所示.由图可见,该同学在操作时的一个明显错误是________________________________________,烧杯的实际质量为 。

(3)在下图所示仪器中,配制上述溶液肯定不需要的是_____________(填序号)。
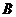
A B C D
(4)在容量瓶的使用方法中,下列操作正确的是____________(可多选)
A.使用容量瓶前应首先检验是否漏水。
B.容量瓶用水洗净后,再用待配溶液润洗2~3次。
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.如果配制溶液时,溶质溶解速率比较慢,可以将容量瓶在酒精灯上加热,促进溶质的溶解,节省配制溶液的时间。
E.洗烧杯和玻璃棒的洗涤液必须转移入容量瓶中,不能倒掉。
(5)下图是该同学转移溶液的示意图,该同学在操作过程中存在明显的错误为:
。
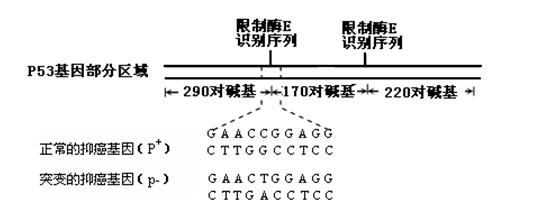
(6)在配制该溶液过程中,下列操作会引起配制溶液浓度偏高的是___________________。
①没有洗涤烧杯和玻璃棒 ②所用天平的砝码生锈
③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视标线
⑤定容时仰视标线
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
知识点:综合性实验
![]()
略