下列说法不正确的是( )
A.工业合成氨的过程是固氮的过程
B.为防止粮食、罐头、水果等食品腐烂,常用氮气做保护气
C.CO、NO、 NO2都是大气污染气体,在空气中都能稳定存在
D.过量SO2通入紫色石蕊试液,溶液只变红不褪色
知识点:基本概念、基本理论的综合运用
C
略
NA表示阿伏加德罗常数。下列说法中正确的是( )
A.Cu和足量的稀硝酸反应产生4.48L气体时,转移的电子数为0.6NA
B.1.2g NaHSO4晶体中阳离子和阴离子的总数为0.03 NA
C.标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为2NA
D.S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA
知识点:化学中常用计量
D
略
下列离子方程式正确的是( )
A.用KIO3 氧化酸性溶液中的KI: 5I-+IO3-+3H2O =3I2+6OH-
B.工业上尾气中的二氧化硫用过量氨水吸收:![]()
C.向NH4HCO3溶液中加少量的NaOH溶液并加热:NH4+ + OH-![]() NH3↑+H2O
NH3↑+H2O
D.浓硝酸中加入少量铁粉并加热:Fe+3NO3-+6H+![]() Fe3+ +3NO2↑+3
H2O
Fe3+ +3NO2↑+3
H2O
知识点:离子方程式
D
略
下列叙述中正确的是( )
A.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-
B.向某溶液中先滴加CaCl2溶液,产生白色沉淀,再滴加稀盐酸沉淀溶解并产生无色
气体,该气体能使澄清石灰水变浑浊,则该溶液中一定有![]()
C.液溴易挥发,存放液溴应加水封,并保存在棕色试剂瓶中
D.向某溶液中先滴加BaCl2溶液,产生白色沉淀,再滴加稀盐酸白色沉淀不溶解,该
溶液一定含有SO
知识点:物质的检验和鉴别
C
略
硫酸铵在强热条件下分解:4(NH4)2SO4==6 NH3↑+ N2↑+3SO2↑+SO3↑+7H2O若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
A.BaSO3和BaSO4 B.BaS C.BaSO3 D.BaSO4
知识点:氧族元素
A
略
下列溶液暴露于空气中,开始一段时间其pH变小的是(不考虑溶质挥发)( )
①H2S ②H2SO3 ③Na2S ④Ca(OH)2 ⑤氯水 ⑥Na2SO3
A. ①③④ B. ②④⑤⑥ C. ①②④⑤ D. ②③④⑤⑥
知识点:水的电离和溶液的酸碱性
B
略
羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00mL 0.049 mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.50mL 0.020 mol/L的KMnO4酸性溶液完全作用。已知(未配平):FeSO4+KMnO4+H2SO4→Fe2(SO4)3+K2SO4+MnSO4+H2O则在上述反应中,羟胺的氧化产物是( )
A.N2 B.N2O C.NO D.NO2
知识点:氧化还原反应
B
略
(15分)1774年,瑞典化学家舍勒发现软锰矿石(主要成分是MnO2)与浓盐酸混合加热得到黄绿色气体。甲、乙两同学分别利用上述原理制取氯气做实验。
甲同学设计实验测定某混有NaI杂质的食盐样品中氯化钠的纯度,过程如下图所示,完成下列问题:
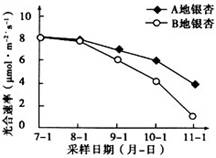
(1)两同学制备氯气的离子方程式为____ ____;
(2)该同学想通过实验验证样品中确实含I-,所用的操作方法及实验现象是
______________________ _____ 。
(3)依据上图,在操作③中可选取的有机溶剂为 ( )
A、酒精 B、苯 C、四氯化碳 D、直溜汽油
(4)试计算原食盐样品中氯化钠的质量分数为_ _ __。
(5)乙同学将制得的纯净氯气缓慢通入FeI2、FeBr2的混合溶液中,溶液中某些离子的物质的量变化如下图所示。已知:2Fe2++Br2===2Fe3++2Br- 2Fe3++2I-===2Fe2++I2
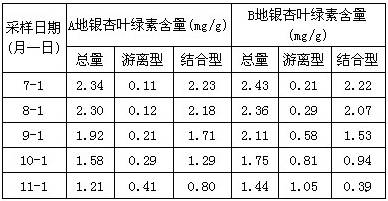
① Fe2+、Br- 、I-的还原性强弱比较:
②当通入2molCl2时,溶液中发生的离子反应总方程式为:
③原溶液中n(Fe2+):n(I-):n(Br-)=
知识点:卤素
( 15分)
(1)MnO2+4H++ 2Cl-=== Mn2++Cl2↑+2H2O ( 2分)
(2)取少量样品溶于水再滴加硝酸酸化的AgNO3溶液,观察是否有黄色沉淀生成,即可证明是否有I-。( 2分)(其它答案合理也给分)
(3) BD( 2分); (4)88.1% ( 3分)
(5)①I-> Fe2+>Br- ( 2分)
②2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- (2分)
③ 2:1:3 ( 3分)
略
(14分)A、B、C、D、E为五种中学常见物质,均含有同一种元素,有如图所示的转化关系。
(1)若A为难溶于水,微溶于酒精,易溶于二硫化碳的固体单质,
B→C为工业生产中的重要反应,则:
①A为 ;E的电子式为 ;
②写出D→B属于氧化还原反应的化学方程式:
(2)若A为单质,且五种物质所含相同元素的价态均不相同,则:
①E的空间构型为 ;
②写出E→B的化学方程式:
该反应中氧化产物与还原产物的物质的量之比为
③写出C→D的化学方程式:
知识点:无机框图推断
( 14分)
(1)①
S ( 2分) ![]() ( 2分)
( 2分)
② Cu + 2H2SO4(浓)== Cu SO4 + SO2↑ + 2H2O ( 2分)
(2)①三角锥形( 2分)
②4NH3 + 5O2 = 4NO + 6H2O(2分) 2:5 ( 2分)
③3NO2 + H2O = 2HNO3 + NO ( 2分)
略
(14分)某校学生活动小组设计如图所示装置探究工业制硫酸接触室中反应产物,并测定此条件下二氧化硫的转化率。实验时,装置D锥形瓶中溶液产生白色沉淀,装置E中溶液褪色。
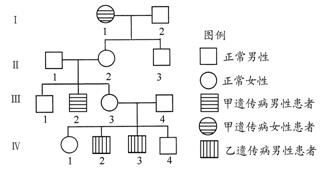
(1)实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)。
A.往烧瓶中加入Na2SO3粉末 B.加热 C.往烧瓶中加入浓硫酸
(2)为了提高测定SO2转化率的准确度,下列操作或改进可行的是( )
A.熄灭酒精灯后,立刻停止通入SO2和O2
B.熄灭酒精灯后,停止通入SO2,继续通入O2一段时间
C.熄灭酒精灯后,停止通入O2,继续通入SO2一段时间
(3)D中锥形瓶盛放的溶液可以是(选填序号) 。
①足量澄清石灰水 ②足量小苏打溶液 ③足量盐酸酸化的氯化钡溶液
④足量硝酸钡溶液
(4)SO2中的S元素显+4价,具有较强还原性,利用SO2的这一点性质,F中盛放的试
剂也可用 代替。
(5)若从锥形瓶溶液中得到的沉淀质量为m g,要测定该条件下二氧化硫的转化率,
实验时还需要测定的数据是(选填序号)
① 装置F增加的质量a g ② 装置A中亚硫酸钠减少的质量b g
③ 装置B增加的质量c g ④ 装置E增加的质量d g
则此条件下二氧化硫的转化率是 ______________ __________________
(用含有m、a、b、c、d中的一种或几种字母的代数式表示,不要化简)。
知识点:氧族元素
( 14分)
⑴ABC(3分) ⑵ B ( 2分) ⑶ ③;( 2分)
(4)酸性高锰酸钾或溴水(2 分) (5)①④(2分)  ×100%(3分)
×100%(3分)
略
(15分)(1)大气中SO2和NOx是形成酸雨的主要物质。某地酸雨中可能含有下列离子:Na+、Mg2+、NH4+、SO32-、SO42-、NO3-等。某研究小组取该地一定量的酸雨分成4份,进行如下实验:第一份酸化后滴加适量的淀粉KI溶液,呈蓝色;第二份滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;第三份滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝;请回答下列问题:
①该酸雨中肯定存在的离子有 ;肯定不存在的离子有 ,说明其不存在的理由: 。
②写出试液中滴加淀粉KI溶液所发生反应的离子方程式:
。
(2) 铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l 、+2。已知Cu2O与稀硫酸反应后溶液呈蓝色并有红色固体生成。现向Cu、Cu2O和CuO组成的混合物中,加入2 L 0.6 mol/L HNO3溶液恰好使混合物溶解,同时收集到4480 mL NO气体(标准状况)。请回答下列问题:
①写出Cu2O跟稀硝酸反应的离子方程式
。
②若将上述混合物用足量的H2加热还原,所得到固体的质量为 。
③若混合物中含0.2 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4
的物质的量为 。
知识点:物质的检验和鉴别
( 15分)
(1)① SO42-、NO3-、NH4+ ;( 2分) SO32-;( 1分)
SO32-具有较强的还原性,酸性条件下,与NO3-不能共存。( 2分)
②6I- + 2NO3- + 8H+ = 3I2 + 2NO↑+ 4H2O ( 2分)
(2)① 3 Cu2O +14 H+ + 2 NO3- = 6 Cu2+ + 2 NO↑ + 7 H2O (3分)
②32 g (2分) ③ 0.2 mol (3分)
略