下列各组物质,需要用丁达尔效应区分的是
A.氯化钠溶液与氯化铁溶液 B.氢氧化铁胶体与碘化银胶体
C.红褐色的某溶液和氢氧化铁胶体 D.氯化钠溶液和硫酸铜溶液
知识点:分散系
C
略
下列说法正确的是
A.摩尔是一种国际基本物理量 B.标准状况下气体摩尔体积约为22.4 L
C.1 mol氧原子的摩尔质量为16 g D.1 mol H2O的质量为18 g
知识点:物质的量
D
略
下列实验中,利用了盐酸的氧化性的是
A.用盐酸除去铜粉中混有的铁粉 B.用浓盐酸和MnO2制氯气
C.用盐酸跟氢氧化钠溶液反应 D.盐酸和硝酸银溶液反应生成白色沉淀
知识点:氧化还原反应
A
略
某盐的混合物中含有0.2 mol Na+、0.4 mol Mg2+、0.4 mol Cl -,则SO42- 为
A.0.1 mol B.0.3 mol C.0.5 mol D.0.15 mol
知识点:溶液浓度的计算
B
略
下列说法正确的是
A.铜、石墨均导电,所以它们均是电解质
B.NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质
C.液态HCl、固体NaCl均不导电,所以HCl、NaCl均是非电解质
D.蔗糖、酒精在水溶液或熔融状态下均不导电,所以它们均是非电解质
知识点:物质的分类
D
略
根据下列化学方程式,判断有关物质的还原性强弱的顺序为
① I2+SO2+2H2O![]() H2SO4+2HI; ② 2FeCl2+Cl2
H2SO4+2HI; ② 2FeCl2+Cl2![]() 2FeCl3;
2FeCl3;
③ 2FeCl3+2HI![]() 2FeCl2+2HCl+I2
2FeCl2+2HCl+I2
A.I->Fe2+>Cl->SO2 B.Cl->Fe2+>SO2>I-
C.Fe2+>I->Cl->SO2 D.SO2>I->Fe2+>Cl-
知识点:氧化还原反应
D
略
分类是学习和研究化学的一种重要方法,下列分类合理的是
A.K2CO3和K2SO4都属于盐 B.KOH和Na2CO3都属于碱
C.NaHSO4和HNO3都属于酸 D.Na2O和SiO2都属于氧化物
知识点:物质的分类
AD
略
下列有关气体的叙述中,错误的是
A.不同的气体,若体积不同,则它们所含的分子数肯定不同
B.气体的摩尔质量越大,体积越大
C.当分子数目相同时,气体体积的大小主要决定于气体分子之间的距离
D.一定温度和压强下,气体分子的物质的量决定了它们的体积
知识点:物质的量
AB
略
下列各组中的离子,能在溶液中大量共存的是ks5u
A.K+、H+、SO42-、OH- B.Na+、Ca2+、CO32-、NO3-
C.Na+、NH4+、Cl-、CO32- D.Na+、Mg2+、Cl-、SO42-
知识点:离子共存
CD
略
用NA表示阿伏加德罗常数,下列说法中正确的是
A.在常温常压下,11.2 L氯气所含的原子数目为NA
B.32 g氧气含的原子数目为2NA
C.5.6 g铁与足量盐酸反应转移的电子数为0.2 NA
D.如果5.6 L N2含有n个氮分子,则阿伏加德罗常数一定约为4 n
知识点:物质的量的计算
CB
略
下列溶液的溶质都是强电解质,这些溶液中的Cl-浓度与50 ml 1 mol˙L-1 MgCl2溶液中的Cl-浓度相等的是
A. 100 ml 1 mol˙L-1 NaCl溶液 B. 25 ml 1 mol˙L-1 CaCl2溶液
C. 25 ml 2 mol˙L-1 KCl溶液 D. 50 ml 1 mol˙L-1 AlCl3溶液
知识点:溶液浓度的计算
BC
略
在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐(BrO3-)”这一潜在致癌物质被做了严格限制。有关专家解释,矿泉水在开采过程中会含有少量溴化物(Br-),在后续的生产过程中经臭氧(O3)处理逐渐转化成溴酸盐。下列有关该转化过程的认识正确的是
A.该过程中溴化物(Br-)失去电子
B.该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂
C.该过程中溴元素被还原,氧元素被氧化
D.该过程中溴元素发生氧化反应,氧元素发生还原反应
知识点:氧化还原反应
AD
略
无论在化学实验室还是在家中进行实验或探究活动,都必须注意安全和操作正确。下列实验操作正确的是
A.为制取Fe(OH)3胶体,可将FeCl3溶液加热煮沸即得
B.试管、蒸发皿可直接加热,烧杯和烧瓶加热时要垫上石棉网
C.不慎将酒精洒到桌面上引起着火,应立即用较多的水浇灭
D.稀释浓H2SO4时,先在烧杯中加一定量的水,边搅拌边慢慢加入浓H2SO4
知识点:化学实验安全常识
BD
略
下列离子方程式正确的是
A.氧化镁与稀盐酸混合: MgO + 2 H+ == Mg2+ + H2O
B.三氯化铝溶液中加入过量氨水:Al3++ 3OH– == Al(OH)3↓
C.铜片插入硝酸银溶液中:Cu + Ag+ = Cu2+ + Ag
D.在硫酸氢钠溶液中加入Ba(OH)2溶液至溶液中性(pH=7):
2H++SO42-+Ba2++2OH– == BaSO4↓+2H2O
知识点:离子方程式
AD
略
(14分)(1)1.5mol H3PO4的质量是 ,含有 个H3PO4分子;(2)同温、同压下等质量的SO2和NO2,它们所占的体积比为 ,所含氧元素的物质的量之比为______________________;
(3)2 mol O2与1 mol O3的摩尔质量的比是______________。
(4)某化合物的相对分子质量为m,在t ℃ 时A ml该化合物的饱和溶液为B g,将其蒸干后得到固体C g。该化合物在t ℃ 时的溶解度为 g,该饱和溶液中溶质的物质的量浓度为 mol/L。
知识点:化学计算的综合运用
(共14分,每空2分) (1)147 g 1.5NA(9.03×1023) (2)5:4 5:6
(3)2:3
(4)![]()
略
(7分)用于提纯或分离物质的方法有: A.萃取分液 B.加热分解 C.结晶
D.分液 E.蒸馏 F.过滤、G.渗析等,请将提纯或分离的序号填在后面横线上。
(1)分离饱和食盐水与泥沙的混合物 (2)分离水和汽油的混合物___
(3)海水淡化 (4)从碘水里提取碘_
(5)除去氢氧化铁胶体中混有的氯离子、钠离子 (6)除去氧化钙中的碳酸钙
(7)分离NaCl和KNO3的混合物
知识点:物质的分离、除杂和提纯
.(共7分,每空1分)(1)F (2)D (3)E (4)A
(5)G (6)B (7)C
略
8分)下表是某地市场销售的一种“加碘食盐”包装袋上的部分文字说明。
配 料
氯化钠、碘酸钾
含碘量
(20mg~40mg)/1kg
保质期
18个月
食用方法
勿长时间炖炒
贮藏指南
避热、防潮
(1)已知碘在碘酸钾中的化合价为+5,碘酸钾的化学式为_________________。
(2)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是_______________。
(3)用单质碘与氯酸钾发生置换反应可制得碘酸钾,该反应的化学方程式为__________。
该反应中氧化剂是: ,氧化产物是: ,若有0.2mol Cl2产生,则转移电子的物质的量为 。
知识点:卤素
(共8分)(1)KIO3 (1分) (2) 受热分解(热不稳定)(1分)
(3)I2+2KClO3==2KIO3+Cl2(3分) KClO3(1分) KIO3(1分) 1mol(1分)
略
(11分)某溶液含有Ba2+、 Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下(请写出最佳答案):
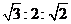
(1)所加试剂的化学式:A_________、B__________、C__________
(2)写出生成沉淀1的离子方程式_________________________;
生成沉淀3的离子方程式_____________________________;
(3)试猜想上述溶液中一定存在的另一种离子是__________(写化学式),请写出该离子所对应的一种盐的电离方程式____________________。
知识点:物质的分离、除杂和提纯
(共11分)(1) A.HCl B.Na2SO4 C.NaOH (各1分)
(2) Ag+ + Cl- = AgCl↓ ;Cu2+ + 2OH- = Cu(OH)2↓ (各2分)
(3)NO3-;NaNO3=Na++NO3-。(各2分)
略
(10分) 某实验需要用92 ml 3.0 mol˙L-1 稀硫酸,现用质量分数为98%的浓硫酸配制,其实验步骤如下:① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④ 转移、洗涤 ⑤ 定容 ⑥ 摇匀
回答下列问题:
(1)若所用浓硫酸密度为1.84 g/cm3,则该浓硫酸的物质的量浓度为 ,配制上述稀硫酸所需浓硫酸的体积是 (小数点后保留一位),量取浓硫酸所用的量筒的规格是 ,(从下列选项中选用A.10 ml B.20 ml C.50 ml D.100 ml)。
(2)为了保证实验的准确性,在第③和第④步操作之间还应该加多一步什么操作 ,在第⑤步操作中最后要改用 实验仪器。ks5u
(3)如果在配制溶液过程中出现下列情况对所配稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视溶液的凹液面
E.定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度
知识点:仪器和基本操作
(共10分,每空1分)(1)18.4 mol/L, 16.3 ml B
(2)冷却, 胶头滴管
(3) A.偏小 B.无影响 C.偏小 D.偏大 E.偏
略