下列说法错误的是( )
A.钠的单质在化学反应中只能做还原剂
B.钠钾合金通常状况下呈液态,可用作快中子反应堆的热交换剂
C.钠在自然界中不可能以游离态存在
D.钠元素性质活泼,不可能应用在电光源上
知识点:钠和碱金属
D
略
有关溶液中所含离子的检验,下列判断正确的是( )
A.加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+存在
B.加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有CO32-存在
C.用某溶液做焰色反应时火焰为黄色,则该溶液中一定有钠元素,可能有钾元素
D.分别含Mg2+、Cu2+、Fe2+和Na+的四瓶盐溶液,只用NaOH溶液不能一次鉴别开
知识点:物质的检验和鉴别
C
略
以下关于钠及其化合物的叙述中正确的是( )
A.金属钠是活泼金属,应保存在冷水中
B.钠原子和钠离子具有相同的化学性质
C.钠投入水中熔化成小球,说明钠的熔点低,且反应放热
D.刚切开的金属钠为银白色,在空气中很快变暗,生成过氧化钠
知识点:钠和碱金属
C
略
在反应3NO2+H2O=2HNO3+NO中,得电子的原子和失电子的原子个数之比为( )
A.3:1 B.1:l C.1:2 D.2:1
知识点:氧化还原反应
C
略
下列有关金属的说法正确的是( )
A.金属原子只有还原性,金属阳离子只有氧化性
B.金属单质在常温下都是固体
C.含金属元素的离子都是阳离子
D.金属阳离子被还原不一定得到金属单质
知识点:金属及其化合物
D
略
人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变为Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有 ( )
A.酸性 B.碱性 C.氧化性 D.还原性
知识点:化学与生活
D
略
制备硅单质时,主要化学反应如下:
(1) SiO2+2C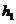 Si+2CO
(2)Si+2Cl2
Si+2CO
(2)Si+2Cl2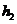 SiCl4
SiCl4
(3)SiCl4+2H2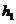 Si+4HCl 对上述三个反应,下列说法不正确的是 ( )
Si+4HCl 对上述三个反应,下列说法不正确的是 ( )
A.(1)(3)为置换反应 B.(1)(2)(3)均为氧化还原反应
C.(2)为化合反应 D.三个反应的反应物中硅元素均被还原
知识点:氧化还原反应
D
略
在FeCl3、CuCl2和HCl的混合溶液中加入铁粉,待反应结束后,将剩余的固体滤出,发现固体能被磁铁吸引,则反应后溶液中大量存在的阳离子是 ( )
A.Fe2+ B.H+ C.Cu2+和Fe2+ D.Fe3+和Cu2+
知识点:金属及其化合物
A
略
下列说法正确的是 ( )
A.除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测定
C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D.加入盐酸可以除去硫酸钠中的少量碳酸钠杂质
知识点:物质的分离、除杂和提纯
A
略
下列物质既能与盐酸反应,又能与烧碱溶液反应的是( )
①Al2O3 ②Al(OH)3 ③Al ④NaHCO3 ⑤CaCO3
A.①②③④⑤ B.①②③④ C.①②③ D.①②
知识点:元素及其化合物的综合运用
A
略
实验室里利用以下反应制取少量氮气:NaNO2+NH4Cl=NaCl+N2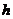 +2H2O。关于该反应的下列说法正确的是( )
+2H2O。关于该反应的下列说法正确的是( )
A.N2既是氧化剂,又是还原剂 B.每生成1molN2转移的电子的物质的量为6mol
C.NH4Cl中的氮元素被还原 D.NaNO2是氧化剂
知识点:氧化还原反应
D
略
由下列实验事实得出结论不正确的是( )
A.蔗糖加入浓硫酸后变黑,说明浓硫酸具有脱水性
B.浓硫酸可用作气体干燥剂,说明浓硫酸具有吸水性
C.铜与浓硫酸共热有刺激性气味气体放出,说明浓硫酸具有强氧化性
D.SO2能使紫红色的酸性高锰酸钾溶液褪色,说明SO2具有漂白性
知识点:氧族元素
D
略
纯碱和小苏打是厨房常备的物质,它们都是白色固体。下列区分这两种物质的方法正确的是( )
A.分别加热两种样品,全部分解且没有固体剩余的原样品是小苏打
B.取等质量样品分别与足量的盐酸反应,产生二氧化碳多的样品是纯碱
C.用洁净铁丝蘸取两种样品分别在火焰上灼烧,焰色呈黄色的样品是纯碱
D.取等质量样品分别加入等体积的水配成溶液,各滴加酚酞,溶液颜色更深的原样品是纯碱
知识点:碳族元素
D
略
下列反应的离子方程式中,书写正确的是( )
A.实验室用大理石跟稀盐酸制取二氧化碳:2H++CO32-==CO2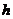 +H2O
+H2O
B.将铝粉投入氢氧化钠溶液中:2Al+2OH-==2AlO2-+H2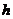
C.铁粉与氯化铁溶液反应:Fe+Fe3+==2Fe2+
D.金属钠与水反应:2Na+2H2O=2Na++2OH-+H2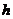
知识点:离子方程式
D
略
有两种金属的合金12g,与足量稀硫酸反应后,在标准状况下产生气体11.2L,则组成该合金的金属可能是( )
A.Mg和Al B.Cu和Zn C.Fe和Zn D.Al和Fe
知识点:化学式的计算
D
略
下列反应中,硝酸既表现酸性,又表现氧化性的是( )
A.Fe2O3跟稀硝酸反应 B.Cu跟稀硝酸反应
C.CuO跟稀硝酸反应 D.Al(OH)3跟稀硝酸反应
知识点:氧化还原反应
B
略
下列离子方程式中正确的是( )
A.H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-==BaSO4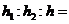 +H2O
+H2O
B.铁粉与氯化铁溶液反应:Fe+Fe3+===2Fe2+
C.向Na2CO3溶液中通入CO2:CO32-+CO2+H2O==2HCO3-
D.将少量SO2通入到NaClO溶液里:SO2+2ClO-+H2O=SO32-+2HClO
知识点:离子方程式
C
略
下列各组离子,在碱性溶液中能大量共存,且溶液为无色透明的是( )
A.K+ MnO4- Cl- SO42- B.Na+ H+ NO3- Cl-
C.Na+ SO42- Cu2+ Cl- D.Na+ NO3- Cl- Ba2+
知识点:离子共存
D
略
下列说法中正确的是( )
A.用光亮洁净的铁丝蘸取某无色溶液,在无色灯焰上灼烧时观察到黄色火焰,则该溶液中一定含Na+,一定不含K+
B.酸、碱中和反应的实质是H+与OH-结合生成水,故酸碱中和反应的离子反应都可用H++OH-==H2O来表示
C.SiC俗称金刚砂,可用作砂纸、砂轮的磨料
D.Na2O与Na2O2都能和水反应生成NaOH,所以它们都是碱性氧化物
知识点:元素及其化合物的综合运用
C
略
在一定温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原温度,下列说法正确的是 ( )
A.溶液中的Na+浓度增大,有O2放出
B.溶液中的OH-浓度不变,有H2放出
C.溶液中的Na+数目减小,有O2放出
D.溶液中OH-的浓度增大,有O2放出
知识点:钠和碱金属
C
略
能与SO2气体发生反应且有沉淀产生的是 ( )
①NaOH溶液 ②H2S溶液 ③Ba(NO3)2酸性溶液④CaCl2和氨水的混合液
A.①②③ B.②③④ C.全部 D.①③④
知识点:氧族元素
B
略
将0.2 molMnO2和含0.6molHCl的浓盐酸混合后加热,反应完全后向剩余溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为(不考虑盐酸的挥发) ( )
A.等于0.3 mol B.小于0.3mol
C.大于0.3mol,小于0.6mol D.等于0.6mol
知识点:化学式的计算
C
略