将下列各组物质按单质、酸、碱、盐分类顺序排列,其中正确的是
A.水银、硫酸、烧碱、蓝矾 B.碘酒、盐酸、烧碱、硫酸钡
C.氧气、硝酸、纯碱、胆矾 D.铁、醋酸、石灰水、氯化铜
知识点:物质的分类
A
略
“绿色化学”要从根本上消灭污染,是一门能彻底阻止污染产生的科学。因此设计化学反应流程时要考虑“原子经济”(即原子利用率),下列反应类型从理论上看原子利用率可达到100%的是(原子利用率是指反应物中的所有原子进入期望产物中的百分比)
A.分解反应 B.复分解反应 C.化合反应 D.置换反应
知识点:化学用语及其规律
C
略
2010年国庆期间我国成功发射了“嫦娥二号”绕月卫星,为中国人登月打下了坚实的基础。据预测,在月球的土壤中含有较丰富的质量数为3的氦,它是核聚变的重要原料。氦的这种核素应表示为
A. B.
B. C.
C. D.
D.
知识点:原子结构与性质
B
略
瘦西湖风景区被称为天然氧吧,其原因是空气中的自由电子附着在分子或原子上形成空气负离子,被称为“空气维生素”。O2-就是一种空气负离子,其摩尔质量为
A.32 g B.33 g C.33 g·molˉ1 D. 32 g·molˉ1
知识点:物质的量
D
略
下列说法正确的是
A.锌、石墨均能导电,所以它们均是电解质
B.NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质
C.液态HCl、固体KNO3均不能导电,所以HCl、KNO3均是非电解质
D.蔗糖、酒精在水溶液和熔融状态下均不能导电,所以它们均是非电解质
知识点:物质的分类
D
略
人们对纳米材料的研究最初来源于对胶体的独特性质的兴趣。胶体与其它分散系的本质区别是
A.胶体粒子直径在1-100nm之间 B.胶体有丁达尔现象
C.胶体粒子能穿过滤纸 D.胶体有相对稳定性
知识点:电化学基础
A
略
下列说法不正确的是
A.实验室中的金属钠通常保存在盛有煤油的试剂瓶中,以便隔绝空气和水
B.150 mL 1 mol·L1NaCl溶液与75 mL 1 mol ·L1 Na2CO3溶液中Na+物质的量浓度相等
C.金属钠投入硫酸铜溶液中,反应后会生成蓝色沉淀
D.用洁净的铂丝蘸取样品在无色火焰上灼烧看见黄色火焰,说明样品中含钠元素
知识点:钠和碱金属
B
略
对于相同物质的量的SO2和SO3,下列说法中正确的是
A.硫元素的质量比为5∶4 B.分子数之比为1∶1
C.原子总数之比为4∶3 D.质量之比为1∶1
知识点:物质的量
B
略
下列溶液中Cl-浓度最小的是
A.200mL 2mol/L MgCl2溶液 B.300mL 2.5mol/L KClO3溶液
C.300mL 2.5mol/L NaCl溶液 D.250mL 1mol/L AlCl3溶液
知识点:溶液浓度的计算
B
略
下列叙述正确的是
A.1 mol H2SO4的质量为98g/mol
B.CH4的密度为16/22.4 g/L
C.6.02×1023个SO2分子的质量为64g
D.标准状况下,1 mol水的体积均为22.4L
知识点:物质的量
C
略
钠与水反应时产生的各种现象如下
①钠浮在水面上;②钠沉在水底;③钠熔化成小球;④小球迅速游动逐渐减小,最后消失;⑤发出嘶嘶的声音;⑥滴入酚酞后溶液显红色。
A.①②③④⑤ B.全部 C.①②③⑤⑥ D.①③④⑤⑥
知识点:钠和碱金属
D
略
传统的引爆炸药由于其中含Pb,使用时将产生污染,同时其引爆后的剩余炸药还严重危害接触者的人身安全,美国UNC化学教授Thomas J.Meyer等研发了环境友好、 安全型的“绿色”引爆炸药,其中一种可表示为Na2R,它保存在水中可以失去活性,爆炸后不会产生危害性残留物。已知10 mL Na2R溶液含Na+的微粒数为N个,该Na2R溶液的物质的量浓度为
A.N×10-2 mol/L B. mol/L
mol/L
C. mol/L D.
mol/L D. mol/L
mol/L
知识点:物质的量
B
略
天宫一号搭载的长征二号火箭使用的主要燃料是偏二甲肼(用R表示)和四氧化二 氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R + 2N2O4 = 3N2 + 4H2O + 2CO2,下列叙述错误的是
A.此反应可在瞬间产生大量高温气体,推动火箭飞行
B.此反应是氧化还原反应,N2O4做还原剂
C.此反应是氧化还原反应,偏二甲肼做还原剂
D.此反应中R的分子式为C2H8N2
知识点:氧化还原反应
B
略
下列说法正确的是(NA表示阿伏加德罗常数的值)
A.常温常压下,18g NH4+所含的电子数为10NA
B.标准状态下,22.4L氧气所含的氧原子数为2 NA
C.56g金属铁与氯气反应时得到的电子数为2NA
D.1 mol由Na2O2和Na2O组成的混合物,其中的钠离子数为4 NA
知识点:物质的量的计算
AB
略
下列电离方程式错误的是
A.CaCl2=Ca2++2Cl- B.NaHSO4=Na++H++SO42-
C.HNO3=H++NO3- D.NaHCO3=Na++H++CO32-
知识点:弱电解质的电离
D
略
下列装置或操作能达到实验目的的是

A.用甲图装置可从食盐水中提取食盐
B.用乙图装置验证NaHCO3和Na2CO3的热稳定性
C.用丙图装置除去乙醇中的水
D.用丁图装置完成酒精萃取碘水中的碘
知识点:仪器和基本操作
B
略
为了除去粗盐中的Ca2+,Mg2+,SO42—及泥沙,得到纯净的NaCl,可将粗盐溶于水,
然后在下列操作中选取必要的步骤和正确的操作顺序
①过滤; ②加过量NaOH溶液; ③加适量盐酸;
④加过量Na2CO3溶液; ⑤加过量BaCl2溶液
A.④②⑤ B.④①②⑤③ C.②⑤④①③ D.①④②⑤③
知识点:物质的分离、除杂和提纯
C
略
对于某些离子的检验及结论正确的是
A.加盐酸有无色气体产生,该气体能使澄清石灰水变混浊,原溶液中一定有CO32—
B.用可溶性钡盐检验SO42—离子的存在时,先在待测溶液中加入盐酸,其作用是排除SO42—以外的其它阴离子及Ag+的干扰
C.加氢氧化钠溶液加热产生的气体使湿润红色石蕊试纸变蓝,原溶液中一定有NH4+
D.在某待测液中滴加碳酸钠溶液有白色沉淀产生,说明待测液中必有Ca2+
知识点:物质的检验和鉴别
BC
略
现有mg某气体,它由三原子分子构成,它的摩尔质量为M g·mol—1。则:
(1)该气体的物质的量为__________________mol。
(2)该气体所含原子总数为________________个。
(3)该气体在标准状况下的体积为_____________L。
知识点:物质的量的计算
(1)m/M (2)1.806×1024m/M (3)22.4m/M
略
实验室需要480 mL 0.5 mol·L-1的NaOH溶液,配制过程中有如下操作步骤:
①把称量好的NaOH固体放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液小心转入 中;
③继续向容量瓶中加蒸馏水至液面距离刻度l~2 cm处,改用胶头滴管小心滴加适量的蒸馏水后停止滴加;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞紧,充分摇匀。
⑥待溶液恢复到室温。
请填写下列空白:
(1)实验操作步骤的正确顺序为(填序号) ___________。步骤②中该填 。
(2)实验中用托盘天平称取NaOH固体的质量是 。
(3)若实验时出现如下情况,使所配溶液的物质的量浓度偏高的有 。
A.在托盘天平上称取氢氧化钠固体时,将砝码放在天平的左盘,盛有氢氧化钠固体的小烧杯放在天平的右盘。
B.定容时,俯视刻度线。
C.移液后,未洗涤烧杯和玻璃棒。
D.容量瓶中原有少量的蒸馏水。
E.前一次配制定容时加水超过了刻度线,所以将溶液倒掉了,后来容量瓶未用蒸馏
水润洗,就重新配制溶液
知识点:仪器和基本操作
(1)①⑥②④③⑤ 500 mL容量瓶 (2)10.0g (3)BE
略
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳制取漂白粉,反应的化学方程式为: 。
(2)漂白粉的有效成分是(填化学式) 。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 。
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号) 。
(5)将漂白粉溶于适量水中,呈白色浊状物,静置沉降,取少许上层清液,滴加几滴酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈 性,并可能具有 性。
知识点:卤素
(1)2Cl2 + 2Ca(OH)2 =CaCl2 + Ca(ClO)2 + 2H2O
(2)Ca(ClO)2
(3)Ca(ClO)2+ CO2 + H2O = CaCO3 ↓+ 2HClO
(4)(1) (5)碱性 漂白性(强氧化性)
略
海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:

(1)指出提取碘的过程中有关的实验操作名称:① ③ 。
(2)过程②中充入适量Cl2的方程式是 。
(3)操作③中所用的有机试剂可以是 (只填一种)。
(4)操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50 mL碘水和15 mL有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
(a)过程③正确操作步骤的顺序是:(填编号字母)
→ → →A→ H→ →E →F。
(b)上述G步操作的目的是: 。
知识点:综合性实验
(1)① 过滤 ③ 萃取、分液
(2)2I—+ Cl2= I2+2Cl—
(3)苯(或四氯化碳)
(4)(a)C B D A H G E F (b)保持分液漏斗内外压力平衡,使液体易于流下。
略
如图中,A是氯气的发生装置,B、C是净化气体的装置,D中装铁丝网;反应后E的底部有棕色固体聚集;F是吸收多余气体的装置。

(1)上述装置中有一处错误,请指出是 处(用字母表示)。
(2)通过B是为了除去 ,在B中应加入 ;通过C是为了除去 。
(3)写出D、F中发生反应的化学方程式 、 。
(4)如果A中产生氯气3.36L(标准状况),请计算:
①写出A中方程式,并用双线桥法分析A中的电子转移情况 。
②消耗MnO2的物质的量 。③被氧化的HCl的物质的量 。
知识点:物质的制备
(1)B (2)HCl 饱和食盐水 水蒸气
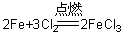
(3) Cl2+2NaOH=NaCl+NaClO+H2O
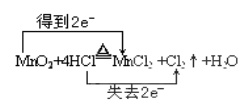
(4)①
②0.15mol ③0.3mol
略