化学与生产、生活、社会密切相关。下列有关说法错误的是( )
A.利用农作物秸秆制取乙醇 B.回收地沟油,制备生物柴油
C.焚烧废旧塑料,防止白色污染 D.开发利用各种新能源,减少对化石燃料的依赖
知识点:化学
C
A、秸秆成分是纤维素,纤维素水解最终产物是葡萄糖,利用葡萄糖制取乙醇,故说法正确;B、利用地沟油,制备生物柴油,故说法正确;C、焚烧塑料,产生有毒物质,污染环境,故说法错误;D、开发新能源,减少对化石燃料的依赖,减少对环境的污染,故说法正确。
下列有关化学用于表述正确的是( )
A.质子数和中子数均为6的碳原子 C
C
B.溴化铵的电子式:
C.氢氧化钠的电子式:
D.2-丙醇的结构简式: 
知识点:化学
D
A、左上角应是质量数,即数值为12,故错误;B、没有体现出Br-的最外层电子数,故错误;C、氢氧化钠是离子化合物,应体现出阴阳离子,故错误;D、2是羟基的位置,故正确。
下列有关物质的性质与用途具有对应关系的是( )
性质
用途
A
液氨气化吸热
可用作制冷剂
B
NH4HCO3受热易分解
可用作氮肥
C
二氧化硅能与HF反应
可用作光导纤维
D
二氧化硫能使溴水褪色
可用作漂白剂
知识点:化学
A
A、氨气易液化,利用液氨的气化,从外界吸收热量,常用作制冷剂,故正确;B、用作氮肥,是因为含有氮元素,与是否分解无关,故错误;C、利用SiO2与HF的反应,雕刻玻璃,与作光导纤维无关,故错误;D、发生的是氧化还原反应,利用的是SO2的还原性,不是漂白性,故错误。
下图是部分短周期主族元素原子半径与原子序数的关系图。下列说法错误的是( )

A.X、R的最高化合价相同
B.简单离子的半径:X>Y>Z
C.Y、Z、R最高价氧化物对应水化物相互之间可以发生反应
D.电解熔融的X与Z组成的化合物可以得到单质Z
知识点:化学
A

下列反应的离子方程式书写不正确的是( )
A.用氨水吸收过量的二氧化硫:NH3·H2O+SO2=HSO3-+NH4+
B.用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+ = I2+2H2O
C.向NH4Al(SO4)2溶液中滴入Ba(OH) 2溶液恰好使SO42-完全沉淀:2Ba2+ + Al3+ + 2SO42- + 4OH- = AlO2- + 2BaSO4↓+ 2H2O
D.向含0.1mol·L-1 Na2CO3和0.2mol·L-1 NaOH的混合溶液中加入等体积的0.15mol·L-1的硫酸:CO32-+3H++2OH- = 2H2O+HCO3-
知识点:化学
C
A、A、氨水吸收过量的SO2,因此发生NH3·H2O+SO2=NH4HSO3,离子反应式是NH3·H2O+SO2=NH4++HSO3-,故说法正确;B、利用过氧化氢的强氧化性,把I-氧化成I2,离子反应式为H2O2+2I-+2H+=2H2O+I2,故说法正确;C、1molNH4Al(SO4)2中有2molSO42-,SO42-全部转化成沉淀,需要2molBa(OH)2,结合OH-的能力:Al3+>NH4+,当Al3+全部转化成Al(OH)3时,继续滴加Ba(OH)2时,OH-先结合NH4+生成NH3·H2O,离子反应式为2Ba2++4OH-+Al3++NH4+=2BaSO4↓+NH3·H2O+Al(OH)3↓,故说法错误;D、设溶液的体积为1L,硫酸先和氢氧化钠反应:OH-+H+=H2O,消耗H+的物质的量为:0.2mol,剩余H+的物质的量(0.15×2-0.2)mol=0.1mol,碳酸钠和H+反应:CO32-+H+=HCO3-,n(CO32-)=0.1mol,因此两者恰好完全反应,因此总离子反应反应式为CO32-+3H++2OH- = 2H2O+HCO3-,故说法正确。
【点睛】离子反应方程式正误判断时,常见的错误类型有:不符合客观事实、化学式的拆分不正确、反应物间量的关系不正确、违背三个守恒(之一);一种氧化剂(还原剂)多种还原剂(氧化剂)反应,注意反应的先后顺序,判断氧化性或还原性强弱,存在先后顺序,此类题属于中档题。
巧妙的实验设计有助于更好地解决问题。下列装置不能达到实验目的的是( )

A.用装置甲验证HCl气体易溶于水
B.用装置乙验证SO2具有漂白性
C.用装置丙采集到的压强数据判断铁钉发生析氢腐蚀还是吸氧腐蚀
D.用装置丁检验NH4Cl分解产生的气体
知识点:化学
B

下列说法正确的是( )
A.铅蓄电池放电一段时间后,负极质量减小,正极质量增加
B.298K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其ΔH<0
C.pH=3的盐酸与pH=11的某碱溶液等体积混合,溶液呈碱性,说明该碱为强碱
D.标准状况下,22.4L甘油中含有3mol羟基(—OH)
知识点:化学
B
A、铅蓄电池,正极反应式PbO2+4H++SO42-+2e-=PbSO4+2H2O,正极质量增大,负极电极反应式Pb+SO42--2e-=PbSO4,负极质量增大,故错误;B、根据△G=△H-T△S,自发进行,△G<0,根据反应方程式,此反应是熵减,即△S<0,低温下能自发进行,因此△H<0,故正确;D、甘油标准状况下不是气体,故错误。
在给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
A.NH3 NO2
NO2 HNO3
HNO3
B.SiO2 SiCl4
SiCl4  Si
Si
C.Al2O3 NaAlO2
NaAlO2 Al(OH)3
Al(OH)3
D.Na Na2O2
Na2O2 Na2CO3
Na2CO3
知识点:化学
C
A、氨气的催化氧化成生成的是NO,不是NO2,故错误;B、SiO2不与HCl反应,应先和C发生生成Si,然后和氯气反应生成SiCl4,故错误;C、氧化铝是两性氧化物,和氢氧化钠生成NaAlO2,碳酸的酸性强于偏铝酸,偏铝酸钠溶液中通入CO2,产生白色沉淀Al(OH)3,故正确;D、金属钠在加热或点燃的条件下生成过氧化钠,常温下生成Na2O,题目中金属钠是在常温下和氧气反应,故错误。
以N2和H2为反应物、溶有A的稀盐酸为电解质溶液,可制成能固氮的新型燃料电池,原理如下图所示。下列说法错误的是 ( )

A.b电极为负极,发生氧化反应
B.a电极发生的反应为N2+8H++6e-=2NH4+
C.A溶液中所含溶质为NH4Cl
D.当反应消耗1mol N2时,则消耗的H2为67.2L
知识点:化学
D
A、此电池总反应式是:N2+3H2+2HCl=2NH4Cl,氢气的化合价升高,失去电子,根据原电池的工作原理,负极失去电子,化合价升高,因此b极为负极,发生氧化反应,故说法正确;B、环境是酸性环境,因此有N2-6e-+6e-=2NH4+,故说法正确;C、根据选项A中总电极反应式,分离出的A为NH4Cl,故说法正确;D、题目没有说明是否是标准状况,故说法错误。
H2与ICl的反应分①、②两步进行,其能量曲线如图所示,下列有关说法错误的是 ( )

A.反应①、反应②均为放热反应
B.反应①、反应②均为氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能无关
D.反应①、反应②的焓变之和为ΔH=-218kJ·mol-1
知识点:化学
C
A、反应物的总能量大于生成物的总能量,说明此反应是放热反应,根据图像,故说法正确;B、反应①中H的化合价由0价→+1价,部分I的化合价降低,属于氧化还原反应,反应②中,I的化合价发生变化,属于氧化还原反应,故说法正确;C、反应①比反应②慢,说明反应①中正反映的活化能较小,反应②中正反应的活化能较大,故说法错误;D、根据盖斯定律,只与始态和终态有关,与反应的途径无关,因此△H=-218kJ·mol-1,故说法正确。
(不定项)合成药物异搏定路线中某一步骤如下:

下列说法错误的是( )
A.物质X中所有碳原子可能在同一平面内
B.可用FeCl3溶液鉴别Z中是否含有X
C.等物质的量的X、Z 分别与H2加成,最多消耗H2的物质的量之比为3:5
D.等物质的量的X、Y分别与NaOH反应,最多消耗NaOH的物质的量之比为1∶2
知识点:化学
C
A、苯环空间构型是平面正六边形,羰基是平面结构,因此所有碳原子可能在一平面,故说法正确;B、X中含有酚羟基,Y中不含酚羟基,加入FeCl3溶液,X发生显色反应,而Y不行,因此可以鉴别,故说法正确;C、1molX中含有1mol苯环和1mol羰基,1mol苯环需要3mol氢气,1mol羰基需要1mol氢气,因此1molX需要4mol氢气,1molZ中含有1mol苯环、2mol碳碳双键,酯中羰基和羧基中羰基不能与氢气发生加成,因此1molZ最多消耗5mol氢气,故错误;D、1molX中只含有1mol酚羟基,即1molX消耗1mol氢氧化钠,1molY中含有1mol酯基、1mol溴原子,因此消耗2mol氢氧化钠,故说法正确。
(不定项)下列根据实验操作和现象所得出的结论正确的是( )
选项
实验操作及现象
结论
A
测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH,前者pH比后者的大
非金属性:S>C
B
向苯酚浊液中滴加Na2CO3溶液,浊液变澄清
CO32-结合质子能力比C6H5O-强
C
向10 mL 0.2 mol·L-1NaOH溶液中滴入2滴0.1 mol·L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol·L-1FeCl3溶液,白色沉淀转化为红褐色沉淀
相同温度下的Ksp:Mg(OH)2>Fe(OH)3
D
将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色
Fe3+的氧化性大于I2
知识点:化学
BD
A、通过酸性比较非金属性,应是最高价氧化物对应水化物的酸性,酸性越强,非金属性越强,但Na2SO3中S的价态是+4价,不是最高价,故错误;B、溶液变澄清,发生反应生成苯酚钠和碳酸氢钠,说明CO3-结合质子能力强于C6H5O-,故正确;C、氢氧化钠过量,再加入FeCl3溶液,和过量的NaOH反应生成沉淀,应是NaOH少量,出现红褐色沉淀,说明Ksp(Mg(OH)2>Ksp(Fe(OH)3,故错误;D、发生2Fe3++2I-=2Fe2++I2,氧化剂的氧化性大于氧化产物的氧化性,Fe3+是氧化剂,I2是氧化产物,故正确。
(不定项)向实验室做完铝热反应(Al和氧化铁)后的混合物中,加入足量稀硫酸将其溶解,室温下向所得溶液中加入指定物质,反应后的溶液中主要存在的离子组正确的是( )
A.通入过量Cl2: Cl-、Fe2+、SO42-、Al3+
B.加入过量NaOH溶液:Na+、AlO2-、SO42-、OH-
C.加入过量氨水:Na+、NH4+、SO42-、AlO2-
D.加入过量铜粉:NO3-、Fe3+、SO42-、Al3+
知识点:化学
B
加入稀硫酸后溶液的离子是Al3+、Fe3+,H+、SO42-,A、通入氯气,Cl2能把Fe2+氧化成Fe3+,故错误;B、加入过量的氢氧化钠溶液,中和H+,Fe3+转化成Fe(OH)3,氢氧化铝表现两性,生成AlO2-,因此反应后的溶液的离子是Na+、AlO2-、SO42-、OH-,故正确;C、氢氧化铝不溶于弱碱,反应后存在的离子是Na+、NH4+、SO42-,故错误;D、加入铜粉后,发生2Fe3++Cu=Cu2++2Fe2+,反应后离子有Fe2+、SO42-、Al3+、H+,故错误。
(不定项)25℃时,下列溶液中微粒的物质的量浓度关系正确的是( )
A.0.1mol·L-1NaHC2O4溶液(pH=5.5):c(Na+)> c(HC2O4-)> c(H2C2O4)> c(C2O42-)
B.0.1mol·L-1NaHS溶液:c(OH-)+ c(S2-)= c(H+)+ c(H2S)
C.0.1mol·L-1CH3COOH溶液和0.1mol·L-1CH3COONa溶液等体积混合:c(Na+)> c(CH3COOH)> c(CH3COO-)> c(H+)> c(OH-)
D.0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液至中性:c(Na+)> c(SO42-)>c(NH4+)> c(OH-)= c(H+)
知识点:化学
BD
A、pH=5.5,说明HC2O4-的电离程度大于水解程度,因此c(C2O42-)>c(H2C2O4),故错误;B、物料守恒:c(Na+)=c(HS-)+c(S2-)+c(H2S),电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-),得到:c(OH-)+ c(S2-)= c(H+)+ c(H2S),故正确;C、CH3COOH的电离程度大于CH3COO-的水解程度,因此是c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-),故错误;D、假设氢氧化钠全部中和NH4HSO4中的H+,2NaOH+2NH4HSO4=Na2SO4+(NH4)2SO4+2H2O,溶质为Na2SO4、(NH4)2SO4,溶液显酸性,确保溶液显中性,继续滴加NaOH,此时的溶质为Na2SO4、(NH4)2SO4、NH3·H2O,因此离子浓度大小顺序是c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-),故正确。
【点睛】本题考查溶液中离子浓度大小比较,在比较中遇见等号,应运用物料守恒、电荷守恒、质子守恒解决问题,①电荷守恒,电解质溶液中,阴离子所带电荷数等于阳离子所带电荷数,②物料守恒,电解质溶液中,某些离子存在的所有形式之和等于其分析浓度,如NaHS中S元素,HS-既能水解也能电离,因此存在HS-、S2-、H2S三种形式,有如下守恒关系:c(Na+)=c(HS-)+c(S2-)+c(H2S),③质子守恒,水电离产生的H+等于水电离出OH-;离子浓度大小比较中注意量、注意弱电解质或盐的水解程度微弱的特点,进行分析,从而得出正确结果。
(不定项)一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:
CO(g)+Cl2(g) COCl2(g)
COCl2(g)
其中容器Ⅰ中5 min时到达平衡。
容器编号
温度/℃
起始物质的量/mol
平衡物质的量/mol
CO
Cl2
COCl2
COCl2
Ⅰ
500
1.0
1.0
0
0.8
Ⅱ
500
1.0
a
0
0.5
Ⅲ
600
0.5
0.5
0.5
0.7
下列说法正确的是( )
A.容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B.该反应的正反应为吸热反应
C.容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D.若起始时向容器Ⅰ中加入CO 0.8 mol、Cl2 0.8 mol,达到平衡时CO的转化率大于80%
知识点:化学
C
根据化学反应速率的数学表达式,v(COCl2)=0.8/(0.5×5)mol/(L·min)=0.32 mol/(L·min),化学反应速率之比等于化学计量数之比,因此v(CO)=v(COCl2)=0.32mol/(L·min),故错误;B、CO(g)+Cl2(g) COCl2(g)
COCl2(g)
起始: 1 1 0
变化: 0.8 0.8 0.8
平衡: 0.2 0.2 0.8 根据平衡常数定义,K=c(COCl2)/=1.6/0.42=10,容器III中的平衡常数K≈4,化学平衡常数只受温度的影响,升高温度,化学平衡常数降低,平衡向逆反应方向移动,即正反应方向是放热反应,故错误;C、
CO(g)+Cl2(g) COCl2(g)
COCl2(g)
起始: 1 a 0
变化: 0.5 0.5 0.5
平衡: 0.5 a-0.5 0.5 化学平衡常数只受温度影响,即有K=0.1/=10,解得a=0.55mol,故正确;D、相当于在I基础上去掉0.2molCO、0.2molCl2,相当于降低压强,平衡向逆反应方向移动,CO的转化率小于80%,故错误。
【点睛】本题考查化学反应速率、化学平衡的计算,化学反应速率的计算应注意是变化浓度与时间的比值,许多学生往往用变化的物质的量与时间的比值,同时用化学反应速率之比等于化学计量数之比;化学平衡的计算,一般如果是一个反应平衡,常采用“三段式”,如本题中化学平衡常数的计算,如果是两个是反应平衡,常采用等效方法,如本题的选项D,或化学平衡常数不变进行计算,如选项中的A或B、 C选项的判断等。
钇的常见化合价为+3价,我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇。

已知:①该流程中有关金属离子形成氢氧化物沉淀时的pH见下表:
离子
开始沉淀时的pH
完全沉淀时的pH
Fe3+
2.7
3.7
Y3+
6.0
8.2
②在元素周期表中,铍元素和铝元素处于第二周期和第三周期的对角线位置,化学性质相似。请回答下列问题:
(1)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。
①最好选用盐酸和__________两种试剂,再通过必要的操作即可实现。
A.NaOH溶液 B.氨水 C.CO2 D.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式__________。
(2)为使Fe3+沉淀完全,用氨水调节pH=a时,a应控制在__________范围内;继续加氨水调节pH=b发生反应的离子方程式为__________;检验Fe3+是否沉淀完全的操作方法是__________。
(3)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇煅烧的化学方程式__________。
知识点:化学
(1)B BeO22-+4H+=Be2++2H2O
(2)3.7~6.0 Y3++3NH3·H2O=Y(OH)3↓+3NH4+
取少量最后一次洗涤过滤液,滴加几滴KSCN溶液,观察溶液是否变为血红色,若溶液不呈血红色,则Fe3+沉淀完全。
(3)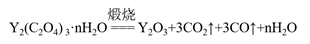
解析:(1)①因为Be和Al的性质相似,因此先加过量的盐酸,生成H2SiO3、BeCl2、NaCl,然后过滤,氢氧化铍溶于强碱,不溶于弱碱,因此加入氨水,故选项B正确;②氢氧化铝表现两性,因此Be(OH)2也表现两性,即有BeO22-+4H+=Be2++2H2O;(2)根据表格数据,以及实验目的,调节pH应是除去Fe3+,不影响Y3+,因此pH的范围控制在3.7~6.0;加入氨水,Y3+转化成沉淀,发生反应是Y3++3NH3·H2O=Y(OH)3↓+3NH4+,检验Fe3+常用KSCN溶液,溶液变为血红色,说明Fe3+存在,步骤是取少量最后一次洗涤过滤液,滴加几滴KSCN溶液,观察溶液是否变为血红色,若溶液不呈血红色,则Fe3+沉淀完全;(3)澄清石灰水变浑浊,说明产生CO2,Y的化合价无变化,C2O42-中C的化合价为+3价,有化合价的升高,就有化合价的降低,因此C的化合价转化成+2价,即CO,方程式为: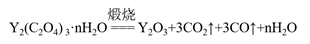 。
。
【点睛】本题考查化学工艺流程,涉及化学反应原理、物质的除杂和提纯、实验基本操作等知识,流程中充分利用题目所给信息,如本题中在元素周期表中,铍元素和铝元素处于第二周期和第三周期的对角线位置,化学性质相似;把握每个步骤的作用或反应,实验基本操作中叙述中注意化学用语的正确使用,如本题中沉淀如何证明沉淀已洗净:应说取最后一次洗涤液,加入什么,如果出现什么,证明什么,还有如何洗涤沉淀,应说沿玻璃棒向原过滤器中加入蒸馏水,没过沉淀,待水流完后,充分上述操作2-3次等。
青蒿素人工合成的部分反应流程如下:

已知羰基的α-H可以发生如下反应:

(1)化合物G中含有的官能团名称为:__________、__________,E→F的反应类型为__________。
(2)D→E先后由加成和消去两步反应完成,加成后得到的中间产物的结构简式为__________。
(3)B→C的方程式为__________。
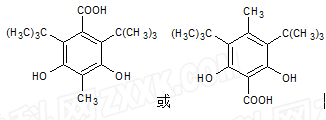
(4)写出符合下列要求的H的一种同分异构体的结构简式__________。
①既能与NaHCO3反应放出气体,也能使FeCl3溶液显紫色;
②分子中有四种不同环境的氢原子。
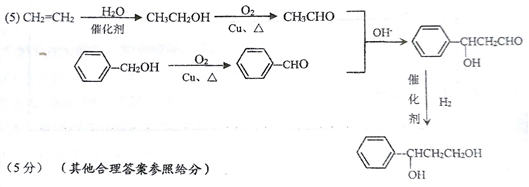
(5)利用题中所给信息,试以苯甲醇( )和乙烯为原料(其他无机试剂任选),合成
)和乙烯为原料(其他无机试剂任选),合成 。__________________________
。__________________________
知识点:化学
(1)醚键 碳碳双键 还原反应
(2)
(3)2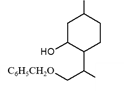 +O2
+O2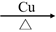 2
2 +2H2O
+2H2O
(4)
(5)
解析:(1)根据G的结构简式,含有的官能团是碳碳双键、醚键;对比E和F的结构简式 E中的碳碳双键转化成碳碳单键,因此E→F发生加成反应或还原反应;(2)根据信息,与羰基所连碳原子上的一个碳氢键发生断裂,另一个羰基碳氧双键中一个碳氧键打开,即产物是 ;(3)对比B、C结构简式,B→C发生醇的氧化,反应方程式为:2
;(3)对比B、C结构简式,B→C发生醇的氧化,反应方程式为:2 +O2
+O2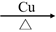 2
2 +2H2O;(4)①能与NaHCO3发生反应,生成CO2,说明含有羧基,能与FeCl3显色,说明含有酚羟基;②含有四种不同环境的氢原子,应是对称结构,因此H的结构简式为
+2H2O;(4)①能与NaHCO3发生反应,生成CO2,说明含有羧基,能与FeCl3显色,说明含有酚羟基;②含有四种不同环境的氢原子,应是对称结构,因此H的结构简式为 ;(5)根据信息,推出合成产物的原料是应是苯甲醛和乙醛,苯甲醛由苯甲醇氧化而成,乙醛可以由乙烯先和水加成为乙醇,乙醇催化氧化成乙醛,也可以由乙烯和氧气在一定条件下发生氧化反应生成乙醛,因此路线之一是
;(5)根据信息,推出合成产物的原料是应是苯甲醛和乙醛,苯甲醛由苯甲醇氧化而成,乙醛可以由乙烯先和水加成为乙醇,乙醇催化氧化成乙醛,也可以由乙烯和氧气在一定条件下发生氧化反应生成乙醛,因此路线之一是
 。
。
【点睛】本题考试有机物的合成和推断,主要考查官能团的性质,知道有机物中常见的官能团有哪些,同时注意苯环不是官能团,发生的反应类型的判断一看反应条件,如氢氧化钠的醇溶液,必然发生消去反应,二对比反应物和产物的结构简式,找出不同,不同的是断键和生成键,如本题中E→F,E中含有碳碳双键,F中不含碳碳双键,说明反应中碳碳双键断裂,发生加成反应或还原反应;有机物中的难点是同分异构体的书写和判断,往往限制条件的,通过条件判断出含有的官能团或取代基大概的位置,如本题中能和碳酸氢钠反应,有机物中只有羧基和碳酸氢钠反应生成CO2,说明含有羧基,能和FeCl3发生显色反应,说明含有酚羟基,因此作出合理的判断。
硫酸亚铁铵(俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。
(1)制备莫尔盐的流程如下:

①用热的Na2CO3溶液清洗废铁屑的目的是__________。
②其中最后一步用少量无水乙醇洗涤晶体目的是________。
(2)现取0.4gCu2S和CuS的混合物在酸性溶液中用40mL0.150mol·L-1KMnO4溶液处理,发生反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O,
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O,
反应后煮沸溶液,赶尽SO2,剩余的KMnO4用0.2mol·L-1(NH4)2Fe(SO4)2溶液来滴定,完全反应消耗(NH4)2Fe(SO4)2溶液VmL。已知:MnO4-+Fe2++H+→Mn2++Fe3++H2O(未配平)
①滴定终点的现象为________。
②若V=35,试计算混合物中CuS的质量分数________(写出计算过程)。
知识点:化学
(1)①除去废铁屑表面的油污 ②洗去晶体表面杂质,减少晶体损失
(2)①滴入最后一滴溶液时红色褪去,半分钟内不变红
②60%
解析:(1)①铁屑表面常有油污,这些油污阻碍铁屑和硫酸的接触,需要除去,碳酸钠的水溶液显碱性,油污在碱性中完全水解,因此碳酸钠的作用是除去铁屑表面的油污;②莫尔盐不溶于乙醇,用乙醇洗涤可以减少莫尔盐的溶解,同时乙醇易挥发;(2)①用(NH4)2Fe(SO4)2滴定高锰酸钾溶液,Fe2+能使酸性高锰酸钾溶液褪色,因此滴定到终点的现象是滴入最后一滴时紫红色褪去,且半分钟不变色;②V=35,与35mL(NH4)2Fe(SO4)2溶液完全反应需要高锰酸钾的物质的量为:
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
1mol 5mol
0.014mol 0.035L×0.2mol·L-1
所以高锰酸钾的物质的量为0.0014mol,
故与固体混合物反应的高锰酸钾的物质的量为:0.150mol·L-1×0.040L-0.0014mol = 0.0046mol
设Cu2S物质的量为x,CuS物质的量为y 根据得失电子数目守恒,2x×1+6x+6y=0.0046×5,根据题意得出160x+96y=0.40g
解得x=0.001mol,y=0.0025mol
则混合物中CuS的质量分数为0.0025mol×96g/0.4g×100%=60%
甲酸钙广泛用于食品、化工、石油等工业生产上,300~400℃左右分解。

Ⅰ、实验室制取的方法之一是:Ca(OH)2 +2HCHO + H2O2 = Ca(HCOO)2 + 2H2O + H2↑。实验室制取时,将工业用氢氧化钙和甲醛依次加入到质量分数为30-70%的过氧化氢溶液中(投料物质的量之比依次为1∶2∶1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品。
(1)过氧化氢比理论用量稍多,其目的是__________。
(2)反应温度最好控制在30-70℃之间,温度不易过高,其主要原因是__________。
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是__________。
(4)实验时需强力搅拌45min,其目的是__________;结束后需调节溶液的pH 7~8,其目的是__________。最后经结晶分离、干燥得产品。
Ⅱ、某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙。结合如图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算),现提供的试剂有:A.甲酸钠,B.5mol·L-1硝酸,c.5mol·L-1盐酸,d.5mol·L-1硫酸,e.3%H2O2溶液,f.澄清石灰水。
金属离子
开始沉淀的pH
沉淀完全的pH
Fe3+
1.1
3.2
Al3+
3.0
5.0
Fe2+
5.8
8.8
请补充完整由碳酸钙制备甲酸钙的实验步骤 :
步骤1.称取13.6g甲酸钠溶于约20mL水,配成溶待用,并称取研细的碳酸钙样品10g待用。
步骤2._________。
步骤3._________。
步骤4.过滤后,将滤液与甲酸钠溶液混合,调整溶液pH 7~8,充分搅拌,所得溶液经蒸发浓缩、__________、洗涤、60℃时干燥得甲酸钙晶体。
知识点:化学
Ⅰ.(1)使甲醛充分氧化,提高甲醛的利用率和产品纯度
(2)防止H2O2分解和甲醛挥发
(3)除去重金属离子(使重金属离子形成硫化物沉淀除去)
(4)使反应物充分接触,提高产率
防止甲酸钙水解(或除去甲酸)
Ⅱ.用稍过量硝酸溶解碳酸钙样品
用石灰水调节溶液pH为 5
趁热过滤
解析:I.(1)过氧化氢用量较多,为了使甲醛充分反应,提高甲醛的利用率;(2)温度不宜过高,因为过氧化氢受热易分解,且甲醛容易挥发,造成原料的浪费;(3)题干中指出得到重金属含量极低的优质产品,因此加入硫化钠的作用是让重金属阳离子转化成难溶的硫化物,除去重金属离子;(4)搅拌的目的使反应物充分接触,使其反应完全,提高产率;甲酸钙是强碱弱酸盐,HCOO-水解,因此调节pH的目的使抑制HCOO-的水解;II.步骤2得到可溶的含钙溶液,因为硫酸钙微溶于水,因此不能选用硫酸,硝酸钠溶解度受温度的影响较大,容易除去,因此碳酸钙中加入稍微过量硝酸溶解,即步骤2:用稍过量的硝酸溶解碳酸钙样品;碳酸钙中含有Al2O3和FeCO3杂质,因为步骤2中加入硝酸,硝酸把Fe2+氧化成Fe3+,因此步骤3是除去杂质离子Al3+和Fe3+,根据表格数据,调节pH除去Al3+和Fe3+,引入的物质的不能引入新的杂质,应加入含Ca的物质,根据所给药品,应加入石灰水,调节pH到5,步骤3:用石灰水调节溶液pH为5;甲酸钙的溶解度较低,因此采用蒸发浓缩,趁热过滤的方法得到。
I.锰是在地壳中广泛分布的元素之一,其单质和化合物在工农业生产中有着重要的作用。已知Al的燃烧热为ΔH=—ckJ·mol—1,金属锰可用铝热法制得。其余相关热化学方程式为:3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) ΔH1 = akJ·mol—1
3MnO2(s)=Mn3O4(s)+O2(g) ΔH2 = b kJ·mol—1
则3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) ΔH3 =__________kJ·mol—1(用含a、b、c的式子表示)
II.无机和有机氰化物在工农业生产中应用广泛,尤其是冶金工业常用氰化物,含氰废水的处理显得尤为重要。含氰废水中的氰化物常以3-和CN-的形式存在,工业上有多种废水处理方法。
(1)电解处理法:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为__________(填“阴极”或“阳极”),阳极产生ClO-的电极反应为__________,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为__________。

(2)UV(紫外光线的简称)—H2O2氧化法。
实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2,置于UV工艺装置中,光照一定时间后取样分析。
【查阅资料】
①在强碱性溶液中4[Fe(CN)6]3-+4OH—=4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更稳定;
②[Fe(CN)6]3-转化为CN-容易被H2O2除去;
③HCN是有毒的弱酸,易挥发。c
①废水中的CN一经以下反应实现转化:CN—+H2O2+H2O=A+NH3↑,则A是__________(用符号表示)。
②含氰废水在不同pH下的除氰效果如图所示,pH选择的最佳范围应为__________(a.7-10;b.10-11;c.11-13),解释该pH不宜太大的原因__________。

知识点:化学
I.ΔH=a/3+b — 4/3c kJ·mol-1
II.(1)阴极 Cl-+2OH--2e-=ClO-+H2O 5ClO—+2CN—+2OH—=2CO32—+N2↑+5Cl—+H2O
(2)①HCO3—
②b 碱性太强,溶液中4[Fe(CN)6]3-+4OH—===4[Fe(CN)6]4-+O2↑+2H2O生成[Fe(CN)6]4-后难以除去
解析:I.①3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) ,②3MnO2(s)=Mn3O4(s)+O2(g),③4Al(s)+3O2(g)=2Al2O3(s) △H=-4ckJ·mol-1,(①+3×②+③)/3,得出△H=(a+3b-4c)/3kJ·mol-1; II.(1)依据电解原理,金属作阳极,先失电子,题目中提供信息:阳极产生的是ClO-,因此铁作阴极,阳极是失电子,化合价升高,控制溶液的pH在9-10,说明溶液显碱性,阳极反应式为Cl-+2OH--2e-=ClO-+H2O,ClO-将CN-氧化成无害物质,即Cl转化成Cl-,环境是碱性环境,C转化成CO32-,N转化成N2,ClO-+CN-→CO2↑+N2↑+Cl-,然后根据化合价升降进行配平,5ClO-+2CN-→2CO32-+N2↑+5Cl-,利用电荷守恒和原子守恒,配平其他,写出缺少的微粒,因此离子反应方程式为:5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O;(2)①根据元素守恒、原子守恒、电荷守恒,A应带一个单位的负电荷,A中含有的一个C原子、一个H原子、3个氧原子,因此A为HCO3-,②根据不同pH对除氰效果的影响图,应选择除氰率最高的即pH在10~11,故选项b正确;根据查阅资料①,[Fe(CN)6]4-在碱性条件下更稳定,难以除去,具体回答是:碱性太强,溶液中4[Fe(CN)6]3-+4OH—===4[Fe(CN)6]4-+O2↑+2H2O生成[Fe(CN)6]4-后难以除去。
【点睛】考查化学反应原理的应用,学生主要在电极反应式的书写、氧化还原反应方程式的书写、化学平衡的计算上失分,电极反应式的书写应注意先写出化合价变化的微粒和产物,像本题写出Cl-→ClO-,然后根据化合价变化写出得失电子的物质的量,即Cl--2e-→ClO-,根据环境判断出缺少的微粒,本题的环境是碱性,应是OH-、H2O参与反应和生成,然后前后所带电荷守恒,写出反应式:Cl-+2OH--2e-=ClO-+H2O;氧化还原反应方程式的书写类似电极反应式的书写,只要平时多加练习,这部分内容应是不难的。
在5-氨基四唑( )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
(1)基态Ga原子的电子排布式可表示为__________;
(2)5-氨基四唑中所含元素的电负性由大到小的顺序为__________;在1mol 5-氨基四唑中含有的σ键的数目为__________.
(3)叠氮酸钠(NaN3)是传统家用汽车安全气囊中使用的气体发生剂.
①叠氮酸钠(NaN3)中含有叠氮酸根离子(N3-),根据等电子体原理N3-的空间构型为__________.

②以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化 钛化合物.其结构是用碳原子取代氮化钛晶胞(结构如图示)顶点的氮原子,这种碳氮化钛化合物的化学式为__________.
③2+中的化学键有__________.
a.σ键 b.π键 c.离子键 d.配位键.
知识点:化学
(1)1s22s22p63s23p63d104s24p1或 3d104s24p1
(2)N>C>H 9NA
(3)①直线形 ②Ti4CN3 ③ad
解析:(1)Ga属于31号元素,第四周期第IIIA族元素,电子排布式为:1s22s22p63s23p63d104s24p1或 3d104s24p1;(2)电负性越大,非金属性越强,同周期从左向右电负性增大,因此电负性的顺序是N>C>H,成键原子之间只能形成一个σ键,因此1mol该物质中含有σ键数目是9NA;(3)①N3-与CO2互为等电子体,CO2为直线形,因此N3-的空间构型为直线形;②Ti位于棱上和体心,Ti的个数为12×1/4+1=4,C位于顶点,个数为8×1/8=1,N位于面心,个数为6×1/2=3,因此化学式为Ti4CN3;③Ti4+与OH-、H2O之间存在配位键,OH-、H2O中存在共价键,或σ键故选项ad正确。