人类正面临着石油短缺、油价上涨的困惑。以下解决能源问题的方法不当的是( )
A.用木材作燃料 B.用液氢代替汽油 C.开发风能 D.开发地热能
知识点:化学反应的热效应
A
略
下列说法正确的是
A、需要加热才能发生的反应一定是吸热反应 B、化学反应中的能量变化都表现为热量变化
C、任何放热反应在常温下一定能发生反应
D、反应物和生成物所具有的总能量决定了反应是放热还是吸热
知识点:化学反应与能量的变化
D
略
下列反应中属于吸热反应的是( )
A.CaO+H2O===Ca(OH)2 B.C+H2OCO+H2
C.HCl+NaOH===NaCl+H2O D.2Al+3H2SO4===Al2(SO4)3+3H2↑
知识点:化学反应与能量的变化
C
略
在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+O2(g)===CO2 (g)+2H2O(l) ΔH=+725.8 kJ/mol
B.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1 452 kJ/mol
C.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-725.8 kJ/mol
D.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=+1 452 kJ/mol
知识点:化学反应的热效应
B
略
已知下列热化学方程式:
Zn(s)+O2(g)===ZnO(s) ΔH1=-351.1 kJ/mol
Hg(l)+O2(g)===HgO(s) ΔH2=-90.7 kJ/mol
由此可知反应Zn(s)+HgO(s)===ZnO(s)+Hg(l)的ΔH3的值是( )
A.-441.8 kJ/mol B.-254.6 kJ/mol C.-438.9 kJ/mol D.-260.4 kJ/mol
知识点:化学反应的热效应
D
略
已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1 mol氢气的化学键消耗的能量为Q1 kJ,破坏1 mol氯气的化学键消耗的能量为Q2kJ ,破坏1 mol氯化氢中的化学键消耗的能量为Q3kJ,下列关系式正确的是
A、Q1 + Q2 > Q3 B、Q1 + Q2 > 2Q3 C、Q1 + Q2 < Q3 D、Q1+ Q2 < 2Q3
知识点:化学反应的热效应
D
略
已知反应:①101 kPa时,2C(s)+O2(g)===2CO(g) ΔH=-221 kJ/mol;
②稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol。
下列结论正确的是( )
A.碳的标准燃烧热,ΔH =-110.5 kJ/mol B.①的反应热为221 kJ/mol
C.0.5mol稀硫酸与1mol稀NaOH溶液反应放出的热量为57.3 kJ
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
知识点:化学反应的热效应
C
略
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热
ΔH=2×(-57.3) kJ/mol
B.CO(g)的标准燃烧热,ΔH =-283.0 kJ/mol
则2CO2(g)===2CO(g)+O2(g)反应的ΔH=2×283.0 kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
知识点:化学反应的热效应
B
略
已知H2(g)+Cl2(g)===2HCl(g) ΔH=-184.6 kJ·mol-1,则反应HCl(g)===H2(g)+Cl2(g)的ΔH为( )
A.+184.6 kJ·mol-1 B.-92.3 kJ·mol-1 C.-369.2 kJ·mol-1 D.+92.3 kJ·mol-1
知识点:化学反应的热效应
D
略
已知:2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1
H2(g)+O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
由此可知,在等温下蒸发45 g液态水需吸收的热量( )
A.483.6 kJ B.110 kJ C.285.8 kJ D.221 kJ
知识点:化学反应的热效应
B
略
已知25 ℃ 101 kPa条件下:(1)4Al(s)+3O2(g)===2Al2O3(s)ΔH=-2 834.9 kJ·mol-1
(2)4Al(s)+2O3(g)===2Al2O3(s)ΔH=-3 119.1 kJ·mol-1 由此得出的正确结论是
A.等质量的O2比O3能量低,由O2变O3为吸热反应
B.等质量的O2比O3能量低,由O2变O3为放热反应
C.O3比O2稳定,由O2变O3为吸热反应 D.O2比O3稳定,由O2变O3为放热反应
知识点:化学反应的热效应
A
略
废电池必须进行集中处理的问题被提到议事日程。其首要原因是( )
A.利用电池外壳的金属材料 B.防止汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品 D.回收其中石墨电极
知识点:原电池
B
略
下列说法正确的是( )
A.碱性锌锰电池是二次电池 B.铅蓄电池是一次电池
C.蓄电池是二次电池,它放电后可以再充电使活性物质获得再生
D.氢气、甲烷等燃料在燃料电池的内部进行燃烧,从而将化学能转化为电能
知识点:原电池
C
略
下列几种金属制品的镀层损坏后,金属腐蚀的速率最快的是( )
A.镀铝铁桶 B.食品铁罐头盒(镀锡) C.白铁水桶(镀锌) D.镀银铜质奖章
知识点:金属的电化学腐蚀与防护
B
略
为了避免青铜器生成铜绿,以下方法正确的是 ( )
A.将青铜器放在银质托盘上 B.将青铜器与直流电源的正极相连
C.将青铜器保存在潮湿的空气中 D.在青铜器的表面覆盖一层防渗的高分子膜
知识点:金属的电化学腐蚀与防护
D
略
在钢铁腐蚀过程中,下列五种变化可能发生的是( )
①Fe2+转化为Fe3+②O2被还原③产生H2 ④Fe(OH)3失水形成Fe2O3·H2O⑤杂质碳被氧化
A.只①② B.只②③④ C.①②③④ D.①②③④⑤
知识点:金属的电化学腐蚀与防护
C
略
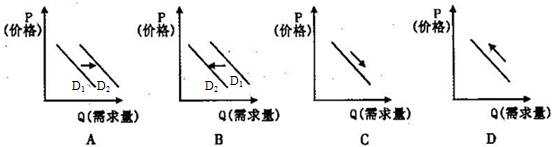
等质量的两份锌粉a、b分别加入到两份质量相同的过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,下列各图为产生H2的体积V(L)与时间t(min)的关系,其中正确的是

知识点:原电池
A
略
蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。关于标有“+”的接线柱,下列说法中正确的是
A.充电时作阳极,放电时作负极 B.充电时作阳极,放电时作正极
C.充电时作阴极,放电时作负极 D.充电时作阴极,放电时作正极
知识点:电解池
B
略
如下图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在记录卡片上写下了一些记录:

在卡片上,描述合理的是
A.①②③ B.③④⑤ C.④⑤⑥ D.②③④
知识点:原电池
B
略
一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳,该电池负极发生的反应是
A.CH3OH(g)+O2(g)===H2O(l)+CO2(g)+2H+(aq)+2e- B.O2(g)+4H+(aq)+4e-===2H2O(l)
C.CH3OH(g)+H2O(l)===CO2(g)+6H+(aq)+6e- D.O2(g)+2H2O(l)+4e-===4OH-
知识点:原电池
C
略
下列叙述正确的是
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
知识点:电解池
C
略
在pH=a的某电解质溶液中,插入两支惰性电极,通直流电一段时间后,溶
液的pH>a,则该电解质可能是( )
A.NaOH B.H2SO4 C.AgNO3 D.Na2SO4
知识点:电解池
A
略
当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是
A.当电池负极消耗mg气体时,电解池阳极同时有mg气体生成
B.电池的正极反应式为:O2十4H+十4e-==2H2O
C.电解后c(Na2CO3)不变,且溶液中有晶体析出
D.电池中c(KOH)不变;电解池中溶液pH变大
知识点:电解池
C
略