(6分)配平方程式
(1) CrCl3+ KMnO4+ H2O= K2Cr2O7+ MnCl2+ HCl+ MnCr2O7
(2) As2S2+ HNO3+ H2O= H3AsO4+ NO↑+ H2SO4
知识点:氧化还原反应
(1)10、6、11,3、4、22、2
(2)3、28、4,6、28、9
略
(12分)(1)实验证明,硫化铜与硫酸铁在细菌作用下,在潮湿多雨的夏季,成为硫酸和硫酸盐而溶解于水,这就是废石堆渗沥水,矿坑水成为重金属酸性废水的主要原因,试写出配平的化学方程式。
(2)从金矿中提取金,传统的也是效率极高的方法是氰化法。氰化法提金是在氧存在下氰化物盐类可以溶解金。试写出配平的化学方程式。
(3)对二乙苯在酸性高锰酸钾溶液中被氧化并有气体产生,试写出配平的反应式。
知识点:芳香烃 石油 苯 煤
(1)CuS+4Fe2(SO4)3+4H2O![]() CuSO4+8FeSO4+4H2SO4
CuSO4+8FeSO4+4H2SO4
(2)4Au+8NaCN+2H2O+O2=4NaAu(CN)2+4NaOH
(3)5CH3CH2-![]() -CH2CH3+24KMnO4+36H2SO4
-CH2CH3+24KMnO4+36H2SO4![]() 5HOOC-
5HOOC-![]() -COOH+12K2SO4+24MnSO4+10CO2+10CO2↑56H2O
-COOH+12K2SO4+24MnSO4+10CO2+10CO2↑56H2O
略
(12分)(1)用石灰乳跟硫熬煮而成的石硫合剂含多硫化钙(CaSn)。多硫化钙在空气中与二氧化碳等酸性物质接触易析出多硫化氢,多硫化氢是一种极不稳定的黄色液体,试用化学方程式说明多硫化钙具有杀虫作用的原因。
(2)在强碱B-:(如NH4+NH2-),的存在下CH3CH2CH2CH2Cl可按下列两种历程发生消除反应,分别称之为Eα消除和E2消除:
Eα: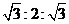
E2: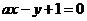
试构思一个实验证实上述历程。
知识点:有机合成及高分子化合物
(1)CaSn+H2O0+CO2=CaCO3十H2Sn
H2Sn=H2S+(n-1)S
生成的硫具有杀虫作用
(2)采用同位素标记法:
解法一;在α位上引入两个D原子即CH3CH2CH2CD2Cl
脱HCl后可分离出两种产物:
CH3CH2CH=CHD这是Eα反应的产物
CH2CH2CH=CD2这是E2反应的产物
解法二,在β位上引入2个D原子,即CH3CH2CD2CH2Cl
脱HC后可分离出两种产物:
CH3CH2CD=CHD这是Eα反应的产物
CH3CH2CD=CH2这是E2反应的产物
略
(12分)(1)实验室中所用的氧化钢(CuO)是黑色粉末。在使用电烙铁时,其头部是一铜制的烙铁头,长期使用,表面被氧化,但脱落下来的氧化膜却是红色的,试说明原因。
(2)法医鉴定砷中毒(通常为砒霜)的方法是用锌、盐酸和试样混在一起,将生成的气体导入热玻璃管,如果试样中有砷化物存在,则在玻璃管的壁上出现亮黑色的“砷镜”。试写出有关的反应式。
(3)把CO2气体通入澄清的石灰水,立即会产生浑浊,但把SO2气体通入澄清的石灰水,却不容易看那浑浊,而CaCO3和CaSO3都是难溶的电解质,试说明原因。
知识点:基本概念、基本理论的综合运用
(1)答因为Cu2O比CuO稳定;在加热条件下总是生成红色的Cu2O
(2)As2O3+6Zn+12HCl=2AsH3+6ZnCl2+3H2O
2AsH3![]() 2As+3H2↑
2As+3H2↑
(3)因为SO2在水中的溶解度比CO2大得多,而且H2SO4的酸性比H2CO3强得多,所以通SO2于澄清的石灰水中极易过量,过量后生成Ca(HSO4)2而溶解。
略
(6分)分子式为C7H10的开经烃A,可发生下列反应:
(1)A经催化加氢可生成3一乙基戊烷。
(2)A与硝酸银氨溶液反应可产生白色沉淀。
(3)A在Pd/BaSO4催化作用下吸收1摩尔氢生成化合物B,B可以生成橡胶状的物质C。
请写出A、B、C的结构简式。
知识点:有机分子式的确定
A:![]() B:
B:![]()
C: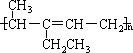
略
(10分)试写出分子式为C4H10Cl的所有异构体的结构简式。
知识点:卤代烃
①
![]() ②
② ![]() ③
③ ![]()
④ ![]() ⑤
⑤ ![]() ⑥
⑥ ![]()
⑦ ![]() ⑧
⑧ ![]() ⑨
⑨ ![]() ⑩ ClCH2CH2CH=CH2
⑩ ClCH2CH2CH=CH2
11 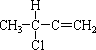 12
12 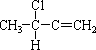 13
13 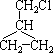 14
14 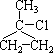
15 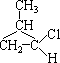 16
16 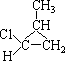 17
17 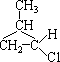 18
18 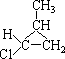
略
(12分)已知某元素A能与ⅦA族某一元素B生成A本身的最高价化合物,在此化合物中B的含量为92.2%,而在与此相应的氧化物中,氧的含量为72.7%。A与B生成的化合物为一无色透明液体,沸点77℃,对空气的相对密度为5.3。回答下列问题:
(1)A元素名称,并指出属于第几周期第几族;
(2)A元素与B元素形成的化合物的分子式,A元素相应的氧化物教分子式;
(3)列举A与B形成的化合物的两种用途用途。
知识点:元素周期律与元素周期表
(1)A元素是C,位于第二周期第Ⅳ族
(2)CCl4和CO2
(3)可用作灭火剂和有机溶剂
略
(12分)测定分子量的常用方法之一是凝固点下降法。例如水是常用的溶剂,当水中溶解了某种不挥发的溶质时,水的凝固点(即冰点)即会下降,海水在0℃时不会结冰就是这个原因。凝固点下降的程度与溶质的分子数有关,而与溶质是何种物质无关。当溶剂的量确定时,凝固点的降低值与溶质的分子数成正比。已知10.0g樟脑中溶解0.412g萘,凝固点下降了13℃。某种由C、H、O组成的有机物2.30g溶于15.6 g樟脑中,凝固点下降了49.5℃。如果把3.667g该有机物完全燃烧,生成 9.236g CO2和1.634g H2O,求该物质的分子式(已知萘的相对分子质量为:128,相对原子质量:H 1 C 12 O 16)
知识点:化学式的计算
C7H6O2
略