制取下列物质的方案能够达到目的的是
A 用生锈的废钢铁与稀硫酸反应制绿矾
B 用碳酸钠与稀H2SO4反应制CO2
C 用食盐、二氧化锰和稀H2SO4共热制Cl2
D 用铁与稀盐酸反应制氯化铁
知识点:综合性实验
AB
略
两种盐的混和物,加热或遇水均能放出使澄清石灰水变浑浊的气体,这两种盐不可能的是
A NaHSO4和Na2CO3 B Al2(SO4)3和NaHCO3
C NaHSO4和KHCO3 D MgSO4和Na2CO3
知识点:镁铝及其化合物
D
略
A、B是短周期元素,最外层电子排布式分别为msx,nsxnpx+1。A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石德试纸变蓝,则该化合物的分子量是
A 38 B 55 C 100 D 135
知识点:原子结构与性质
C
略
已知,常温下CH3COOH的电高平衡常数为1.76×10-5,常温下将pH=3的 CH3COOH溶液用水稀释一后,溶液的pH值为
A 3 B 3.15 C 3.3 D 2.7
知识点:弱电解质的电离
B
略
某无色溶液中加入过县盐酸有沉淀产生,过滤后向油液中加入过量纯碱溶液又有沉淀产生,下列溶液中符合此条件的是
① Ag+、Fe3+、Na+ ② Ag+、Al3+、K+ ③ Ag+、Ba2+
④ SiO32-、AlO2-、K+ ⑤ Ag+、NH4+、H+ ⑥ SiO32-、K+、Al3+
A 各组均符合 B ②③④⑥ C ②③④ D ①②③④⑥
知识点:离子共存
C
略
某元素x的原子量为a,它的最高价氧化物的水化物的分子式为HmXOn(m>1),下列有关叙述正确的是
A 该酸的水溶液中,[H+]︰[XOnm-]=m︰1
B 该酸的摩尔质量为(m+a+16n)克
C 100毫升该酸溶液只能中和4克NaOH
D 若0.1摩/升该酸溶液的pH=1,则NamXOn的水溶液的pH值>7
知识点:盐类水解
D
略
常温时,下列三个反应都能自发的向右进行:
2W-+X2=2X-+W2
2Y-+W2=2W-+Y2
2X-+Z2=2X-+Z2
由此得出的正确结论是
A X-、Y-、Z-、W-中,Z-还原性最强
B X2、Y2、Z2、W2中,Z2的氧化性最弱
C 2Z-+Y2=2Y-+Z2不能自发向右进行
D 还原性X->Y-
知识点:氧化还原反应
C
略
某密闭容器中放入一定量的NO2,发生反应2NO2![]() N2O4+Q,达平衡后,若分别单独改变下列条件,重新达到平衡后,能使混和气体平均分子量增大的是
N2O4+Q,达平衡后,若分别单独改变下列条件,重新达到平衡后,能使混和气体平均分子量增大的是
A 通入N2 B 通入 NO2 C 通入N2O4 D 升高温度
知识点:化学平衡状态及移动
BC
略
甲酰胺的氮原子上两个氢原子都被甲基取代后所得到的产物称为N,N-二甲基甲酰胺,简称为DMF,是现在常用的溶剂。下列四种化合物的分子量,只有一个跟其它3个不同,它是
A DMF B 丙酸 C 乙醛酸 D 乙醚
知识点:蛋白质和核酸
A
略
有一瓶无色气体可能含H2S、CO2、HBr、HCl、SO2中的一种或几种,将此气体通入稀氯水中,恰好完全反应,得无色透明溶液。把此溶液分成两份,分别加入盐酸酸化的BaCl2溶液和硝酸酸化的AgNO3溶液,均出现白色沉淀。对此结论:①原气体中肯定有SO2;②原气体中可能有SO2;③原气体中肯定没有HBr和H2S;④不能确定原气体中有无HCl;⑤原气体中肯定没有CO调原气体中肯定有HCl,正确的是
A ①③④ B ①④⑤ C ①③④⑥ D ①③⑤⑥
知识点:物质的检验和鉴别
A
略
已知蓄电池在放电时起原电池的作用,充电时起电解他的作用。铅蓄电池在放电和充电时发生的化学反应可用下式表示:
Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O
2PbSO4+2H2O
据此判断下列叙述中正确的是
A 放电时铅蓄电池负极的电极反应为:PbO2+4H++SO42-十2e=PbSO4+2H2O
B 充电时铅蓄电池阴极的电极反应为;PbSO4+2e=Pb2++SO42-
C 用铅蓄电池来电解CuSO4溶液,要生成1.6克Cu,电池内部要消耗0.05摩H2SO4
D 铅蓄电池充电时,若要使3.03千克PbSO4转变为Pb和PbO2,需通过20摩电子
知识点:电解池
BC
略
在等物质的量的短周期金属单质A和B中,分别加入足量的酸,在A中加盐酸,在B中加稀硫酸。反应完全后,生成的氢气体积分别为VA和VB。,而且VA≠VB。若要确定反应生成物中A和B的化合价,你还可以要求下列选项中任何一个数据,它们是
A VA︰VB的值 B VA或者VB的值
C 所耗两种酸的物质的量之比 D 两种酸的摩尔浓度之比
知识点:元素周期律与元素周期表
AC
略
A、B、C、D、E均为氯的含氧化合物,我们不了解它们的分子式(或化学式),但知道它们在一定条件下具有如下的转换关系(未配平):
① B+H2O![]() C+H2O
② A→B+NaCl
C+H2O
② A→B+NaCl
③ E+NaOH→B+C+H2O ④ D+NaOH→A+B+H2O
这五种化合物中氯的化合价由高到低的顺序为
A C、B、E、D、A B B、D、A、C、E
C C、D、E、A、B D C、E、B、D、A
知识点:氧化还原反应
D
略
粗食盐中除含有钙、镁、硫酸根等可溶性杂质外,还含有泥砂等不溶性杂质。
实验室中粗食盐提纯的操作如下:
(1)在台称上称取租食盐15克,研细,放入小烧杯中,加40毫升蒸馏水,用电炉加热并搅拌,使其溶解。然后往热溶液中加入3~4毫升25%的BaCl2溶液。小心用电炉保温10分钟,使BaSO4沉淀完全。
请问:如何运用最简方法检验溶液中已无SO42-离子?
操作时需保温的原因是
(2)在上述溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的是
(3)将经过操作(2)后的溶液趁热进行减压过滤。请问这一操作能除掉哪些杂质?
(4)用纯净氯化氢通入操作(3)所得滤液中,直至不再析出NaCl晶体为止。通氯化氢气体的作用是
(5)用减压过滤方法将产品(NaCl晶体)抽干,并将产品移入蒸发皿,在通风橱中炒干。请问烘炒的原因是
知识点:物质的分离、除杂和提纯
(1)静止片刻在上层清液处,滴加一滴BaCl2溶液,不出现浑浊就说明SO42-已经除尽。
避免形成BaSO4胶体,加速BaSO4沉降。
(2)除去Ca2+、Mg2+以及加入过量Ba2+
(3)BaSO4、CaCO3、MgCO3、BaCO3以及泥砂等不溶性杂质
(4)除去溶液中的CO32-,同离子效应使NaCl结晶析出
(5)去掉吸附在晶体表面的HCl
略
SnCl2极易水解,生成白色沉淀Sn(OH)Cl后难以溶解,所以,配制SnCl2溶液时应防止它的水解,并防止它氧化为SnCl2。
那么,怎样配制100mL 0.1000mol·L-1的SnCl2溶液呢?
知识点:盐类水解
称取1.896gSnCl2固体,溶于约30mL浓HCl中,然后用少量水洗三次,并全部转移入100mL容量瓶中,配成100mL溶液,然后加入少量Sn粒以防止它氧化。
略
在硫酸铬溶液中,逐滴加入氢氧化钠溶液,开始生成灰兰色沉淀,继续加碱,沉淀又溶解,再向所得溶液中加溴水,直到溶液的绿色转为黄色。写出各步的化学方程式。
知识点:水的电离和溶液的酸碱性
Cr2(SO4)2+6NaOH=Cr(OH)3+3Na2SO4
Cr(OH)3+NaOH=NaCr(OH)4
2NaCr(OH)4+3Br2+8NaOH=2Na2Cr2O4+6NaBr+8H2O
略
氯酸是一种强酸,其浓度若超过40%就会迅速分解,产生一种比它酸性更强的酸,同时放出两种气体的混合气体,该气体干燥后的平均分子量为45.57,它可以使湿润的淀粉——KI试纸变兰后又褪色。试写出
(1)氯酸分解的方程式
(2)气体与淀粉——KI试纸反应方程式。
知识点:糖类
26HClO3=15O2+8Cl2+10HClO4+8H2O
Cl2+2KI=2KCl+I2 I2+5Cl2+6H2O=2HIO3+10HCl
略
将14.7克镁、铝合金全部溶于500毫升 6摩/升的盐酸中,充分反应后,再加入400毫升 8摩/升的NaOH溶液,结果得到26.3克沉淀,求合金中各组分的质量。
知识点:镁铝及其化合物
①若Al(OH)3全部溶解:nMg=0.453mol nAl=0.141mol
②若Al(OH)3部分溶解:nMg=0.050mol nAl=0.500mol
略
两个有机化合物A和 A’,互为同分异构体,其元素分析都含溴58.4%(其它元素数据不全,下同)。A、A’在浓KOH(或NaOH)的乙醇溶液中强热都得到气态化合物B,B含碳85.7%。B跟浓HBr作用得到化合物A’。
将A、A’分别跟稀NaOH溶液微微加热,A得到C;A’得到C’。C可以被KMnO4酸性溶液氧化得到酸性化合物D,D中含碳氢共63.6%;而在同样条件下C’却不被氧化。
1.试写出A、A’、B、C、C’、D的结构简式,并据此画一框图,表示它们之间的联系,但是不必写反应条件。
2.试写出C→D的氧化反应的离子方程式。
知识点:羧酸和酯
(1) 
(2)5(CH3)2CHCH2OH+4MnO4-+12H+→5(CH3)2CHCOOH+4Mn2++11H2O
略
有机分子的构造式中,四价的碳原子以一个、二个、三个或四个单键分别连接一个、二个、三个或四个其它碳原子时,被分别称为伯、仲、叔或季碳原子(也可以分别称为第一、第二、第三或第四碳原子),例如化合物A中有5个伯碳原子,仲、叔、季碳原子各1个。
[A]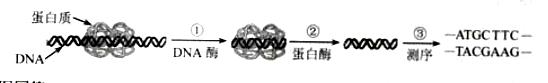
请回答以下问题:
(1)化合物A是汽油燃烧品质抗震性能的参照物,它的学名是 。它的沸点比正辛烷的 (填写下列选项的字母)A 高;B 低;C 相等;D 不能肯定。
(2)用6个叔碳原子和6个伯碳原子(其余为氢原子)建造饱和烃的构造式可能的形式有种 (不考虑顺反异构和光学异构)。请尽列之。
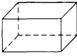
(3)只用8个叔碳原子(其余的为氢原子)建造一个不含烯、炔健的烃的结构式。
知识点:烷烃
(1)2,2,4—三甲基戊烷;B;
(2)8种: 
(3)
略
两个体积相等的玻璃球,中间用细管连通(其体积不计),开始时两球温度均为300K,共含0.7mol H2,其压强为0.5×P0(P0为标准压力,其值为101.325KPa,1Kp=103Pa)
若将(甲)球放入400K油浴中,而(乙)球仍为300K。求两球内的压强和H2的物质的量。
知识点:物质的量的计算
0.572P0 甲球0.3nol 乙球0.4mol
略