通过复习总结,你认为下列化学知识合理的是( )
A、所有的有机物都可以燃烧
B、一定条件下,甲烷、苯、乙酸、乙醇、油脂、淀粉都可以发生取代反应
C、糖类、油脂、蛋白质都属于高分子化合物
D、石油的分馏、裂化、裂解和煤的干馏都属于化学变化
知识点:蛋白质和核酸
B
略
下列事实与电化学腐蚀无关的是( )
A、钢铁制品生锈后用盐酸处理
B、黄铜(Cu、Zn合金)制的铜锣不易产生铜绿
C、铜、铝电线一般不连接起来作导线
D、生铁比熟铁(几乎是纯铁)容易生绣
知识点:金属的电化学腐蚀与防护
A
略
有8种物质,①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯;⑧环已烯。其中既不能使KMnO4酸性溶液褪色,也不能与溴水反应使溴水褪色的是( )
A、①②③⑤ B、④⑥⑦⑧ C、①④⑥⑦ D、②③⑤⑧
知识点:有机合成及高分子化合物
C
略
关于A(g) + 2B(g) == 3C(g)的化学反应,下列表示的反应速率最大的是( )
A、v(A) = 0.6 mol/(L·min) B、v(B) = 1.2 mol/(L·min)
C、v(C) = 1.2 mol/(L·min) D、v(B) = 0.03 mol/(L·s)
知识点:化学反应速率
D
略
下列说法正确的是( )
A、可逆反应的特征是正反应速率总是和逆反应速率相等
B、在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态
C、在其他条件不变时,升高温度可以使化学平衡向放热反应的方向移动
D、在其他条件不变时,增大压强一定会破坏气体反应的平衡状态
知识点:化学平衡状态及移动
B
略
用标准盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验误差的是( )
A、用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定
B、用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定
C、用碱式滴定管取10.00 mL NaOH溶液放入用蒸馏水洗净的锥形瓶中,加入少量的蒸馏水再进行滴定
D、用酚酞作指示剂滴至红色刚变无色时即停止加盐酸
知识点:水的电离和溶液的酸碱性
C
略
下列事实可以证明一水合氨是弱电解质的是( )
① 0.1 mol/L的氨水可以使酚酞试液变红
② 0.1 mol/L的氯化铵溶液的pH约为5
③ 在相同条件下,氨水溶液的导电性比强碱溶液弱
④ 铵盐受热易分解
A、①② B、②③ C、③④ D、②④
知识点:弱电解质的电离
B
略
常温下下列各组离子在指定溶液中能大量共存的是( )
A、PH =
1的溶液中:Fe2+、NO![]() 、SO
、SO![]() 、Na+
、Na+
B、由水电离出的c(H+) = 1×10—14
mol/L的溶液中:Ca2+、Cl—、HCO![]() 、K+
、K+
C、c(H+)/c(
OH— ) = 1×1012的溶液中:NH4+、Cl—、NO![]() 、Al3+
、Al3+
D、c(Fe3+)
= 0.1 mol/L的溶液中:K+、ClO—、SO![]() 、SCN—
、SCN—
知识点:离子共存
C
略
在密闭容器中发生下列反应aA(g) ![]() A、A的转化率变大
B、平衡向正反应方向移动
A、A的转化率变大
B、平衡向正反应方向移动
C、D的体积分数变大 D、a < c + d
知识点:化学平衡状态及移动
D
略
下列说法正确的是( )
A、在一定温度下AgCl水溶液中Ag+ 和Cl—浓度的乘积是一个常数
B、AgCl水溶液的导电性很弱,所以AgCl为弱电解质
C、温度一定时,当AgCl水溶液中Ag+ 和Cl—浓度的乘积等于KSP值时,此溶液为AgCl的饱和溶液
D、向饱和AgCl水溶液中加入盐酸,c(Cl—)增大,KSP值变大
知识点:溶解平衡
C
略
今有室温下四种溶液,有关叙述不正确的是( )
①
②
③
④
pH
11
11
3
3
溶液
氨水
氢氧化钠溶液
醋酸
盐酸
A、分别加水稀释10倍,四种溶液的PH①>②>④>③
B、①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
C、①、④两溶液等体积混合,所得溶液中c(Cl—)>c(NH4+)>c(OH—)>c(H+)
D、Va L④与VbL②溶液混合后,若混合后溶液PH = 4,则Va : Vb = 11 : 9
知识点:水的电离和溶液的酸碱性
C
略
下列有机物有四种同分异构体的是( )
A、分子式为C4H10的二氯取代物
B、分子式为C4H8O2的有机物
C、乙苯的一氯取代物
D、分子式为C3H9N的有机物,其中N原子以三个单键与其他原子相连
知识点:有机化合物的分类、命名与结构特点
D
略
(13分)在某一容积为2 L的密闭容器内,加入0.8 mol的H2和0.6 mol的I2,在一定条件下发生如下反应:
H2(g) + I2(g)
![]() 2HI(g)
△H = Q(Q<0)
2HI(g)
△H = Q(Q<0)
反应中各物质的浓度随时间变化情况如图1
(1)根据图1数据,反应开始至达到平衡时,平均速度v(HI)为 。
(2)反应达到平衡后,第8分钟时:
① 该反应的平衡常数表达式:K = ;若升高温度,化学平衡常数K (填“增大”、“减小”或“不变”),HI浓度的变化正确的是 (用图2中a ~ c的编号回答)。
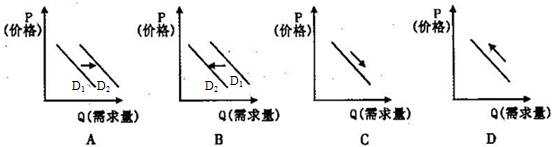
② 若加入I2,H2浓度的变化正确的是 (用图2
中d ~ f的编号回答)。
(3)反应达到平衡后,第8分钟时,若把容器的容积扩大一倍, 请在图3中画出8分钟后HI浓度的变化情况。
知识点:化学平衡状态及移动
(1)0.167 mol·L—1·min—1
(2)①![]() 减小
c ② f
减小
c ② f
(3)

略
(15分)(1)氯化铝水溶液呈 性,原因是(用离子方程式表示):
。把AICI3溶液蒸干,灼烧,最后得到的主要固体产物是 ,Al2(SO4)3溶液蒸干最后得到的固体产物是 ;
(2)NaHCO3的水溶液呈 (填“酸”、“中”或“碱”)性,实验室保存NaHCO3溶液的试剂瓶应用 塞,原因是 (写出有关的离子方程式);
(3)普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是 。
(4)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) ;④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号) 。
知识点:盐类水解
(1)酸
Al3+ + 3H2O![]() Al(OH)3+ 3H+
Al2O3 Al2(SO4)3
Al(OH)3+ 3H+
Al2O3 Al2(SO4)3
(2)碱
橡皮 HCO![]() + H2O
+ H2O ![]() H2CO3
+ OH— 2OH—
+SiO2 = SiO2
H2CO3
+ OH— 2OH—
+SiO2 = SiO2![]() + H2O
+ H2O
(3)3HCO![]() + Al3+ =
Al(OH)3↓+ 3CO2↑
+ Al3+ =
Al(OH)3↓+ 3CO2↑
(4)④、②、③、① ⑥、⑦、④、⑤、⑧
略
(6分)某有机物含有C、H、O、N四中元素,如图为该有机物的球棍模型。

(1)该有机物结构简式 ;
(2)该有机物可能发生的化学反应有(填编号) ;①水解 ②加聚 ③取代 ④消去 ⑤酯化
(3)该有机物发生水解反应的化学方程式为 。
知识点:蛋白质和核酸
(1)C5H11NO2 CH3CH2CONHCH2CH2OH
(2)① 、③、④、⑤、
(3)CH3CH2CONHCH2CH2OH + H2O → CH3CH2COOH + H2NCH2CH2OH
略
(10分)乳酸分子式为C3H6O3,在一定的条件下可发生许多化学反应,下图是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。
请回答相关问题:

(1)C的结构简式为 ;反应②的反应类型是 。
(2)E中所含的官能团有 。
(3)反应①的化学方程式为 。
(4)作为隐形眼镜的制作材料,对其性能的要求除应具有良好的光学性能外,还应具有良好的透气性和亲水性。一般采用E的聚合物G而不是D的聚合物H来制作隐形眼镜,其主要理由是 。
知识点:有机合成及高分子化合物
(1)CH2 = CHCOOCH3 消去反应
(2)碳碳双键、羟基、酯基
(3)nCH2—CH—COOH![]()
|
OH
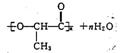
(4)高聚物G中含有的—OH使该物质具有亲水性,而H则不具有
略
(14分)某课外活动小组同学用图一装置进行实验,试回答下列问题。

(1)① 若开始时开关K与a连接,则铁发生的是电化学腐蚀中的 腐蚀;
② 若开始时开关K与b连接,则总反应的离子方程式 。
(2)芒硝(化学式为Na2SO4·10H2O),无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法。用如图二所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是提高原料的利用率来看都更加符合绿色化学理念。
① 该电解槽的阳极反应式为: ,此时通过阴离子交换膜的离子数 (填“大于”或“小于”或“等于”)通过阳离子交换膜的离子数。
② 制得的氢氧化钠溶液从出口(选填“A”、“B”、“C”、“D”) 导出。
③ 若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为 。已知H2的燃烧热为285.8 kJ/mol,则该燃料电池工作产生36 g H2O时,理论上有 kJ的能量转化为电能。
知识点:电解池
(1)① 吸氧
② 2Cl—
+2H2O![]() 2OH—
+ H2↑+ Cl2↑
2OH—
+ H2↑+ Cl2↑
![]() (2)①
4OH—
(2)①
4OH—![]() 4e— 2H2O + O2↑
小于
4e— 2H2O + O2↑
小于
② D ③
H2![]() 2e—+
2OH— == 2H2O
57
2e—+
2OH— == 2H2O
57
略