科学家预测:人类将在21世纪大量使用氢气作燃料。其中最理想获得氢气的途径是
A.以焦炭和水制取水煤气后分离出氢气
B.用铁、锌等活泼金属与稀硫酸反应制取氢气
C.由火力发电厂提供电力电解水产生氢气
D.利用高效催化剂和太阳能使海水分解产生氢气
知识点:化学与技术
D
已知碳有三种常见的同位素:12C、13C、14C,氧也有三种同位素:16O、17O、18O,由这六种微粒构成的二氧化碳分子中,其相对分子质量最多有
A.18种 B.6种 C.7种 D.12种
知识点:原子结构与性质
C
甲、乙是周期表中同一主族的两种元素,若甲的原子序数为X,则乙的原子序数可能为
①X+2 ②X+8 ③X+26 ④X-18 ⑤X+14
A.①②③④ B.①③④⑤ C.①②④ D.全部
知识点:元素周期律与元素周期表
A
现有如下各说法:①原子种类由原子核内质子数决定;②全部由非金属元素形成的化合物一定为共价化合物;③离子键是阳离子、阴离子之间的相互吸引作用;④互为同分异构体的物质一定具有相同的相对分子量;⑤同素异形体在一定条件下的转化为物理变化;⑥CCl4晶体和NH4Cl晶体中所含的化学键类型相同。上述各种说法正确的是
A.①②⑤正确 B.仅④正确
C.仅①不正确 D.都不正确
知识点:化学用语及其规律
B
下列数据是对应物质的熔点,据此做出的下列判断中错误的是
物质
Na2O
NaCl
AlF3
AlCl3
熔点℃
920
801
1291
190
物质
BCl3
Al2O3
CO2
SiO2
熔点℃
-107
2073
-57
1723
A.铝的化合物的晶体中不完全是离子晶体
B.同族元素的氧化物可形成不同类型的晶体
C.表中只有BCl3和干冰是分子晶体
D.不同族元素的氧化物可形成相同类型的晶体
知识点:晶体结构与性质
C
在一定条件下,测得2CO2![]() 2CO+O2(反应从CO2开始)平衡体系的平均相对分子质量为M,在此条件下,CO2的分解率为
2CO+O2(反应从CO2开始)平衡体系的平均相对分子质量为M,在此条件下,CO2的分解率为
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
知识点:化学反应速率和化学平衡的计算
B
已知SO2和O2反应生成4 mol SO3时放出的热量为Q kJ,那么2 mol SO2和1 mol O2,在一有催化剂的密闭容器中发生反应时,放出的热量为
A.等于Q kJ B.等于0.5Q kJ C.小于0.5Q kJ D.无法确定
知识点:反应热的计算
C
已知镁和稀硝酸反应时,每有1mol HNO3反应,就有0.8mol电子转移,此时硝酸的还原产物可能是
A.NO2 B.N2O C.N2 D.NO
知识点:氧化还原反应
B
(4分)某简单微粒的结构示意图为:

且X、Y 均为不大于20的正整数,据此回答下列问题:
(1)若该微粒一般情况下不与其它元素的原子反应,这种微粒的符号是
(2)若该微粒有很强的非金属性,且只需得到一个电子就能达到稳定结构,这种微粒的结构示意图为
(3)若该微粒为一价阳离子,且对应的碱为可溶性强碱,则x= y= 。
知识点:元素周期律与元素周期表
(1)微粒符号是 Ar
(2)这种微粒的结构示意图为 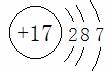
(3) x= 19 ,y= 8 。
(4分)在试管里放入一块铜片,注入一定体积的浓硫酸,给试管加热,使之反应。
(1)若铜片还有剩余,硫酸________消耗完毕(填“已经”或“没有”)。
其理由是____________________________________________________________________________________。
(2)往上述试管中加入以下物质会使铜的质量进一步减少的是_____________________。
A、KNO3 B、氨水 C、FeCl2 D、FeCl3
知识点:氧族元素
(1)____没有___ (填“已经”或“没有”)。
其理由是__随着反应的进行,硫酸的浓度在逐渐下降,而Cu与稀硫酸不会发生反应。
(2)____AD____。
(8分)某学生课外活动小组利用右图所示装置分别做如下实验:
 ⑴在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________________溶液;
⑴在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________________溶液;
加热时溶液由红色逐渐变浅的原因是:________ _____
⑵在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________________溶液;加热时溶液由无色变为红色的原因是: _________________。
知识点:物质的分离、除杂和提纯
⑴ _溶有NH3的酚酞______溶液;
原因是: 加热时NH3逸出,溶液变为无色 。
⑵__SO2的品红____ 溶液;
原因是: 加热时SO2逸出,品红溶液呈红色__ 。
(12分)在下图中,左边为CuCl2溶液,右边为含少量NaOH的H2O溶液。现以惰性电极进行电解。
(1)写出A、B电极的名称以及相应的电极方程式:
A:________________________________
B:________________________________
(2)右边水溶液中加少量NaOH的作用是____________________________。
(3)在A、B、C、D各电极上产生的生成物的物质的量之比为____________________________。

(4)若此电源是利用肼(NH2-NH2)、氧气与KOH溶液组成的碱性燃料电池,已知其总反应为:NH2-NH2+O2==N2+2H2O
请分别写出该电池正极和负极的电极反应式:
负极 ;
正极 。
知识点:电解池
(1) A:_阴极:Cu2++2e=Cu_______________________________
B:__阳极:2Cl——2e=Cl2_↑_______________________
(2)加少量NaOH的作用是_增强溶液的导电性_____________。
(3)在A、B、C、D产生的生成物的物质的量之比为:___2:2:2:1_______。
(4)负极 NH2—NH2 +4OH—==4H2O+N2 ;
正极 O2+2H2O+4e=4OH— 。
(8分)碳酸氢铵和熟石灰共热时可能发生如下反应:
NH4HCO3+Ca(OH)2![]() CaCO3+NH3↑十+2H2O
CaCO3+NH3↑十+2H2O
NH4HCO3![]() NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
取碳酸氢铵和熟石灰的混合物共0.1mol,在密闭容器中加热至200℃,充分反应后,排出多余的气体,冷却后称量,固体剩余物质量为a g。
(注:CaCO3的分解温度为898℃)
求:(1)碳酸氢铵和熟石灰以等物质的量混合时,a等于多少?
(2)若以bmol表示混合物中碳酸氢铵的物质的量,通过计算确定a随b变化的数学表达式。
知识点:氮族元素
(1) a= 5 g。(3分)
(2)表达式: 0<b<0.05;a=100b+74(0.1-2b)
0.05≤b<0.1;a=100(0.1-b) (5分)
(6分)在酸溶液中,10.00g Cu2S和CuS的混合物与250.0mL 0.7500 mol·L-1的MnO4-反应生成了SO42-、Cu2+和Mn2+。剩余的MnO4-恰好与175.0mL浓度为 1.000 mol·L-1的Fe2+ 溶液反应。
(1)分别写出Cu2S、CuS与酸性KMnO4溶液反应的离子方程式,并配平。
(2)试计算原始混合物中 CuS 的质量分数。
知识点:氧族元素
(1)Cu2S+2MnO4- +8H+==2Cu2+ + SO42-+ 2Mn2+ + 4H2O (2分)
5CuS+8MnO4- +24H+==5Cu2+ + 5SO42- + 8Mn2+ + 12H2O (2分)
5Fe2+ + MnO4- +8H+ === 5Fe3+ + Mn2+ + 4H2O (2分)
(2) 设 Cu2S Xmol CuS Ymol
160X + 96Y == 10
![]()
X=0.02125 Y=0.06875 W=66% (2分)
(5分)在少量水存在下,使9.8g的固体物质A和3.6 g的固体物质B反应,生成了4.48L气态产物C(标况下),该气体的密度为0.759g/L。将同样多的物质A同过量2倍的氢氧化钙一起加热,产生1.70g气体,向3.6g物质B中逐滴加入氢溴酸直至反应终止,同样生成1.70g气体。若已知在三种情况下,均生成了同一气态和固态产物,由此推知:
(1)A是 ,B是 ,C是
(2)写出化学方程式:A和B
知识点:氮族元素
(1)NH4Br;Ca(NH2)2;NH3
(2)2NH4Br+Ca(NH2)2=CaBr2+4NH3
(9分)铜及其合金是人类最早使用的金属材料。
 (1)铜原子的核外电子排布式是 。
(1)铜原子的核外电子排布式是 。
(2)如图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为 。
(3)Cu2+能与NH3、H2O、C1-等形成配位数为4的配合物。
①[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 。
②某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO。在丙烯醇分子中发生某种方式杂化的碳原子数,是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化方式为 。
(4)CaO晶体的结构与NaCl相同,CaO晶体中Ca2+的配位数为 。
晶格能分别为:CaO为-3401 kJ·mol-1、NaCl为-786 kJ·mol-1。导致两者晶格能差异的主要原因是 。
(5)假定铁有简单立方、体心立方(bcp)、面心立方(ccp)三种同素异形体,三种晶体在不同温度下能发生相互转化。若三种同素异形体晶胞边长分别为a cm, b cm,c cm则三种晶体密度比为 。
知识点:晶体结构与性质
(1)1s22s22p63s23p63d104s1;
(2)1:5;
(3)平面正方形;sp2;
(4)6;CaO晶体中离子电荷数大于NaC1,所以晶格能大;
(5)1/a3:12/b3:4/c3
(11分)利用燃料和氧化剂之间发生的氧化还原反应,将化学能直接转化为电能的装置叫燃料电池,它是一种高效低污染的新型电池。燃料电池所用燃料可以是氢气,也可以是甲烷、甲醇、肼、氨等。肼分子(H2N-NH2)可以在氧气中燃烧生成氮气和水,回答下列问题:
(1)利用肼、氧气与KOH溶液组成碱性燃料电池,请写出该电池负极的电极反应式:
,并指出电解质溶液中OH-离子向 极移动。
若用该燃料电池电解饱和食盐水得C12 7.1g,则需肼 g,若想将电解后饱和食盐水恢复原状,需 。
(2)用电离方程式表示肼的水溶液呈碱性的原因 ;
(3)天然气有着来源广,污染小的优点,但未能在汽车燃料中推广应用,而其催化氧化产物甲醇却被推广使用,主要是因为 。
(4)如果将燃料改为汽油则为汽油燃料电池,该燃料电池最大的障碍是氧化反应不完全产生 堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间,正是新一代化学家的历史使命。
(5)肼是强还原剂,与氧化剂H2O2反应时可放出大量的热,因此,肼可以作为火箭推进剂。
某些共价键的键能
键
键能/kJ·mol-1
键
键能/kJ·mol-1
键
键能/kJ·mol-1
N-N
193
N=N
418
N≡N
946
O-O
142
O=O
497
H-H
436
N-H
391
O-H
463
根据以上信息,试写出肼与H2O2反应的热化学方程式 。
知识点:原电池
(1)N2H4-4e-+4OH-=N2+4H2O;负;1.6;通0.2molHC1气体。
(2)![]()
(3)甲烷难液化(甲烷是气体,而甲醇是液体)。 (1分)
(4)碳
(5)N2H4(g)+2H2O2(g)=N2(g)+4H2O(g) △H=-757kJ/mol
(8分)某研究性学习小组成员,利用稀硫酸与某金属的反应来探究影响化学反应速率的因素,下表是研究过程中记录的实验数据:(表中某些数据记录已模糊不清,个别数据已丢失。)
![]() 实验
实验
序号
金属
质量/g
金属
状态
c(H2SO4)
/mol·L-1
v(H2SO4)
/mL
溶液温度/°C
金属消失的时间/s
1
0.10
丝
0.5
50
20
34
500
2
0.10
粉末
0.5
50
20
35
50
3
0.10
丝
0.7
50
20
36
数据模糊
4
0.10
丝
0.8
50
20
35
200
5
0.10
粉末
0.8
50
20
36
数据模糊
6
0.10
丝
1.0
50
20
35
数据模糊
7
0.10
丝
1.0
50
35
数据模糊
50
8
0.10
丝
1.1
50
20
34
100
9
0.10
丝
1.1
50
数据丢失
44
40
若实验操作、数据记录均是正确的,请分析上述数据,回答下列问题:
(1)该实验主要是探究 因素对反应速率的影响。
(2)经仔细辨认,模糊的数据疑为25、50、125、250,试将这些疑似数据填入表中,使实验数据较为合理。
(3)试猜测实验9反应前溶液的温度约为 °C。推测的依据是 。
知识点:化学反应速率
(1)金属表面积、硫酸溶液浓度、反应的温度。(2分)
(2)(4分)
|
序号 |
金属 质量/g |
金属 状态 |
c(H2SO4) /mol·L—1 |
v(H2SO4) /mL |
溶液温度/°C |
金属消失的时间/s | |
|
1 |
0.10 |
丝 |
0.5 |
50 |
20 |
34 |
500 |
|
2 |
0.10 |
粉末 |
0.5 |
50 |
20 |
35 |
50 |
|
3 |
0.10 |
丝 |
0.7 |
50 |
20 |
36 |
250 |
|
4 |
0.10 |
丝 |
0.8 |
50 |
20 |
35 |
200 |
|
5 |
0.10 |
粉末 |
0.8 |
50 |
20 |
36 |
25 |
|
6 |
0.10 |
丝 |
1.0 |
50 |
20 |
35 |
125 |
|
7 |
0.10 |
丝 |
1.0 |
50 |
35 |
50 |
50 |
|
8 |
0.10 |
丝 |
1.1 |
50 |
20 |
34 |
100 |
|
9 |
0.10 |
丝 |
1.1 |
50 |
数据丢失 |
44 |
40 |
(3)30(1分)等量的金属和酸反应放出的热量基本相同,使等量的溶液温度均约升高15°C。(1分)
液态锂离子电池是指Li+嵌入化合物为正负电池的二次电池。正极采用锂化合物LiCoO2,负极采用碳电极,充电后成为锂-碳层间化合物LixC6(0<x≤1),电解质为溶解有锂盐LiPF6、LiAsF6等的有机溶液。下列有关说法不正确的是
A.将LiCoO2改写成为氧化物的形式为Li2O·Co2O3
B.该电池的电解液必须使用有机溶剂主要是由于有机溶剂有良好的导电性
C.Li是3号元素,是最轻的金属之一,这类电池比能量高
D.在电池充、放电时,Li+在两个电极之间往返嵌入和脱嵌。该电池的充放电反应方程式为:
![]()
知识点:原电池
BD
有一包白色固体,可能有①(NH4)2SO4,②Al2(SO4)3,③NaCl,④AgNO3,⑤KOH,⑥KI,⑦BaCl2中的一种或几种组成,该固体溶于水得到澄清溶液,而且该溶液能使酸酞呈红色,若在该溶液中加入适量的稀硝酸,可得到白色沉淀。该白色固体可能的组成是
A.②③⑤ B.②⑤⑦ C.①③④⑤ D.①④⑤⑦
知识点:元素及其化合物的综合运用
AC
如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是
 A.b中铁钉附近呈现红色
A.b中铁钉附近呈现红色
B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应
D.b中铝条附近有气泡产生
知识点:原电池
AB