图分别代表NaCl、金刚石、干冰、石墨结构的一部分.下列说法正确的是( )

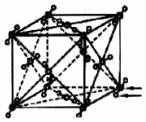
A.如图,NaCl晶体只有在熔融状态下离子键被完全破坏,才能形成自由移动的离子
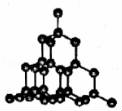
B.如图,金刚石中存在的化学键只有共价键,不能导电
C.如图,干冰中的化学键只需吸收很少的热量就可以破坏,所以干冰容易升华

D.如图,石墨中碳原子的最外层电子都参与了共价键的形成,故熔点很高、硬度很大
知识点:化学
B
【考点】不同晶体的结构微粒及微粒间作用力的区别.
【分析】A、熔融状态下离子键被削弱,形成自由移动的离子;
B、金刚石是原子晶体,原子间通过共价键结合形成空间网状结构;
C、干冰是分子间作用力,而不是化学键;
D、石墨中碳原子的最外层电子只有三个电子参与成键,层与层之间滑动.
【解答】解:A、熔融状态下离子键被削弱,而不是离子键被完全破坏,故A错误;
B、金刚石是原子晶体,原子间通过共价键结合形成空间网状结构,无自由电子,所以不能导电,故B正确;
C、干冰是分子间作用力,而不是化学键,故C错误;
D、石墨中碳原子的最外层电子只有三个电子参与成键,层与层之间滑动,很软,故D错误;
故选B.
【点评】本题考查化学键与晶体类型,难度不大,掌握常见物质的晶体类型是解题的关键.