下列叙述中正确的是 ( )
A.1 mol CO的质量是28 g
B.硝酸的摩尔质量为63 g
C.2 g氢气所含原子数目为1 mol
D.铁的摩尔质量就是铁原子的相对原子质量
知识点:化学
A
下列说法正确的是 ( )
A.CO2的相对分子质量为44 g·mol-1
B.“物质的量”是“物质的质量”的简称
C.摩尔只能用于计量纯净物
D.阿伏加德罗常数的单位是mol-1
知识点:化学
D
绿色植物是空气天然的“净化器”,研究发现,1万平方米柳杉每月可以吸收160 kg SO2,则1万平方米柳杉每月吸收的SO2的物质的量为 ( )
A.164 kg B.2.5 mol
C.2 500 g·mol-1 D.2 500 mol
知识点:化学
D
下列叙述正确的是 ( )
A.氢氧化钠的摩尔质量是40 g
B.1 mol NaOH的质量是40 g·mol-1
C.1 g H2和1 g N2所含分子数相等
D.等质量的N2、CH4、CO、H2O中,CH4所含分子数最多
知识点:化学
D
下列关于2 mol二氧化碳的叙述中,正确的是 ( )
A.含有2 mol的氧气分子 B.质量为88 g
C.分子数为6.02×1023 D.含有4 mol原子
知识点:化学
B
下列有关阿伏加德罗常数(NA)的说法错误的是 ( )
A.常温常压下28 g N2所含的原子数目为2NA
B.标准状况下0.5 mol H2O含有的原子数目为1.5NA
C.任何条件下0.5 mol氨气分子的分子数一定是0.5NA
D.49 g H2SO4中含有的原子数目为1.5NA
知识点:化学
D
(1)甲烷(CH4)的摩尔质量为__ __;8 g CH4中约含有__ _个分子、含有__ _mol电子。
(2)含原子数相等的甲烷和氨气(NH3)的质量比为__ _。
知识点:化学
(1) 16 g·mol-1 3.01×1023 5
(2) 64:85
解析:(1)甲烷(CH4)的摩尔质量为16 g·mol-1。8 g CH4的物质的量为0.5 mol,约含有3.01×1023个分子、含有5 mol电子。(2)假设所含的原子均为1 mol,甲烷和氨气(NH3)的质量比=(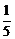 ×16):(
×16):( ×17)=64:85。
×17)=64:85。
(1)请填写下表:
物质
摩尔质量
物质的量
质量
分子或
离子数目
SO2
64 g·mol-1
2 mol
SO
96 g·mol-1
6.02×1022
O2
32 g·mol-1
8.0 g
(2)摩尔质量是指单位物质的量的物质所含有的质量。
①已知NH3的相对分子质量为17,则NH3的摩尔质量为 。
②NA为阿伏加德罗常数,已知a g某气体中含分子数为b,则该气体的摩尔质量为 。
③已知一个铁原子的质量为b g,则铁的摩尔质量为 。
④1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为 。
知识点:化学
(1)请填写下表:
物质 | 摩尔质量 | 物质的量 | 质量 | 分子或 离子数目 |
SO2 |
|
| 128 g | 1.204×1024 |
SO |
| 0.1 mol | 9.6 g |
|
O2 |
| __0.25 mol__ |
| __1.505×1023__ |
(2)①17 g·mol-1
②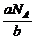 g·mol-1
g·mol-1
③bNA g·mol-1
④64 g·mol-1
解析:(1)结合各元素原子的相对原子质量可得其相应摩尔质量,由n=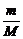 关系式,可推导其他未知量。(2)①相对分子质量在数值上与摩尔质量相等,M(NH3)=17 g·mol-1。②由公式N=n·NA=
关系式,可推导其他未知量。(2)①相对分子质量在数值上与摩尔质量相等,M(NH3)=17 g·mol-1。②由公式N=n·NA=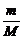 NA,可得M=
NA,可得M=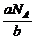 g·mol-1。③由公式M(Fe)=NA·m(Fe)=b·NA g·mol-1。
g·mol-1。③由公式M(Fe)=NA·m(Fe)=b·NA g·mol-1。
④由公式N=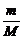 ·NA,知1.204×1022=
·NA,知1.204×1022=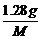 ×6.02×1023mol-1,M=64 g·mol-1。
×6.02×1023mol-1,M=64 g·mol-1。