分类法是学习和研究化学的一种重要方法。下列分类不合理的是 ( )
A.KOH和Na2CO3都属于碱 B.K2CO3和KHCO3都属于盐
C.H2SO4和HNO3都属于酸 D.Na2O和SiO2都属于氧化物
知识点:化学
A
下列化合物依次属于氧化物、碱、盐的一组是 ( )
A.Na2CO3、KOH、CaO B.CO、NaOH、KCl
C.H2O、H2SO4、NaCl D.CuO、Cu2(OH)2CO3、CaCO3
知识点:化学
B
解析:A项中的Na2CO3属于盐,C项中的H2SO4属于酸,D项中的Cu2(OH)2CO3属于盐。
下列物质间的转化不能一步实现的是 ( )
A.Na2CO3―→NaOH B.CaCO3―→CaO
C.NaCl―→NaNO3 D.C―→CuO
知识点:化学
D
解析:Na2CO3与Ba(OH)2、Ca(OH)2等反应可一步生成NaOH;CaCO3受热分解生成CaO;NaCl与AgNO3反应可生成NaNO3;C不能一步生成CuO。
下表所列各组物质中,物质之间按箭头方向不能通过一步反应实现如图所示转化的是 ( )

物质
选项
甲
乙
丙
A
CuO
CO2
H2O
B
C
CO
CO2
C
CaCO3
CaO
Ca(OH)2
D
H2SO4
H2O
H2
知识点:化学
C
解析:CuO与CO反应生成铜和CO2,CO2与碱反应能生成水,氧化铜与氢气反应能生成水,图示为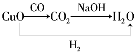 ,A正确;碳不完全燃烧生成一氧化碳,一氧化碳继续燃烧生成二氧化碳,碳完全燃烧生成二氧化碳,图示为
,A正确;碳不完全燃烧生成一氧化碳,一氧化碳继续燃烧生成二氧化碳,碳完全燃烧生成二氧化碳,图示为 ,B正确;CaCO3难溶于水,不与碱溶液发生反应,不能生成氢氧化钙,C错误;硫酸与碱反应可以生成水,与活泼金属反应生成氢气,电解水生成氢气,图示为
,B正确;CaCO3难溶于水,不与碱溶液发生反应,不能生成氢氧化钙,C错误;硫酸与碱反应可以生成水,与活泼金属反应生成氢气,电解水生成氢气,图示为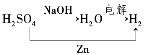 ,D正确。
,D正确。
给如图中①~⑤选择适当的物质,使有连线的两物质能发生反应。供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉。下列说法正确的是 ( )

A.单质①为铜 B.氧化物④为CO2
C.①与②反应为置换反应 D.③与④反应为复分解反应
知识点:化学
C
解析:据单质①能和酸②发生化学反应,由题意可推知①应为活泼金属单质即为铁。而酸只有H2SO4,则氧化物④应为金属氧化物CaO,则氧化物③为酸性氧化物,即CO2,⑤属于盐且既能与稀硫酸反应。又能与CaO反应,则⑤应为Na2CO3。其中①与②反应为置换反应,③与④反应为化合反应。
盐是一类常见的物质,下列物质通过一步反应可直接形成盐的是 ( )
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸
A.①②③ B.①④⑥
C.②⑤⑥ D.全部
知识点:化学
D
解析:题中所列物质均可通过一步反应直接形成盐。
单质、氧化物、酸、碱、盐之间可按照如下关系进行转化。
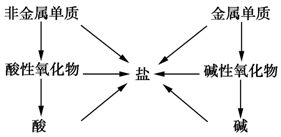
熟练掌握单质、氧化物、酸、碱、盐之间的反应关系和反应类型即可得出正确答案。
下列叙述正确的是 ( )
A.纯碱、烧碱均属碱
B.SiO2、SO2均属酸性氧化物
C.凡能电离出H+的化合物均属酸
D.盐类物质一定含有金属离子
知识点:化学
B
解析:A.纯碱由金属阳离子和酸根离子组成,属于盐,碱是电离出的阴离子全部是氢氧根离子的化合物,故A错误;B.SiO2、SO2均能与碱反应生成盐和水,属于酸性氧化物,故B正确;C.电离出来的阳离子全部是H+离子的化合物属于酸,如NaHSO4也能电离出来H+离子,但同时也电离出Na+离子,属于盐,故C错误;D.铵盐全部为非金属元素组成的化合物,故D错误。故选B。
下列各组物质中有一种物质与其他三种物质的分类不同,请找出该物质并书写在横线上。
(1)HCl H2SO4 H2CO3 HNO3 __ __
(2)NaCl KNO3 Na2CO3 NaNO3 __ _
(3)Fe Al Zn C __ _
(4)溶液 水 浊液 胶体 __ _
知识点:化学
(1) __HCl__
(2) __NaCl或KNO3__
(3)__C__
(4) __水__
解析:(1)只有HCl是无氧酸,其余是含氧酸。(2)只有KNO3是钾盐,其余是钠盐;只有NaCl是无氧酸盐,其余是含氧酸盐。(3)只有C是非金属单质,其余都是金属单质。(4)只有水是纯净物,其余都是混合物。
无机化合物可根据其组成和性质进行分类:
(1)下图所示的物质分类方法名称是__ __;

(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。(只需填一种)
物质类别
强酸
强碱
盐
氧化物
化学式
①HCl
②
③
④KOH
⑤Na2CO3
⑥__
⑦CO2
⑧Na2O2
(3)写出⑦转化为⑤的化学方程式:
知识点:化学
(1)树状分类法;
(2)②H2SO4 ③NaOH ⑥K2CO3
(3) 2NaOH+CO2===Na2CO3+H2O
解析:(1)物质分类常用树状分类法和交叉分类法,此分类法为树状分类法。(2)由题中元素形成常见的强酸有H2SO4、HNO3;形成的强碱有NaOH、KOH;形成的盐有Na2CO3、K2CO3、Na2SO4、K2SO4、NaNO3、KNO3、Na2SO3、K2SO3。(3)二氧化碳与氢氧化钠反应生成碳酸钠和水,化学方程式为2NaOH+CO2===Na2CO3+H2O。