V L Fe2(SO4)3溶液中含Fe3+m g,则溶液中SO42-的物质的量浓度为 ( )
A. mol·L-1 B.
mol·L-1 B. mol·L-1
mol·L-1
C. mol·L-1 D.
mol·L-1 D. mol·L-1
mol·L-1
知识点:化学
D
解析:n(Fe3+)=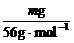 ,n(SO42-)=
,n(SO42-)=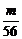 ×
×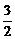 mol=
mol=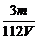 mol,c(SO42-)=
mol,c(SO42-)= =
=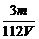 mol·L-1。
mol·L-1。
下列溶液中c(NO3-)比100 mL 2 mol·L-1的硝酸钡溶液中c(NO3-)大的是 ( )
A.300 mL 1 mol·L-1的硝酸钠溶液
B.200 mL 1.5 mol·L-1的硝酸镁溶液
C.100 mL 1.5 mol·L-1的硝酸铝溶液
D.200 mL 3 mol·L-1的硝酸钾溶液
知识点:化学
C
在标准状况下,将ω g A气体(摩尔质量为M g·mol-1)溶于1 L水中,所得溶液密度为d g·mL-1,则此溶液的物质的量浓度为 ( )
A. B.
B.
C. D.
D.
知识点:化学
A
下列有关溶液配制的叙述正确的是 ( )
A.将58.5 g NaCl溶于1 L水中可得1 L 1.00 mol·L-1NaCl溶液
B.溶液定容时仰视容量瓶的刻度线,所得溶液的浓度偏大
C.定容摇匀后发现液面低于刻度线,需再加水至刻度线
D.容量瓶中原有少量的蒸馏水,不影响配制溶液的浓度
知识点:化学
D
300 mL 0.2 mol·L-1KCl溶液与100 mL 0.3 mol·L-1AlCl3溶液中Cl-物质的量浓度之比是 ( )
A.1﹕3 B.2﹕3
C.2﹕1 D.2﹕9
知识点:化学
D
实验室需要1.0 mol·L-1NaOH溶液400 mL,根据溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号);配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。

(2)下列有关容量瓶的构造和使用描述中,正确的是__ __(填序号)。
A.用于配制一定体积的、浓度准确的溶液
B.用于贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.容量瓶上标有温度和容积
E.配制一定体积、浓度的溶液时,容量瓶未干燥,所配溶液浓度偏小
(3)请计算需用托盘天平称取固体NaOH的质量为__ __g。
知识点:化学
(1) __A、B__ __玻璃棒_
(2)__A、D_
(3) __20.0__
配制480 mL 0.5 mol·L-1的NaOH溶液,试回答下列问题:
(1)选择仪器:完成本实验所必需的仪器有托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、_ __、__ __等。
(2)计算、称量:需称量NaOH固体的质量为__ 。
(3)溶解、冷却:该步实验中需要使用玻璃棒,作用是__ __。
(4)转移、洗涤:洗涤烧杯2~3次是为了__ __。
(5)定容、摇匀:定容的具体操作是
(6)不规范的实验操作会导致实验结果的误差,下列使所配制溶液的物质的量浓度偏高的是____,偏低的是____(填序号)。
①在溶解过程中有少量液体溅出烧杯外
②定容时俯视刻度线
③将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
④定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线
知识点:化学
(1) __胶头滴管__、__500_mL容量瓶__
(2) _10.0g_
(3) __搅拌、加速溶解__
(4) __保证溶质全部转移至容量瓶中_
(5) __向容量瓶中加入蒸馏水至距刻度线1~2_cm时,改用胶头滴管滴加蒸馏水至液体的凹液面最低处和刻度线相切__
(6) __②③__ __①④_
解析:(1)配制一定体积、一定物质的量浓度的溶液使用的仪器有托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、胶头滴管、500 mL容量瓶。(2)计算、称量:由于没有480 mL容量瓶,要使用500 mL容量瓶,因此需称量NaOH固体的质量为m=0.5 L×0.5 mol·L-1×40 g·mol-1=10.0 g。(3)溶解、冷却:该步实验中需要使用玻璃棒,作用是搅拌、加速NaOH固体的溶解。(4)转移、洗涤:洗涤烧杯2~3次是为了保证溶质全部转移至容量瓶中,使配制的溶液浓度更准确。(5)定容、摇匀:定容的具体操作是向容量瓶中加入蒸馏水至距刻度线1~2 cm时,改用胶头滴管滴加蒸馏水至液体的凹液面最低处和刻度线相切。(6)①在溶解过程中有少量液体溅出烧杯外,使溶质的质量减少,溶质的物质的量也减少,因此溶液的浓度偏低;②定容时俯视刻度线.则溶液的体积偏小,使溶液的浓度偏高;③将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容,溶液的温度高于容量瓶的使用温度,当恢复至室温时,溶液的体积偏小,使溶液的浓度偏高;④定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线,则溶液的体积偏大,使溶液的浓度偏低。
用物质的量浓度来表示溶液的组成对生产和科学研究都有重要的意义。下表是某人体检表上的部分信息,其中是用物质的量浓度来表示的是 ( )
项目名称 结果 单位 参考值
1谷丙转氨酶 7 U/L <40
8球蛋白 26.7 g/L 20~30
10乳酸脱氢酶 161 U/L 114~240
16葡萄糖 4.94 mmol/L 3.61~6.11
送检日期:2014-06-10 报告日期:2014-06-10
A.谷丙转氨酶 B.球蛋白
C.乳酸脱氢酶 D.葡萄糖
知识点:化学
D
解析:看清物理量的单位即可,物质的量浓度的单位通常为mol/L,此处为mmol/L。
在科学实验和工农业生产中,所使用的一定量的溶液一般都是量取它的体积,而较少称量它的质量。在溶液中发生的化学反应,反应物和生成物的物质的量也存在一定的比例关系。因此我们引入一个新的物理量——物质的量浓度来建立物质的量和溶液体积的关系。认真分析物质的量浓度的概念及其定义式并思考,下列溶液中溶质的物质的量浓度为1 mol/L的是 ( )
A.将40 g NaOH溶解于1 L水中
B.将22.4 L氯化氢气体溶于水配成1 L溶液
C.将1 L 10 mol/L的浓盐酸与9 L水混合
D.将10 g NaOH溶解于水中配成250 mL溶液
知识点:化学
D
解析:物质的量浓度表示的是单位体积溶液(注意不是溶剂)中所含溶质的物质的量。A项错误,溶剂是1 L,溶液必大于1 L;B项错误,谈气体体积不指明状况是毫无意义的,如改为标准状况,则此项正确;C项错误,所得溶液总体积不是10 L;D项正确,NaOH为0.25 mol,溶液体积为0.25 L,其物质的量浓度为1 mol/L。
向60 mL Na2SO4溶液中加入BaCl2溶液,有关数据见下表:
实验编号
1
2
3
4
5
BaCl2溶液体积/mL
0
30
60
100
120
沉淀质量/g
0
0.699
x
2.097
2.097
下列有关说法不正确的是 ( )
A.混合前,BaCl2溶液的物质的量浓度为0.10 mol·L-1
B.混合前,Na2SO4溶液的物质的量浓度为0.15 mol·L-1
C.3号实验中沉淀的质量x为1.398 g
D.完全沉淀60 mL Na2SO4溶液消耗BaCl2溶液的体积为80 mL
知识点:化学
D
解析:A项正确,利用实验2数据,溶液中BaCl2的物质的量为0.003 mol,其浓度为0.1 mol/L;B项正确,利用实验4或实验5数据,知Na2SO4溶液中n(Na2SO4)为0.009 mol,其浓度为0.15 mol/L;C项正确,判断实验3中Na2SO4仍剩余,所以生成沉淀量为实验2的2倍;D项错误,所需BaCl2溶液的体积应为90 mL。
下列关于物质的量浓度表述正确的是 ( )
A.0.3 mol·L-1的Na2SO4溶液中含有Na+和SO的总物质的量为0.9 mol
B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol·L-1,当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol·L-1
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO的物质的量相等,则K+和Cl-的物质的量浓度一定相同
D.10℃时,100 mL 0.35 mol·L-1的KCl饱和溶液蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol·L-1
知识点:化学
D
解析:A项错误,体积未知;B项错误中,状态未定,氨气的量不一定是1 mol;C项错误,根据电荷守恒,c(K+)一定大于c(Cl-);D项正确,温度一定且二者均为饱和溶液,所以溶液组成相同。
观察下图,若用1 L水来代表地球上的总水量,要比较精确地量取地球上的淡水量,应选择的仪器是 ( )

A.100 mL烧杯 B.50 mL烧杯
C.100 mL量筒 D.50 mL量筒
知识点:化学
D
解析:选取计量仪器时要选取比所量液体体积大,且最接近的,误差小,当加液体快到刻度时改用胶头滴管精确滴加。1 L水代表地球上的总水量,根据图示,淡水量为30 mL,所以选取的计量仪器的容积为50 mL量筒(因烧杯没有精确刻度)。
实验室配制一定物质的量浓度的溶液时,需用到容量瓶。容量瓶是一种颈部细长的梨形瓶,其上标有温度、容量和刻度线。由于其颈部细长,所以在向容量瓶中转移液体时,需要有一定的耐心和技巧。有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是 ( )
A.可以按此建议改进,因为可在使用容量瓶时带来方便
B.不能按此建议改进,因为会降低容量瓶的精度
C.如果加粗瓶颈,可将原刻在容量瓶瓶颈上的刻度改刻在容量瓶的瓶身上
D.不必加粗瓶颈,因为向容量瓶中转移液体时,少量液体倒出瓶外,不会对溶液的浓度产生影响
知识点:化学
B
解析:容量瓶是一个精密仪器,改粗瓶颈,必然造成精度降低。
安全是顺利进行实验及避免伤害的保障。下列实验操作正确且不是从实验安全角度考虑的是 ( )

A.操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B.操作②:使用CCl4萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
C.操作③:吸收氨气或氯化氢气体并防止倒吸
D.操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
知识点:化学
D
解析:A项不选,连通氢气发生装置的导管在液面下,燃烧的氢气在液面上,可防气体不纯导致发生装置爆炸;B项不选,振荡后分液漏斗内液体大量挥发,压强增大,打开活塞放气,可避免分液漏斗破坏;C项不选,操作设计错误,水层在下层,不能防止倒吸,如改用四氯化碳则正确;D项可选,此操作用于检验容量瓶是否漏液,确保配制液体量准确,与安全无关。
某研究性学习小组用化学方法测量一个不规则容器的体积。把35.1 g NaCl放入500 mL烧杯中,加入150 mL蒸馏水。待NaCl完全溶解后,将溶液全部转移到容器中。用蒸馏水稀释至完全充满容器。从中取出溶液100 mL,该溶液恰好与20 mL 0.100 mol·L-1AgNO3溶液完全反应。则该容器的容积为____。
知识点:化学
30 L
解析:由题意NaCl~AgNO3,可求出稀释后的NaCl溶液的物质的量浓度。c(NaCl)= =0.020 mol·L-1,则稀释后的NaCl溶液的总体积为:V(NaCl)=
=0.020 mol·L-1,则稀释后的NaCl溶液的总体积为:V(NaCl)=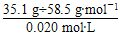 =30 L。
=30 L。
在0.4 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。

(1)该混合液中,NaCl的物质的量为 mol,含溶质MgCl2的质量为__ __g。
(2)该混合液中CaCl2的物质的量为__ _mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为__ __mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀__ __mol。
知识点:化学
(1) __0.4__ __19.0__
(2) __0.2__ __0.2__
(3) __1.2__
解析:(1)根据图象可知钠离子的浓度是1.0 mol·L-1,所以溶液中氯化钠的浓度是1.0 mol·L-1,该混合液中NaCl的物质的量为1.0 mol·L-1×0.4 L=0.4 mol;溶液中镁离子的浓度是0.5 mol·L-1,所以溶液中氯化镁的浓度是0.5 mol·L-1,则含溶质MgCl2的质量为0.4 L×0.5 mol·L-1×95 g·mol-1=19.0 g。
(2)溶液中氯离子的浓度是3.0 mol·L-1,所以根据溶液显电中性可知溶液中钙离子的浓度是(3.0 mol·L-1-1.0 mol·L-1-2×0.5 mol·L-1)÷2=0.5 mol·L-1,因此该混合液中CaCl2的物质的量为0.5 mol·L-1×0.4 L=0.2 mol。将该混合液加水稀释至体积为1 L,由于稀释前后溶质的物质的量不变,则稀释后溶液中Ca2+的物质的量浓度为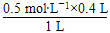 =0.2 mol·L-1。
=0.2 mol·L-1。
(3)溶液中氯离子的物质的量是0.4 L×3.0 mol·L-1=1.2 mol,所以根据方程式Ag++Cl-===AgCl↓可知,向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到氯化银沉淀的物质的量是1.2 mol。