下列有关化学用语使用正确的是

A.硫原子的原子结构示意图: B.NH4Cl的电子式:
 C.原子核内有10个中子的氧原子:
C.原子核内有10个中子的氧原子:![]()
![]() D.次氯酸的电子式:
D.次氯酸的电子式:
知识点:化学用语
略
下列说法正确的是
①离子化合物一定含离子键,也可能含极性键或非极性键
②共价化合物一定含共价键,也可能含离子键W$w#w.k-s+5=u.c.o*m
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物
A.①③⑤ B.②④⑥ C.②③④ D.①③⑥
知识点:化学键
略
NA代表阿伏加德罗常数。下列有关叙述正确的是
A.标准状况下,2.24LH2O含有的分子数等于0.1NA
B.常温下,100mL 1mol·L-1Na2CO3溶液中阴离子总数大于0.1NA
C.分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
D.3.4gNH3中含N—H键数目为0.2NA
知识点:物质的量的计算
略
可以用来判定碳酸氢钠粉末中混有碳酸钠的实验方法是
A.加热时有无色气体放出
B.滴加盐酸时有气泡放出
C.溶于水后,滴加稀的氯化镁溶液有白色沉淀生成
D.溶于水后,滴加澄清石灰水有白色沉淀生成
知识点:碳族元素
略
用下列装置不能达到有关实验目的的是
A.用甲图装置电解精炼铝
B.用乙图装置制备Fe(OH)2
C.用丙图装置可制得金属锰
D.用丁图装置验证NaHCO3和Na2CO3的热稳定性
知识点:仪器和基本操作
略
已知反应:①Cl2+2KBr=2KCl+Br2 ②KClO3+6HCl=3Cl2+KCl+3H2O
③ 2KBrO3+Cl2=Br2+2KClO3,下面说法正确的
A.上述三个反应都有单质生成,所以都是置换反应
B.反应②中还原剂与氧化剂的物质的量之比为6:1
C.反应③中1mol Cl2反应,则氧化剂得电子的物质的量为10mol W$w#w.k-s+5=u.c.o*m
D.氧化性由强到弱的顺序为:KClO3>KBrO3>Cl2>Br2
知识点:氧化还原反应
略
下列说法正确的是:( )
A、仅含有Na+、H+、OH—、CH3COO—四种离子的某溶液中可能存在:
c(Na+)>c(OH—)>c(CH3COO—)>c(H+)
B、铝热法炼铁过程中镁条和氯酸钾起催化作用W$w#w.k-s+5=u.c.o*m
C、二氧化硫![]() 的催化氧化是放热反应,升高温度可以减慢该反应的速率
的催化氧化是放热反应,升高温度可以减慢该反应的速率
D、人体内淀粉、脂肪、蛋白质的水解都是由酶所催化的
知识点:基本概念、基本理论的综合运用
略
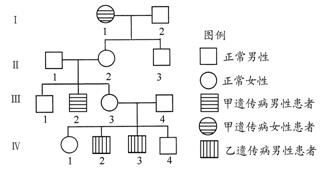
A、B、C为三种短周期元素,A、B在同周期, A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构。下列说法中正确的是
A.原子序数:A>B>C B.原子半径:A>B>C
C.离子半径:A2->C->B2+ D.原子核外最外层电子数:A>C>B
知识点:原子结构与性质
略
下面是以化合物I为原料合成一种香精(化合物Ⅵ)的合成路线,反应在一定条件下进行。化合物Ⅵ广泛用于香精的调香剂。
回答下列问题:
(1)化合物Ⅰ生成化合物Ⅱ的反应原子利用率可达100%,化合物Ⅰ的结构简式为 。
(2)化合物Ⅲ生成化合物Ⅳ发生 反应。
(3)![]() 化合物Ⅴ的多种同分异构体中,与化合物Ⅴ官能团种类相同且无支链的共有_____种。
化合物Ⅴ的多种同分异构体中,与化合物Ⅴ官能团种类相同且无支链的共有_____种。
![]() (4)化合物Ⅵ不能发生的反应类型是
(填字母)。
(4)化合物Ⅵ不能发生的反应类型是
(填字母)。
A.加成反应 B.酯化反应 C.水解反应 D.加聚反应
(5)写出化合物Ⅵ在一定条件下反应,生成高分子化合物的化学方程式: 。
知识点:有机化学知识综合应用
略
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g) ![]() CH3OH(g)
ΔH1
CH3OH(g)
ΔH1
反应Ⅱ: CO2(g) + 3H2(g) ![]() CH3OH(g)
+ H2O(g)
CH3OH(g)
+ H2O(g) ![]() ΔH2
ΔH2
①反应Ⅱ的平衡常数表达式是 。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
温度
250℃
300℃
350℃
K
2.041
0.270
0.012
W$w#w.k-s+5=u.c.o*m由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1 = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2 = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3 = -44.0 kJ/mol
 写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
。
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
。
(3)某实验小组依据甲醇燃烧的反应原理,
设计如图所示的电池装置。该电池正极的电
极反应为 。
知识点:化学反应速率和化学平衡
略
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一![]() 种新工艺流程如下图:
种新工艺流程如下图:
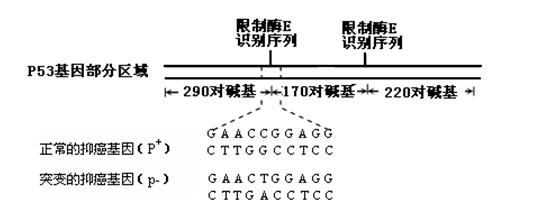
已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的![]() pH见下表:
pH见下表:
沉淀物
Fe(OH)3
Fe(OH)2
Co(OH)2
Al(OH)3
开始沉淀
2.3
7.5
7.6
3.4
完全沉淀
4.1
9.7
9.2
5.2
请回答下列问题:
⑴加入过氧化氢的作用是(用离子方程式示) 。
⑵加入碳酸钠调节pH至a得到的滤渣可部分溶于氢氧化钠溶液,a的范围是 。
⑶操作Ⅰ包含3个基本实验操作,它是 。
⑷制得的CoCl2·6H2O需减压烘干的原因是 ![]() 。
。
知识点:物质的分离、除杂和提纯
略
铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白(可能用到的相对原子质量:Al-27)
[探究一] 实验方案:铝镁合金测定剩余固体质量。
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入VmL 2.0mol·L-1NaOH溶液中,充分反应。NaOH溶液的体积V≥ 。
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
![]() (“偏高”或“偏低”)
(“偏高”或“偏低”)
[探究二] 实验方案:铝镁合金 测定生成气体的体积(实验装置如下图)
问题讨![]() 论:
论:
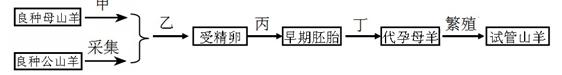
为使测定结果尽可能精确,实验中应注意的
问题是(写出可能的一点): 。
[探究三] 实验方案:称量m g铝镁合金粉末.放在如右图所示装置的惰性电热板上,通电使其充分灼烧。

问题讨论:欲计算Mg的质量分数,该实验中还需测定的
数据是
![]() 。
。
[实验拓展] 请你另设计一个实验方案,测定该铝镁合金中镁的质量分数(书写形式可以模仿探究一、二实验方案)
。
![]()
知识点:综合性实验
略