胡锦涛同志在十七大报告中指出,应加强能源资源节约和生态环境保护,增强可持续发展能力。下列行为与之不相符的是
A.大量使用化肥农药,提高农作物的产量和质量
B.将作物秸秆通过化学反应转化为乙醇用作汽车燃料
C.使用资源节约型、环境友好型的生物降解塑料包装
D.推广煤炭脱硫技术、减少直接燃煤,防止酸雨发生
知识点:化学与生活
A
略
下列化学用语或名称正确的是
A.S原子的结构示意图: B.乙酸乙酯的结构简式:CH3CH2COOCH2CH3
B.乙酸乙酯的结构简式:CH3CH2COOCH2CH3
C.CH4Si的结构式:![]() D.
D.![]() 的名称:2—甲基乙醇
的名称:2—甲基乙醇
知识点:羧酸和酯
C
略
下列说法不正确的是
A.含碳元素的化合物都是有机物
B.饱和一元醇的水溶性随碳原子数的增加而减弱
C.碳酸的酸性比甲酸弱
D. 中含有两种官能团
中含有两种官能团
知识点:乙醇和醇类
A
略
下列反应中原子利用率达100%的是
A.制乙烯: C4H10
![]() C2H4+C2H6
C2H4+C2H6
B.制氯乙烷: CH3CH3+Cl2
![]() CH3CH2Cl+HCl
CH3CH2Cl+HCl
![]() C.制聚乙烯: nCH2=CH2
C.制聚乙烯: nCH2=CH2
![]()
D.制溴苯:![]() +HBr
+HBr
知识点:芳香烃 石油 苯 煤
C
略
下列反应属于吸热反应的是
A.金属钠与水反应 B.氢氧化钡晶体与氯化铵晶体混合的反应
C.盐酸与氢氧化钾溶液反应 D.甲烷在空气中燃烧
知识点:化学反应与能量的变化
B
略
课堂学习中,同学们利用铝条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成。下列结论错误的是

A.原电池是将化学能转化成电能的装置
B.原电池由电极、电解质溶液和导线等组成
C.上图中a极为铝条、b极为锌片时,导线中会产生电流
D.上图中a极为锌片、b极为铜片时,电子由铜片通过导线流向锌片
知识点:原电池
D
略
下列说法正确的是
A.利用分液法可从乙酸和乙醇的混合物中获得乙醇
B.利用新制氢氧化铜浊液在加热条件下可区别葡萄糖和果糖
C.将混有乙烯的甲烷通过盛有溴水的洗气瓶可除去其中的乙烯
D.![]() 和
和 互为同系物
互为同系物
知识点:糖类
C
略
某药物结构简式如右图所示:该物质1mol与足量NaOH溶液反应,消耗的NaOH物质的量为
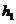
A.3mol B.4mol C.3n mol D.4n mol
知识点:有机合成及高分子化合物
D
略
同温同压下,下列各组热化学方程式中,△H1<△H2的是
A.S(g)+O2(g)=SO2(g) △H1 S(s)+O2(g)=SO2(g) △H2
B.![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g)
△H1
H2(g)+Cl2(g)=2HCl(g)
△H2
Cl2(g)=HCl(g)
△H1
H2(g)+Cl2(g)=2HCl(g)
△H2
C.2H2(g)+O2(g)=2H2O(g) △H1 2H2(g)+O2(g)=2H2O(l) △H2
D.C(s)+![]() O2(g)=CO(g)
△H1
C(s)+O2(g)=CO2(g)
△H2
O2(g)=CO(g)
△H1
C(s)+O2(g)=CO2(g)
△H2
知识点:化学反应的热效应
A
略
已知阿伏加德罗常数近似为6.02×1023mol-1,下列有关叙述不正确的是
A.0.1摩H2O和D2O组成的混合物中含有的中子数为6.02×1023
B.0.5 摩1, 3-丁二烯分子中含有C=C双键数为6.02×1023
C.标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为![]() ×6.02×1023
×6.02×1023
D.1摩碳正离子(CH![]() )所含的电子总数为8×6.02×1023
)所含的电子总数为8×6.02×1023
知识点:化学中常用计量
AC
略
下列反应的离子方程式正确的是
A.苯酚与氢氧化钠溶液反应 C6H5OH+OH—![]() C6H5O—+H2O
C6H5O—+H2O
B.碳酸钙溶于醋酸 CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O
C.碳酸钠溶液加入过量的苯酚 2C6H5OH+CO32— ![]() 2C6H5O—+ CO2↑+H2O
2C6H5O—+ CO2↑+H2O
D.甲醛溶液中加入足量的银氨溶液并加热:
HCHO+2[Ag(NH3)2]++2OH-![]() HCOO-+NH4++2Ag↓+3NH3+H2O
HCOO-+NH4++2Ag↓+3NH3+H2O
知识点:离子方程式
AB
略
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是
A.CH3OH(l)+3/2O2(g)→CO2(g)+2H2O(l)△H=+725.8 kJ/mol
B.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=-1452 kJ/mol
C.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=-725.8 kJ/mol
D.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=+1452 kJ/mol
知识点:化学反应的热效应
B
略
萤光素(X)常用于钞票等防伪印刷,下列关于它的说法不正确的是

A.X中无手性碳原子且所有原子一定共平面
B.X中有12种不同化学环境的氢原子
C.1mol X最多能与9 mol氢气反应
D.X能与糠醛(![]() )发生缩聚反应
)发生缩聚反应
知识点:羧酸和酯
AC
略
A、B两种有机化合物,当混合物质量一定时,无论A、B以何种比例混合,完全燃烧时产生的CO2的量均相等,符合上述条件的是
①同分异构体;②同系物;③具有相同的最简式;④含碳的质量分数相同
A.①③ B.①③④ C.③④ D.①④
知识点:有机化合物的分类、命名与结构特点
B
略
(10分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH
![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)若用下图所示装置来制备少量的乙酸乙酯,其中饱和碳酸钠
溶液的作用是 ▲ 。

(2)此反应以浓硫酸为催化剂,可能会造成 ▲ 、 ▲ 等问题。
(3)在下图所示的装置中进行50 mL 0.50 mol/L醋酸与50 mL 0.55 mol/L NaOH溶液的中和反应。通过测定反应过程中所放出的热量可计算反应热。
回答下列问题:
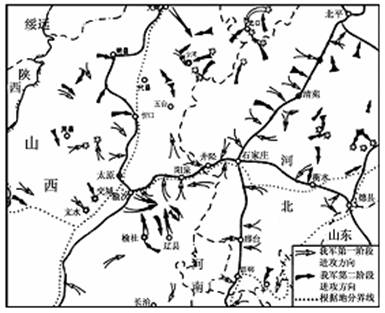
①从实验装置上看,图中尚缺少的一种玻璃用品是 ▲ ;
②在题述反应条件下,测得反应前醋酸和NaOH溶液的温度均
为25.43℃,反应后混合溶液的温度为28.73℃。已知反应前醋酸
和NaOH溶液的密度均为1.0g·cm-3 ,反应后混合溶液的比热容
为c=4.18J/(g·℃)。试写出中和反应的热化学方程式: ▲ 。
知识点:羧酸和酯

(3)①环形玻璃搅拌棒
②CH3COOH (aq)+NaOH(aq)= CH3COONa (aq)+H2O(l) △H=- 55.18 kJ·mol
略
![]() (10分)(1)今有反应
,构成燃料电池,则负极通的应是
▲ ,电极反应式为:
▲ ;正极通的应是
▲ ,电极反应式为:
▲ 。
(10分)(1)今有反应
,构成燃料电池,则负极通的应是
▲ ,电极反应式为:
▲ ;正极通的应是
▲ ,电极反应式为:
▲ 。
(2)如把KOH改为稀H2SO4作电解质,则电极反应式为:
负极: ▲ 正极: ▲ 。
知识点:原电池
(10分)
(1)H2(1分) H2-2e-+2OH-=2H2O(2分); O2 (1分)O2+4e-+2H2O=4OH-(2分)
(2)负极:H2-2e-=2H+(2分) 正极:O2+4e-+4H+=2H2O(2分)
略
(16分)(1)下列5种有机化合物:水杨酸(![]() )、苯酚(
)、苯酚(![]() )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
)、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
①其中能与Na2CO3溶液反应,但不能与FeCl3溶液发生显色反应的是 ▲ 。
②其中能与FeCl3溶液发生显色反应,但不能与NaHCO3溶液反应的是 ▲ 。
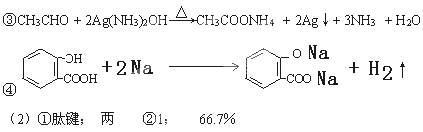
③写出乙醛与银氨溶液发生银镜反应的化学方程式 ▲ 。
④写出水杨酸与金属钠反应的化学方程式 ▲ 。
(2)①蛋白质是维持生命的重要物质,它是由氨基酸通过 ▲ 连接而成的一类高分子化合物;氨基酸因分子中含有氨基和羧基,而具有 ▲ 性。
②2008年,三鹿婴幼儿奶粉由于人为添加三聚氰胺,导致长期食用该奶粉的部分婴幼儿出现肾结石病。三聚氰胺的结构简式如下图所示。

请你预测三聚氰胺在核磁共振氢谱图(1H核磁共振谱图)中会出现 ▲ 个峰;三聚氰胺中氮元素的质量分数为 ▲ (结果用百分数表示,并保留一位小数),添加三聚氰胺会使食品中蛋白质的含量虚高。
知识点:蛋白质和核酸
(16分,每空2分)
(1)①乙酸(CH3COOH
)②苯酚(![]() )
)
略
(8分)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256KJ的热量。
(1)液态肼(N2H4)和液态双氧水反应的热化学方程式为 ▲ 。
(2)又已知H2O(l)=H2O(g);ΔH=+44kJ/mol。则8g液态肼与液态双氧水反应生成液态水时放出的热量是 ▲ kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 ▲ 。
(4)已知N2(g) + 2O2(g) ==== 2NO2(g) ΔH=+67.7kJ/mol
N2H4(g) + O2(g) ==== N2(g) + 2H2O(g) ΔH=-534kJ/mol
则肼与NO2完全反应生成氮气和液态水的热化学方程式 ▲ 。
知识点:化学反应的热效应
(8分,每空2分)
(1)N2H4(l) +2 H2O2(l)= N2(g)+4 H2O(g) ΔH=-640kJ/mol
(2)204
(3)产物是氮气和水,无污染
(4)2N2H4(g)+ 2NO2(g)= 3N2(g)+ 4H2O(l),△H = -1311.7 kJ/mol
略
(16分)黄酮醋酸(F)具有独特抗癌活性,它的合成路线如下:
已知:RCN在酸性条件下发生水解反应:
![]()

(1)写出A转化为B的化学方程式 ▲ 。
(2)F分子中有3个含氧官能团,名称分别为羰基、 ▲ 和 ▲ 。
(3)E在酸性条件下水解的产物可通过缩聚反应生成高分子化合物,该高分子化合物的结构简式为 ▲ 。
(4)写出符合下列条件的D的两种同分异构体的结构简式 ▲ 、 ▲ 。
①分子中有4种化学环境不同的氢原子;②可发生水解反应,且一种水解产物能与FeCl3发生显色反应,另一种水解产物能发生银镜反应。
(5)对羟基苯乙酸乙酯(![]() )是一种重要的医药中间体。写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选)。合成路线
)是一种重要的医药中间体。写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选)。合成路线
流程图示例如下:
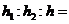
知识点:有机合成及高分子化合物
(16分)
(1)(2分)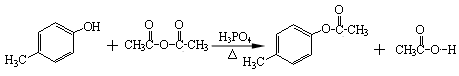
(2)醚键(2分) ;羧基(2分)
(3)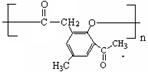 (2分)
(2分)

略
(10分)(1)A、B、C三种醇同足量的金属钠反应,在相同条件下产生相同的氢气时,消耗这三种醇的物质的量之比为3︰6︰2,则A、B、C三种醇分子里羟基数之比为 ▲ 。
(2)白藜芦醇(如图)广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。能够跟1 mol该化合物起反应的Br2或H2的最大用量分别是 ▲ 和 ▲ 。

(3)某液态一卤代烃RX 13.7g与足量的NaOH醇溶液充分共热后,冷却并加入HNO3酸化,再滴入过量的AgNO3溶液,得到淡黄色沉淀18.8g。则该卤代烃的分子式是 ▲ ,其可能的结构有 ▲ 种。
知识点:有机计算
(10分,每空2分)
(1)2:1:3(2)6mol,7mol(3)C4H9Br,4
略