下列说法中正确的是 ( )
A、s区都是金属元素 B、s区都是主族元素
C、稀有气体在ds区 D、所有非金属元素都在p区
知识点:元素周期律与元素周期表
B
略
下列各组分子中,都属于含极性键的非极性分子的是 ( )
A、C2H4 CH4 B、CO2 H2S
C、C60 C2H4 D、NH3 HCl
知识点:分子结构与性质
A
略
下列关系正确的是( )
A、沸点:戊烷 > 2,2——二甲基戊烷 > 2,3——二甲基丁烷 > 丙烷
B、同物质的量的物质燃烧耗O2量:已烷>环已烷>苯>苯甲酸
C、含氢质量分数:甲烷>乙烷>乙烯>乙炔>苯
D、密度:CCl4>CHCl3>H2O>苯
知识点:有机化学知识综合应用
D
略
某有机物X催化氧化的产物是(CH3)2CHCHO,有机物X是 ( )
A、 乙醇的同系物 B、乙醛的同系物
C、 丙醇的同分异构体 D、 丙醛的同分异构体
知识点:乙醇和醇类
A
略
按碳骨架分类,下列说法正确的是 ( )
A、CH3CH(CH3)2属于链状化合物 B、![]() 属于芳香族化合物
属于芳香族化合物
C、![]() 属于脂环化合物
D、
属于脂环化合物
D、![]() 属于芳香烃
属于芳香烃
知识点:有机化合物的分类、命名与结构特点
A
略
禁止使用兴奋剂是奥运会保证运动员比赛公平的重要举措之一。以下两种兴奋剂结构分别为:
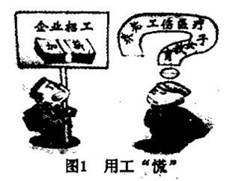
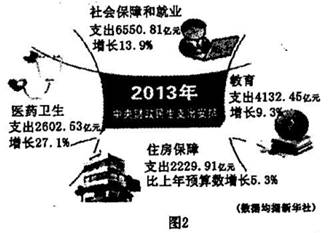
①利尿酸 ②兴奋剂X
则关于它们的说法中正确的是 ( )
A、利尿酸分子中有三种官能团 B、两种分子中的所有碳原子均不可能共平面
C、两种兴奋剂均属于芳香烃 D、两种分子均可发生加成反应
知识点:有机化学知识综合应用
D
略
下列事实与氢键有关的是 ( )
A、水加热到很高的温度都难以分解
B、水结成冰体积膨胀
C、CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
D、HF、HCl、HBr、HI的热稳定性依次减弱
知识点:分子结构与性质
B
略
共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质:①Na2O2;②SiO2;③NH4Cl;④金刚石;⑤CaH2;⑥白磷,其中含有两种结合力的组合是 ( )
A、①③⑤⑥ B、②④⑥ C、①③⑥ D、①②③⑥
知识点:分子结构与性质
C
略
A、B、C均为短周期元素,A、B同周期, A、C的最低价离子分别为A2- 和C-,B2+ 和C-具有相同的电子层结构,下列说法中正确的是 ( )
A、 C元素的最高正价为+7价 B、原子半径:A>B>C
C、离子半径:A2-> C-> B2+ D、还原性:A2-<C-
知识点:元素周期律与元素周期表
C
略
由CH3CH=CH2合成CH2(OOCCH3)CH(OOCCH3)CH2(OOCCH3)时,需要经过的反应( )
A、加成→取代→取代→取代 B、取代→加成→取代→取代
C、取代→取代→加成→取代 D、取代→取代→取代→加成
知识点:有机化学知识综合应用
B
略
不法商贩销售的“致癌大米”,已验证这种大米中含有黄曲霉毒素(AFTB),其分子结构式为如右图所示,人体的特殊基因在黄曲霉素的作用下会发生突变,有转变为肝癌的可能。一般条件下跟1mol AFTB起反应的H2或NaOH的最大量分别是( )
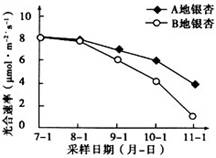
A、6mol;1mol B、5mol;1mol
C、6mol;2mol D、5mol;2mol
知识点:有机化学知识综合应用
C
略
某分子式为C10H20O2的酯,在一定条件下可发生如下图的转化过程:则符合上述条件的酯的结构可能有( )
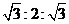
A、2种 B、8种 C、6种 D、 4种
知识点:有机合成及高分子化合物
D
略
断肠草为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构式,下列推断不正确的是( )
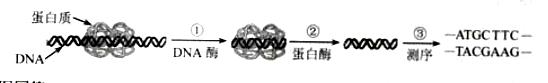
虎茸草素 异虎耳草素 异佛手相内酯 6-甲氧基白芷素
① ② ③ ④
A、①与②、③与④分别互为同分异构体
B、①、③互为同系物
C、等物质的量②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者多
D、①、②、③、④均能与氢氧化钠溶液反应
知识点:有机化合物的分类、命名与结构特点
B
略
某有机物的结构简式如图所示,关于该物质的叙述错误的是( )

A、一个分子中含有12个H原子
B、能使酸性KMnO4溶液褪色
C、苯环上的一氯代物有2种
D、1mol该物质分别与足量H2、NaOH溶液反应,消耗其物质的量均为3mol
知识点:有机化学知识综合应用
C
略
下列关于丙烯(CH3—CH =CH2)的说法正确的是 ( )
A、丙烯分子有8个σ键,1 个π键
B、丙烯分子中3个碳原子都是sp3杂化
C、丙烯分子不存在非极性键
D、丙烯分子中3个碳原子可能在同一直线上
知识点:分子结构与性质
A
略
下列各组原子,彼此性质一定相似的是 ( )
A、1s2与2s2的元素
B、M层上有两个电子与N层上有两个电子的元素
C、 2p上有一个未成对电子与3p上有一个未成对电子的元素
D、 L层上有一个空轨道和M层的p轨道上有一个空轨道的元素
知识点:原子结构与性质
D
略
有Xn+、Ym+、Zn-,已知它们各自带有的电荷数值m>n,且X、Y、Z三种原子的M电子层中的电子数均为奇数。若按X→Y→Z的顺序,下列说法中正确的是 ( )
A、它们的最高价氧化物的相应水化物的碱性依次减弱,酸性依次增强
B、它们的原子半径依次增大;
C、它们的单质在常温、常压下的密度依次减小
D、它们的最高价氧化物的水化物都是强电解质
知识点:元素周期律与元素周期表
A
略
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是 ( )
A、X与Y形成化合物时,X显负价,Y显正价
B、X的第一电离能一定大于Y
C、最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性
D、气态氢化物的稳定性:HnY小于HmX
知识点:物质的结构与性质
B
略
硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如右图是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下面还各有一个镁原子;6个硼原子位于棱柱的侧棱上,则该化合物的化学式可表示为 ( )
A.MgB B.Mg3B2
C.MgB2 D.Mg2B3
知识点:晶体结构与性质
B
略
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,
Y为元素的有关性质);
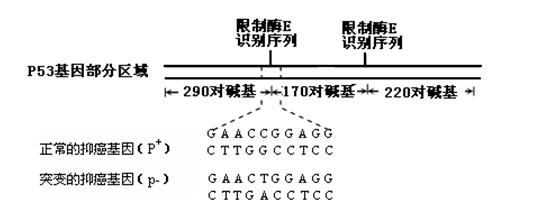

A B C D



E F G H
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数( ) (2)ⅦA族元素氢化物的沸点( )[学_(3)第三周期元素单质的熔点( ) (4)第三周期元素的最高正化合价( )
(5)IA族元素单质熔点( ) (6)F-、Na+、Mg2+、Al3+四种离子的离子半径( )
知识点:物质的结构与性质
B D E C F A
略
X、Y、Z、Q、E五种元素中,X原子核外的M层中有2个单电子且与Z同主族,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)YZ2分子的立体结构是 ;
(3)Q的元素符号是 ,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)(4)E的氢化物的熔沸点比同族其它元素氢化物的熔沸点都要高很多,原因是
。
知识点:元素周期律与元素周期表
(1) S 、 C
(2)直线型 (3)Cr 1S22S22P63S23P63d54S1 +6 (4)HF分子间存在氢键
略