下列有关原子结构和元素周期律的表述正确的是( )
A.同周期非金属元素的氧化物对应的水化物的酸性从左到右依次增强
B.第ⅠA 族元素的金属性比第ⅡA 族元素的金属性强
C.ⅦA族元素是同周期中非金属性最强的元素
D.原子序数为15的元素的最高化合价为+3
知识点:元素周期律与元素周期表
C
【考点】元素周期表的结构及其应用.
【分析】A、同周期,非金属性越强,最高价氧化物的水化物酸性越强;
B、同周期第ⅠA族元素的金属性比第ⅡA族元素的金属性强;
C、同周期元素从左到右元素的非金属性逐渐增强;
D、原子序数为15的元素为P,最外层有5个电子.
【解答】解:A、同周期,非金属性越强,最高价氧化物的水化物酸性越强,非金属元素氧化物对应水化物的酸性不具有此规律,故A错误;
B、同周期第ⅠA族元素金属性比第ⅡA族元素强,但不同周期比较,如Na(ⅠA)、Ca(ⅡA),前者金属性较弱,故B错误;
C、同周期元素从左到右元素的非金属性逐渐增强,即ⅦA族元素是同周期中非金属性最强的元素,故C正确;
D、原子序数为15的元素为P,最外层有5个电子,所以最高化合价为+5,故D错误;
故选C.
制取下列物质不以二氧化硅为原料的是( )
A.光导纤维 B.玻璃 C.粗硅 D.人造刚玉
知识点:碳族元素
D
【考点】硅和二氧化硅.
【分析】A、光导纤维主要成分为二氧化硅;
B、玻璃成分为硅酸钠、硅酸钙、二氧化硅的混合物;
C、粗硅是以二氧化硅和碳高温反应生成;
D、人造刚玉成分为氧化铝.
【解答】解:A、光导纤维主要成分为二氧化硅,以二氧化硅为原料,故A不符合;
B、玻璃成分为硅酸钠、硅酸钙、二氧化硅的混合物,以纯碱、石灰石、石英为原料,故B不符合;
C、粗硅是以二氧化硅和碳高温反应生成,以二氧化硅为原料,故C不符合;
D、人造刚玉成分为氧化铝,不以二氧化硅为原料,故D符合;
故选D.
实验室保存下列试剂的方法不正确的是( )
A.NaOH溶液存放在带橡胶塞的细口玻璃瓶中
B.氯水存放在棕色细口玻璃瓶中,并置于冷暗处
C.浓硫酸存放在带橡胶塞的细口玻璃瓶中
D.金属钠用煤油液封于广口玻璃瓶中
知识点:仪器和基本操作
C
【考点】化学试剂的存放.
【分析】A.因玻璃塞中的二氧化硅能和氢氧化钠反应有硅酸钠(Na2SiO3)生成;
B.见光易挥发、易分解的液体要储存在细口棕色试剂瓶中;
C.浓硫酸有强氧化性;
D.金属钠能与空气中的氧气和水反应,须隔离空气保存.
【解答】解:A.因玻璃塞中的二氧化硅能和氢氧化钠反应有硅酸钠(Na2SiO3)生成,硅酸钠是一种粘合剂,所以氢氧化钠溶液不能用带有磨口玻璃塞的试剂瓶盛装,而应在带橡胶塞的玻璃瓶,故A正确;
B.氯水见光易分解,且氯水是液体,所以应该存放在配有磨口塞的棕色玻璃瓶中,故B正确;
C.浓硫酸有强氧化性,能腐蚀橡胶,故C错误;
D.金属钠能与空气中的氧气和水反应,须隔离空气保存,钠和煤油不反应且大于煤油密度,所以少量的金属钠可以保存在煤油中,故D正确.
故选C.
由短周期元素组成的中学常见物质A、B、C、D、E、X,存在图中转化关系 (部分生成物和反应条件略去).下列推断不正确的是( )

A.若D与盐酸反应,可生成A和B,则X一定是H2O
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
知识点:无机框图推断
A
【考点】无机物的推断.
【分析】根据符合反应的转化关系判断,确定是否符合命题意图,可能发生反应有:
A、FeCl3  FeCl2
FeCl2  Fe
Fe  Fe3O4;
Fe3O4;
B、Na  Na2O
Na2O 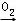 Na2O2
Na2O2  NaOH;
NaOH;
C、NaOH 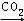 Na2CO3
Na2CO3 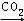 NaHCO3
NaHCO3 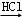 NaCl;
NaCl;
D、N2(NH3)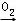 NO
NO 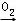 NO2
NO2 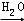 HNO3.
HNO3.
【解答】解:A、符合反应的只有:FeCl3 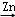 FeCl2
FeCl2 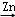 Fe
Fe 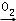 Fe3O4,X不仅可以为H2O,还可为O2,另外铁不是短周期,故A错误.
Fe3O4,X不仅可以为H2O,还可为O2,另外铁不是短周期,故A错误.
B、若D是一种强碱,A可能为Na,反应关系为:Na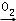 Na2O
Na2O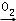 Na2O2
Na2O2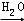 NaOH,故B正确;
NaOH,故B正确;
C、若D为NaCl,且A可与C反应生成B,则E可能是CO2,反应关系为:NaOH 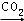 Na2CO3
Na2CO3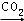 NaHCO3
NaHCO3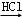 NaCl,故C正确;
NaCl,故C正确;
D、若D是一种强酸,反应关系为:N2(NH3)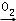 NO
NO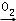 NO2
NO2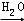 HNO3,故D正确.
HNO3,故D正确.
故选A.
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆﹣氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2﹣)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )

A.有O2放电的a极为电池的负极
B.O2﹣移向电池的正极
C.b极对应的电极反应为2H2﹣4e﹣+2O2﹣═2H2O
D.a极对应的电极反应为O2+2H2O+4e﹣═4OH﹣
知识点:原电池
C
【考点】原电池和电解池的工作原理.
【分析】该电池属于氢氧燃料电池,电池工作时的正负极反应式分别为:正极:O2+4e﹣=2O2﹣;负极:2H2﹣4e﹣+2O2﹣═2H2O,总反应为:2H2+O2=2H2O.
【解答】解:A、在燃料电池中,有O2放电的a极为原电池的正极,故A错误;
B、在燃料电池中,阴离子移向负极,所以O2﹣移向电池的负极,故B错误;
C、在燃料电池中,有H2放电的b极为电池的负极,电极反应为2H2﹣4e﹣+2O2﹣═2H2O,故C正确;
D、a极为正极,电极反应为:O2+4e﹣=2O2﹣,故D错误.
故选C
若aAn+与 bB2﹣两种离子的核外电子层结构相同,则a等于( )
A.b+n﹣2 B.b+n+2 C.b﹣n﹣2 D.b﹣n+2
知识点:原子结构与性质
B
【考点】原子核外电子排布.
【分析】aAn+与 bB2﹣两离子具有相同的电子层结构,说明二者核外电子数相同,阴离子核外电子数=质子数+所带的电荷数,阳离子核外电子数=质子数﹣所带电荷数,据此计算判断.
【解答】解:阳离子核外电子数=质子数﹣所带电荷数,所以aAn+的核外电子数为a﹣n;
阴离子核外电子数=质子数+所带的电荷数,所以bB2﹣的核外电子数为b+2;
aAn+与 bB2﹣两离子具有相同的电子层结构,说明二者核外电子数相同,所以a﹣n=b+2,即a=b+n+2.
故选:B.
已知:物质的能量越低越稳定,白磷转化为红磷是放热的,据此下列说法中正确的是( )
A.白磷转化为红磷是物理变化
B.在相同条件下红磷比白磷稳定
C.相同条件下,红磷所具有的总能量比白磷的高
D.相同质量的红磷和白磷完全燃烧放出的能量相等
知识点:化学反应与能量的变化
B
【考点】吸热反应和放热反应.
【分析】根据能量越低的物质就越稳定,白磷转化成红磷是放热反应,故红磷的能量低,红磷稳定.
【解答】解:白磷转化为红磷是放热的,说明红磷的能量低,
A.白磷转化为红磷,有新物质生成,属于化学变化,故A错误;
B.由题意知:能量越低越稳定,红磷的能量低,红磷稳定,故B正确;
C.物质的总能量高,物质不稳定,故白磷的总能量高于红磷的总能量,故C错误;
D.等质量的白磷与红磷充分燃烧,白磷放出的热量多,故D错误,
故选B.
二氧化硅(SiO2)又称硅石,是制备硅及其化合物的重要原料,其相关转化关系如图所示,下列说法正确的是( )

A.SiO2属于两性氧化物
B.盛放Na2CO3溶液的试剂瓶不能用玻璃塞
C.硅胶吸水后不能重复再生
D.图中所示转化反应都是氧化还原反应
知识点:碳族元素
B
【考点】硅和二氧化硅.
【分析】A.两性氧化物与酸、碱反应产物都只是盐和水;
B.二氧化硅能够与碱反应生成具有粘性的硅酸钠;
C.硅胶吸附水份后,可通过热脱附方式将水份除去重复使用;
D.从化合价是否发生变化的角度判断是否氧化还原反应,化合价的升降为氧化还原反应的特征.
【解答】解:A.二氧化硅与氢氟酸反应生成物为四氟化硅和水,不符合两性氧化物的概念,不是两性氧化物,故A错误;
B.碳酸钠溶液水解显碱性,能够与玻璃中二氧化硅反应生成具有粘性的硅酸钠,将瓶塞与瓶粘到一起,故B正确;
C.硅胶吸附水份后,可通过热脱附方式将水份除去重复使用,故C错误;
D.图中二氧化硅与氢氟酸、氢氧化钠、碳酸钠的反应,硅酸钠与盐酸的反应,硅酸的分解,硅酸的生成,元素的化合价都没有发生变化,是非氧化还原反应,故D错误;
故选B.
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻.X的核电荷数是Y的核外电子数的一半,Y与M可形成化合物M2Y.下列说法正确的是( )
A.还原性:X的氢化物>Y的氢化物>Z的氢化物
B.简单离子的半径:M的离子>Z的离子>Y的离子>X的离子
C.YX2、M2Y都是含有极性键的极性分子
D.Z元素的最高价氧化物的水化物的化学式为HZO4
知识点:元素周期律与元素周期表
D
【考点】位置结构性质的相互关系应用;原子结构与元素周期律的关系.
【分析】X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻.X的核电荷数是Y的核外电子数的一半,推测X为氧元素,则Y为硫元素,Z为氯元素;Y与M可形成化合物M2Y,则M为K元素,然后结合元素及其单质、化合物的性质来解答.
【解答】解:X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻.X的核电荷数是Y的核外电子数的一半,推测X为氧元素,则Y为硫元素,Z为氯元素;Y与M可形成化合物M2Y,则M为K元素
A.非金属性O>S,Cl>S,三种元素中S元素的非金属性最弱,因此其氢化物的还原性最强,则还原性为Y的氢化物>Z的氢化物>X的氢化物,故A错误;
B.电子层数越多,离子半径越大,具有相同电子排布的离子原子序数大的离子半径小,则离子的半径:Y的离子>Z的离子>M的离子>X的离子,故B错误;
C.SO2为含有极性键的极性分子,而K2S属于含有离子键的离子化合物,故C错误;
D.Z为氯元素,其最高价氧化物的水化物为HClO4,故D正确;
故选D.
短周期元素的四种离子aW3+、bX+、cY2﹣、dZ﹣,它们的电子层结构相同,下列关系正确的是( )
A.质子数c>d B.元素的非金属性Y>Z
C.氢化物的稳定性H2Y>HZ D.原子半径X>W
知识点:元素周期律与元素周期表
D
【考点】原子结构与元素周期律的关系.
【分析】短周期元素离子aW3+、bX+、cY2﹣、dZ﹣都具有相同的电子层结构,则有a﹣3=b﹣1=c+2=d+1,可知原子序数a>b>d>c,Y、Z为非金属,处于第二周期,故Y为O元素,Z为F元素,W、X为金属处于第三周期,W为Al元素,X为Na元素,结合元素周期律解答.
【解答】解:短周期元素离子aW3+、bX+、cY2﹣、dZ﹣都具有相同的电子层结构,则有a﹣3=b﹣1=c+2=d+1,可知原子a>b>d>c,Y、Z为非金属,处于第二周期,故Y为O元素,Z为F元素,W、X为金属处于第三周期,W为Al元素,X为Na元素.
A.由以上分析可知,质子数d>c,故A错误;
B.同周期自左而右非金属性减弱,故非金属性O<F,故B错误;
C.非金属性O<F,氢化物的稳定性H2O<HF,故C错误;
D.同周期自左而右原子半径减小,故原子半径Na>Al,故D正确,
故选D.
下列化学应用中不涉及氧化还原反应的是 ( )
A.Na2S水溶液在空气中变浑浊
B.生活中使用明矾净水,除去水中的悬浮颗粒
C.溶有二氧化氮的浓硝酸做火箭的助燃剂
D.漂白粉漂白有色布条
知识点:氧化还原反应
B
【考点】氧化还原反应.
【分析】有电子转移的化学反应是氧化还原反应,其特征是有元素化合价的变化,结合各选项中涉及的反应判断.
【解答】解:A.Na2S水溶液在空气中变浑浊,﹣2价S元素被氧气氧化为硫单质,反应中氧元素和硫元素化合价发生变化,属于氧化还原反应,故A不符合;
B.明矾净水,铝离子水解生成胶体,没有元素的化合价变化,不发生氧化还原反应,故B符合;
C.火箭中的助燃剂是四氧化二氮,NO2在高温下能转化生成四氧化二氮,浓硝酸容易在高温下分解成为NO2、H20和O2,有元素化合价发生变化,属于氧化还原反应,故C不符合;
D.漂白粉漂与二氧化碳和水反应生成次氯酸,次氯酸具有强氧化性而使有色布条褪色,发生氧化还原反应,故D不符合;
故选B.
下列气体,溶于水后可以生成两种酸的是( )
A.SO2 B.CO2 C.Cl2 D.NH3
知识点:卤素
C
【考点】二氧化硫的化学性质;氯气的化学性质;氨的化学性质.
【分析】A.SO2与水反应生成亚硫酸;
B.CO2与水反应生成碳酸;
C.Cl2与水反应生成盐酸和次氯酸;
D.NH3与水反应生成一水合氨.
【解答】解:A.SO2与水反应生成亚硫酸,生成一种酸,故A错误;
B.CO2与水反应生成碳酸,生成一种酸,故B错误;
C.Cl2与水反应生成盐酸和次氯酸,生成两种酸,故C正确;
D.NH3与水反应生成一水合氨,生成一种碱,故D错误;
故选C.
在N2+3H2 2NH3反应中,自反应开始至2s末,氨的浓度由0变为0.4mol•L﹣1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
2NH3反应中,自反应开始至2s末,氨的浓度由0变为0.4mol•L﹣1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
A.0.3 mol•L﹣1•s﹣1 B.0.4 mol•L﹣1•s﹣1
C.0.6 mol•L﹣1•s﹣1 D.0.8 mol•L﹣1•s﹣1
知识点:化学反应速率
A
【考点】化学反应速率和化学计量数的关系.
【分析】根据v= 计算v(NH3),再利用速率之比等于化学计量数之比计算v(H2).
计算v(NH3),再利用速率之比等于化学计量数之比计算v(H2).
【解答】解:自反应开始至2s末,氨的浓度由0变为0.4mol•L﹣1,则v(NH3)=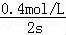 =0.2 mol•L﹣1•s﹣1,速率之比等于化学计量数之比,则v(H2)=
=0.2 mol•L﹣1•s﹣1,速率之比等于化学计量数之比,则v(H2)=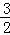 v(NH3)=0.3 mol•L﹣1•s﹣1,故选A.
v(NH3)=0.3 mol•L﹣1•s﹣1,故选A.
下面几种情况,能够形成原电池的是( )
A. B.
B. C.
C. D.
D.
知识点:原电池
C
【考点】原电池和电解池的工作原理.
【分析】根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
【解答】解:A、该装置的两个电极是相等的,不能构成原电池,故A错误;
B、该装置不能构成闭合回路,所以不能构成原电池,故B错误;
C、该装置符合原电池的构成条件,所以能形成原电池,故C正确;
D、酒精不是电解质,锌和酒精不能自发的进行氧化还原反应,所以不能构成原电池,故D错误.
故选C.
X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示.Z元素原子最外层电子数是内层电子总数的1/5.下列说法中正确的是( )
X
Y
Z
W
A.原子半径由小到大的顺序为:X<Z<Y<W
B.Y元素最高价氧化物对应的水化物化学式为H3YO4
C.X、Z两种元素的氧化物中所含化学键类型相同
D.Y最简单气态氢化物比Y相邻周期同主族元素气态氢化物沸点高
知识点:元素周期律与元素周期表
D
【考点】元素周期律和元素周期表的综合应用;原子结构与元素周期律的关系.
【分析】X、Y、Z、W为四种短周期元素,由它们在周期表位置可知,X、Y处于第二周期,Z、W处于第三周期,四元素位于连续的四个主族,Z元素原子最外层电子数是内层电子总数的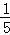 ,最外层电子数为
,最外层电子数为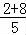 =2,故Z为Mg,则W为Al、X为C、Y为N,据此解答.
=2,故Z为Mg,则W为Al、X为C、Y为N,据此解答.
【解答】解:X、Y、Z、W为四种短周期元素,由它们在周期表位置可知,X、Y处于第二周期,Z、W处于第三周期,四元素位于连续的四个主族,Z元素原子最外层电子数是内层电子总数的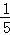 ,最外层电子数为
,最外层电子数为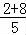 =2,故Z为Mg,则W为Al、X为C、Y为N.
=2,故Z为Mg,则W为Al、X为C、Y为N.
A.同周期从左向右原子半径在减小、同主族自上而下原子半径增大,则原子半径为Y<X<W<Z,故A错误;
B.Y为N元素,最高价氧化物对应的水化物化学式为HNO3,故B错误;
C.X的氧化物为CO、CO2,Z的氧化物为Na2O、Na2O2,CO、CO2中含有共价键,氧化钠和过氧化钠中含有离子键,故C错误;
D.Y最简单气态氢化物为氨气,由于氨气分子之间形成羟基,比Y相邻周期同主族元素气态氢化物沸点高,故D正确,
故选D.
下列说法正确的是( )
A.第ⅠA族金属单质的密度、熔沸点均随着核电荷数的增大而递增
B.金属锂在氧气中燃烧生成Li2 O2
C.金属的还原性:Li>Na>K>Rb
D.氢化物的稳定性:HF>HCl>HBr>HI
知识点:元素周期律与元素周期表
D
【考点】元素周期表的结构及其应用;元素周期律的作用;碱金属的性质.
【分析】A.第ⅠA族金属单质熔沸点从上到下减小,密度增大,但Na的密度比K的大;
B.金属锂在氧气中燃烧生成Li2O;
C.金属性越强,还原性越强;
D.非金属性越强,气态氢化物越稳定.
【解答】解:A.第ⅠA族金属从上到下金属键减弱,则单质熔沸点减小,密度增大,但Na的密度比K的大,故A错误;
B.金属锂在氧气中燃烧生成Li2O,金属性越强,氧化物越复杂,故B错误;
C.金属性越强,还原性越强,则还原性为Li<Na<K<Rb,故C错误;
D.非金属性F>Cl>Br>I,气态氢化物的稳定性为HF>HCl>HBr>HI,故D正确;
故选D.
有六种微粒,它们分别是:1940M、2040N、1840X、1940Q+、2040Y2+、1740Z﹣,它们所属元素的种类为( )
A.3种 B.4种 C.5种 D.6种
知识点:原子结构与性质
B
【考点】元素.
【分析】具有相同核电荷数(即质子数)的同一类原子的总称叫元素;元素符号的左下角表示质子数,左上角表示质量数,质子数相同中子数不同的同一类原子互称同位素,据此分析判断.
【解答】解:因为1940M、1940Q+的质子数相同,所以是同一元素,只是1940M是原子,1940Q+是带一个单位正电荷的离子;
2040N、2040Y2+的质子数相同,所以是同一元素,只是2040N是原子,2040Y2+是带两个单位正电荷的离子;
1740Z﹣是质子数为17的元素;
1840X是质子数为18的元素;
所以共有4种元素.
故选B.
下列含有非极性键的共价化合物是( )
A.HCl B.Na2O2 C.H2O2 D.H2
知识点:化学键
C
【考点】共价键的形成及共价键的主要类型.
【分析】化合物中至少含有两种元素,共价化合物中不含离子键,同种非金属元素之间以非极性键相结合,不同非金属元素之间以极性键相结合,据此解答.
【解答】解:A、HCl中只含极性共价键,故A错误;
B、Na2O2中含有离子键和非极性键,属于含有非极性键的离子化合物,故B错误;
C、H2O2中含有极性键和非极性键,属于含有非极性键的共价化合物,故C正确;
D、H2中只含有非极性共价键,属于单质,故D错误;
故选C.
设某元素的原子核内的质子数为m,中子数为n,则下述论断正确的是( )
A.不能由此确定该元素的相对原子质量
B.这种元素的相对原子质量为m+n
C.若碳原子质量为Wg,此原子的质量为(m+n)Wg
D.核内中子的总质量小于质子的总质量
知识点:原子结构与性质
A
【考点】质量数与质子数、中子数之间的相互关系.
【分析】A、元素相对原子量是指元素的平均原子质量与核素c(碳)12原子质量的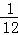 之比;
之比;
B、无法计算该元素的相对原子质量;
C、若碳原子质量为Wg,此原子的质量为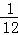 (m+n)Wg;
(m+n)Wg;
D、质子数和中子数的相对多少未知,无法判断.
【解答】解:A、题目已知某元素的一种核素的质子数和中子数,能确定该核素的相对原子质量但不能确定该元素的相对原子质量,故A正确;
B、题目已知某元素的一种核素的质子数和中子数,该核素的丰度未知导致无法计算该元素的相对原子质量,故B错误;
C、该核素的相对原子质量为m+n,该核素的相对原子质量等于该核素的质量与碳﹣12质量的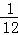 所得的比值,所以该核素的质量为
所得的比值,所以该核素的质量为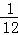 (m+n)Wg,故C错误;
(m+n)Wg,故C错误;
D、一个质子的质量和一个中子的质量相当,质子数和中子数的相对多少未知,导致无法判断,故D错误;
故选A.
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是( )
A.元素Y、Z、W离子具有相同的电子层结构,其半径依次增大
B.元素X与元素Y只能形成一种化合物
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
D.元素W、R的最高价氧化物的水化物都是强酸
知识点:元素周期律与元素周期表
C
【考点】位置结构性质的相互关系应用.
【分析】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,则A为H元素;Y原子最外层电子数是次外层电子数的3倍,Y原子有2个电子层,最外层电子数为6,故Y为O元素;根据Z、W、R处于同一周期,R与Y处于同一族,则R为S元素;Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,则Z、W原子的核外电子数之和为8+16=24,又Z、W处于同一周期,应为第三周期,原子序数W大于Z,故Z为Na,W为Al元素,结合物质性质与元素周期律解答.
【解答】解:X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,则A为H元素;Y原子最外层电子数是次外层电子数的3倍,Y原子有2个电子层,最外层电子数为6,故Y为O元素;根据Z、W、R处于同一周期,R与Y处于同一族,则R为S元素;Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,则Z、W原子的核外电子数之和为8+16=24,又Z、W处于同一周期,应为第三周期,原子序数W大于Z,故Z为Na,W为Al元素.
A.Y是O元素,Z是Na元素,W是Al元素,O2﹣、Na+、Al3+具有相同电子层结构,核外电子排布相同离子半径随着核电荷数的增加而减小,所以离子半径O2﹣>Na+>Al3+,故A错误;
B.氢元素与氧元素可以形成H2O、H2O2,故B错误;
C.非金属性越强,氢化物越稳定,非金属性O>S,所以氢化物稳定性Y>R,故C正确;
D.R为S元素,最高价氧化物的水化物是硫酸,硫酸是强酸.W为Al元素,最高价氧化物的水化物是氢氧化铝,属于两性氢氧化物,表现酸性时为弱酸,故D错误;
故选C.
如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL稀盐酸,试完成下列问题.
(1)实验中观察到的现象是 .
(2)产生上述现象的原因是 .
(3)写出有关反应的离子方程式
(4)由实验推知,MgCl2溶液和H2的总能量 (填“大于”“小于”或“等于”)镁片和盐酸的总能量.
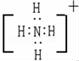
(5)写出下列物质的电子式:Mg HCl NH4+ NaOH Na2O2
.

知识点:化学反应与能量的变化
(1)溶液变浑浊,冒气泡;
(2)该反应放热,温度升高,Ca(OH)2的溶解度变小而析出;
(3)Mg+2H+═Mg2++H2↑;
(4)<;
(5)•Mg•、 、
、 、
、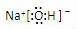 、
、 .
.
【考点】常见的能量转化形式;电子式.
【分析】(1)金属镁和酸反应生成盐和氢气;
(2)金属和酸的反应是放热反应,氢氧化钙的溶解度随着温度升高而降低,随着温度的降低而升高;
(3)金属镁和盐酸反应生成氯化镁和氢气;
(4)当反应物的能量高于生成物的能量,则反映是放热反应,反之是吸热反应;
(5)首先判断化合物是离子化合物还是共价化合物;
若是离子化合物,其电子式 由阴、阳离子的电子式组合而成,相同的离子不能合并;
若是共价化合物,其电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况.
【解答】解:(1)金属镁和盐酸反应产生大量的热,冒气泡,该热量能使氢氧化钙的溶解度降低,所以饱和石灰水中溶液变浑浊,
故答案为:溶液变浑浊,冒气泡;
(2)金属镁和盐酸反应产生大量的热,该热量能使氢氧化钙的溶解度降低,所以饱和石灰水中溶液变浑浊,
故答案为:该反应放热,温度升高,Ca(OH)2的溶解度变小而析出;
(3)金属镁和盐酸反应的实质是:Mg+2H+═Mg2++H2↑,故答案为:Mg+2H+═Mg2++H2↑;
(4)金属镁和盐酸反应产生大量的热,反应物的能量高于生成物的能量,故答案为:<;
(5)镁原子最外层有2个电子,电子式为•Mg•;原子与氯原子之间形成1对共用电子对,HCl电子式为 ;NH4+是多原子构成的阳离子,电子式要加中括号和电荷,其电子式为:
;NH4+是多原子构成的阳离子,电子式要加中括号和电荷,其电子式为: ;氢氧化钠中存在钠离子和氢氧根离子,电子式需要标出阴阳离子所带电荷,氢氧化钠的电子式为
;氢氧化钠中存在钠离子和氢氧根离子,电子式需要标出阴阳离子所带电荷,氢氧化钠的电子式为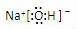 ;Na2O2是离子化合物,由Na+离子和O2﹣离子构成,Na2O2的电子式为
;Na2O2是离子化合物,由Na+离子和O2﹣离子构成,Na2O2的电子式为 ,
,
故答案为:•Mg•、 、
、 、
、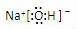 、
、 .
.
某同学实验探究氨气的还原性并进行系列实验.
(1)将光亮的紫红色铜丝绕几圈后,在酒精灯火焰上加热,等铜丝变黑后,趁热将铜丝插入疏松的氯化铵晶体里,即刻发现有白色烟雾生成,拿出铜丝后,铜丝又转变为光亮的紫红色.在焊接铜器时用氯化铵除去铜器表面的氧化铜即利用了该原理,请完成该反应:
CuO+ NH4Cl Cu+ CuCl2+ N2↑+ ( )
Cu+ CuCl2+ N2↑+ ( )
(2)利用下列装置,进行与金属氧化物MxOy反应生成M、H2、H2O,通过测量生成水的质量来测定M的相对原子质量.a中试剂是浓氨水.

①仪器a的名称为 ,仪器b中装人的试剂可以是 .
②按气流方向正确的装置连接顺序为(填序号,装置可重复使用): .
③实验结束时,应首先 (填序号).
I.熄灭A装置的酒精灯
II.停止从a中滴加液体
④若实验中准确称取金属氧化物的质量为mg,完全反应后,测得生成水的质量为ng,则M的相对原子质量为 (用含X、y、m、n的式子表示).
(3)若金属氧化物MxOy为Fe2O3,将反应后固体溶于稀硫酸,然后滴加KSCN溶液没发生明显变化.推测该固体成分可能是(将化学式填入表,你认为有几种可能填几种).
序号
固体成分(填化学式)
1
2
3
知识点:综合性实验
(1)4,2,1,1,1,4H2O;
(2)①分液漏斗;氢氧化钠固体或碱石灰;
②BDADC;
③Ⅱ;
④ 18m-16n)y/nx;
(3)
序号 | 固体成分(填化学式) |
1 | Fe |
2 | Fe和Fe2O3 |
3 |
|
【考点】探究物质的组成或测量物质的含量.
【分析】(1)依据化合价升降法进行配平;
(2)①仪器名称为分液漏斗,仪器b中加入的是氢氧化钠固体或碱石灰,吸收水蒸气得到干燥的氨气;
②从发生装置中出来的氨气带有水蒸气,必须干燥,故B接D,D接A,吸收反应生成的水用装置D,最后空气中的水不能进入装置D,所以需要装置C;
③实验结束时应首先停止从a中滴加液体,没有必要有多余的氨气制备出;
④由MxOy~YH2O关系计算得到M的相对原子质量;
(3)若金属氧化物MxOy为Fe2O3,将反应后固体溶于稀硫酸,然后滴加KSCN溶于没有发生变化,说明溶液中没有三价铁离子,反应后的固体成分可能为铁或是铁和氧化铁混合物,因为Fe+2Fe3+=3Fe2+.
【解答】解:(1)依据反应前后原子守恒可知生成物缺项为生成的水,CuO+NH4Cl Cu+CuCl2+N2↑+H2O,铜元素化合价+2价变化为0价,化合价降低,氮元素化合价﹣3价变化为0价,元素化合价升高,最小公倍数为6,则电子守恒和原子守恒配平书写得到化学方程式为:4CuO+2NH4Cl
Cu+CuCl2+N2↑+H2O,铜元素化合价+2价变化为0价,化合价降低,氮元素化合价﹣3价变化为0价,元素化合价升高,最小公倍数为6,则电子守恒和原子守恒配平书写得到化学方程式为:4CuO+2NH4Cl Cu+CuCl2+N2↑+4 H2O,
Cu+CuCl2+N2↑+4 H2O,
故答案为:4,2,1,1,1,4H2O;
(2)通过测量生成水的质量来测定M的相对原子质量.a中试剂是浓氨水,
①仪器a名称为分液漏斗用来盛放和滴加液体,a中试剂是浓氨水,仪器b中加入的是氢氧化钠固体或碱石灰,滴入浓氨水固体溶解放热使一水合氨分解生成氨气,
故答案为:分液漏斗;氢氧化钠固体或碱石灰;
②从发生装置中出来的氨气带有水蒸气,必须干燥,故B接D,D接A,吸收反应生成的水用装置D,最后空气中的水不能进入装置D,所以需要装置C,按气流方向正确的装置连接顺序为BDADC,
故答案为:BDADC;
③实验结束时应首先停止从a中滴加液体,熄灭A装置的酒精灯,
故答案为:Ⅱ;
④若实验中准确称取金属氧化物的质量为mg,完全反应后,测得生成水的质量为ng,
由MxOy~YH2O关系计算
xM+16y 18y
mg ng
M=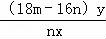
则M的相对原子质量为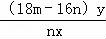 ,
,
故答案为: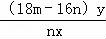 ;
;
(3)若金属氧化物MxOy为Fe2O3,将反应后固体溶于稀硫酸,然后滴加KSCN溶于没有发生变化,说明溶液中没有三价铁离子,反应后的固体成分可能为铁或是铁和氧化铁混合物,因为Fe+2Fe3+=3Fe2+,
故答案为:
序号 | 固体成分(填化学式) |
1 | Fe |
2 | Fe和Fe2O3 |
3 |
|